2NaHSO3 -to→ Na2SO3 +SO2 ↑ + H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
2NaHSO3 -to→ Na2SO3 +SO2 ↑ + H2O
Điều kiện phản ứng
- Nung nóng.
Cách thực hiện phản ứng
- Nhiệt phân NaHSO3.
Hiện tượng nhận biết phản ứng
- Có khí và hơi nước thoát ra.
Bạn có biết
- Các muối hidro sunfit đều bị nhiệt phân.

Ví dụ minh họa
Ví dụ 1:
Nhiệt phân hỗn hợp KHSO3 và NaHSO3 sau phản ứng thu được hỗn hợp chất rắn là?
A. K2SO3 và Na2SO3. C. K2O và Na2O
B. NaHSO3 và K2SO3. D. K2SO3 và Na2O.
Hướng dẫn giải
2KHSO3 
2NaHSO3 
Đáp án A.
Ví dụ 2:
Thể tích khí ở dktc thoát ra khi nhiệt phân hoàn toàn 10,4g NaHSO3 là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Hướng dẫn giải
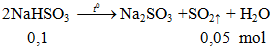
V = 0,05.22,4 = 1,12 lít.
Đáp án A.
Ví dụ 3:
Nhiệt phaan hoàn toàn 10,4 gam NaHSO3 đến khi phản ứng xảy ra hoàn toàn, sau phản ứng thu được chất rắn có khối lượng giảm so với ban đầu là
A. 1,58 gam. B, 4,10 gam. C. 2,78 gam. D. 1,00 gam.
Hướng dẫn giải
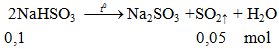
khối lượng giảm = 0,05.(64+18) = 4,1 gam.
Đáp án B.

