Trắc nghiệm Đề kiểm tra Học kì 1 Hóa 10 có đáp án
Trắc nghiệm Đề kiểm tra Học kì 1 Hóa 10 có đáp án
Với bộ bài tập trắc nghiệm Đề kiểm tra Học kì 1 Hóa 10 có đáp án sẽ giúp học sinh hệ thống lại kiến thức bài học và ôn luyện để đạt kết quả cao trong các bài thi môn Hóa lớp 10.
Câu 1: Trong tự nhiên, kali có 3 đồng vị : 1939K (x1 = 93,258%) ; 1940K (x2%) ; 1941K (x3%). Biết nguyên tử khối trung bình của kali là 39,13. Giá trị của x2 và x3 lần lượt là
A. 0,012% và 6,73%
B. 0,484% và 6,73%
C. 0,484% và 6,258%
D. 0,012% và 6,258%
Đáp án: C
x1 + x2 = 100 – 93,258 = 6,742 (1)
Ta có: (39.93,258 + 40.x1 + 41.x2)/100 = 63,546 ⇒ 40x1 + 41x2 = 275,938 (2)
Từ (1)(2) ⇒ x1 = 0,484 ; x2 = 6,258
Câu 2: Có 3 nguyên tử : 612X, 714Y, 614Z. Những nguyên tử là đồng vị của cùng một nguyên tố hóa học là
A. X và Y
B. Y và Z
C. X, Y và Z
D. X và Z
Đáp án: D
Câu 3: Nguyên tử Na (Z = 11) bị mất đi một electron thì cấu hình electron của ion tạo thành là
A. 1s22s22p63s1
B. 1s22s22p63s23p64s1
C. 1s22s22p6
D. 1s22s22p63s3
Đáp án: C
Câu 4: Cho cấu hình electron nguyên tử của Fe (Z = 26) : 1s22s22p63s23p63d64s2. Fe thuộc loại nguyên tố
A. s B. d C. f D. p
Đáp án: B
Câu 5: Có các nguyên tố hóa học: Cr (Z=24), Fe (Z=26), P (Z=15), Al (Z=13). Nguyên tố mà nguyên tử của nó có số electron độc thân lớn nhất ở trạng thái cơ bản là
A. P B. Al C. Cr D. Fe
Đáp án: C
Câu 6: Nguyên tử X có tổng số hạt proton, nowtron, electron là 115 và số khối là 80. Số lớp electron và số electron ở lớp ngoài cùng của X lần lượt là
A. 4 và 7
B. 3 và 5
C. 3 và 7
D. 4 và 1
Đáp án: A
Số electron trong nguyên tử X là 35
Cấu hình electron trong nguyên tử của X là 1s22s22p63s23p63d104s24p5 . Vậy X có 4 lớp electron và 7 electron lớp ngoài cùng.
Câu 7: Nguyên tử nguyên tố X có 12 proton và 12 nowtron. Kí hiệu nguyên tử của X là
A. 1224X
B. 1212X
C. 2424X
D. 2412X
Đáp án: A
Câu 8: Nguyên tử khối trung bình của đồng kim loại là 63,546. Đồng tồn tại trong tự nhiên với hai đồng vị là 2965Cu và 2963Cu. Thành phần phần trăm của đồng 2965Cu theo số nguyên tử là
A. 27,30% B. 26,30% C. 26,7% D. 23,70%
Đáp án: A
2965Cu (x1%) và 2963Cu (x2%)
⇒ x1 + x2 = 100 (1)
Ta có: (65x1 + 63x2)/100 = 63,546 ⇒ 65x1 + 63x2 = 6354,6 (2)
Từ (1)(2) ⇒ x1 = 27,3; x2 = 72,7
Câu 9: Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35Cl và 37Cl. Thành phần phần trăm về khối lượng của 3717Cl chứa trong HClO4 (với hidro là đồng vị 11H, oxi là đồng vị 816O) là
A. 9,40% B. 8,95% C. 9,67% D. 9,20%
Đáp án: D
35Cl(x1%) và 37Cl (x2%)
⇒ x1 + x2 = 100 (1)
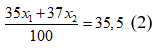
Từ(1)(2) ⇒ x1 = 75; x2 = 25
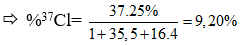
Câu 10: Cho các nguyên tố M (Z = 11), R (Z = 19) và X (Z = 3). Khả năng tạo ion từ nguyên tử của các nguyên tố trên tăng dần theo thứ tự nào sau đây?
A. M < R < X
B. X < R < M
C. X < M < R
D. M < X < R
Đáp án: C
Câu 11: Hợp chất với hidro của nguyên tố X có công thức hóa học XH3. Biết thành phần phần trăm về khối lượng của oxi trong oxit ứng với hóa trị cao nhất của X là 74,07%. Tên gọi của X là
A. nitơ B. asen C. lưu huỳnh D. photpho
Đáp án: A
Công thức oxit tương ứng với hóa trị cao nhất của X có dạng X2O5. Ta có:

Tính ra X = 14 ⇒ X là Nitơ
Câu 12: Tính chất nào sau đây của các nguyên tố không biến đổi tuần hoàn?
A. điện tích hạt nhân
B. độ âm điện
C. số electron lớp ngoài cùng
D. tính kim loại, phi kim
Đáp án: A
Câu 13: Nguyên tố R có công thức oxit ứng với hóa trị cao nhất là R2O5. Công thức hợp chất khí của R với hidro là
A. RH5 B. RH3 C. RH4 D. RH4
Đáp án: B
Câu 14: Trong bảng tuần hoàn, nguyên tố nào dưới đây có độ âm điện lớn nhất?
A. Cs B. F C. Li D. I
Đáp án: B
Câu 15: Các nguyên tố X, Y, Z, T có cấu hình electron nguyên tử lần lượt là:
X : 1s22s22p63s23p64s1
Y : 1s22s22p63s1
Z : 1s22s22p63s23p4
T : 1s22s22p4
Thứ tự tăng dần tính phi kim của các nguyên tố trên là
A. X < Z < Y < T
B. X < Y < Z < T
C. Y <X < Z < T
D. X < Y < T < Z
Đáp án: B
Câu 16: Cấu hình electron nguyên tử của các nguyên tố X, Y, Z, T như sau:
X : 1s22s22p63s23p64s2
Y : 1s22s22p63s23p63d54s2
Z : 1s22s22p5
T : 1s22s22p63s23p63d104s2
Số electron hóa trị trong nguyên tử của các nguyên tố X, Y, Z, T lần lượt là
A. 2 ; 7 ; 7 ; 12.
B. 8 ; 7 ; 7 ; 2.
C. 2 ; 2 ; 5 ; 2
D. 2 ; 7 ; 7 ; 2
Đáp án: D
Câu 17: Ion M3+ có cấu hình electron nguyên tử là [Ne]3s23p63d5. Nguyên tố M thuộc nhóm
A. VIIIB B. IIB C. VB D. IIIB
Đáp án: A
Câu 18:Cấu hình electron nguyên tử của 1939K là 1s22s22p63s23p64s1.
Kết luận nào sau đây sai?
A. Kali là nguyên tố đầu tiên của chu kì 4.
B. Kali thuộc chu kì 4, nhóm IA.
C. Kali có 20 nơtron trong hạt nhân.
D. Nguyên tử kali có 7 electron ở lớp ngoài cùng.
Đáp án: D
Câu 19: Nguyên tử Al có 3 electron hóa trị. Kiểu liên kết hóa học được hình thành khi Al liên kết với 3 nguyên tử flo là
A. liên kết kim loại.
B. liên kết cộng hóa trị có cực.
C. liên kết cộng hóa trị không cực.
D. liên kết ion.
Đáp án: D
Câu 20: Dãy nào sau đây không chứa hợp chất ion?
A. NH4Cl, OF2, H4S
B. CO2, Cl2, CCl4
C. BF3, AlF3, CH4
D. I2, CaO, CaCl2
Đáp án: B
Câu 21: Cho các hợp chất: NH3, H2O, K2S, MgCl2, Na2O, CH4.
Trong các chất trên, những chất có liên kết ion là
A. NH3, H2O, K2S, MgCl2
B. K2S, MgCl2, Na2O, CH4
C. NH3, H2O, Na2O, CH4
D. K2S, MgCl2, Na2O
Đáp án: D
Câu 22: Số oxi hóa của Cu (trong Cu), K (trong K+), Mn (trong KMnO4), N (trong NO3-) lần lượt là
A. 0, +1, +7, +5
B. +1, +5, +7, 0
C. 0, +1, +5, +7
D. +5, +1, +7, 0
Đáp án: A
Câu 23: Cho 3 ion: Na+, Mg2+, F-. Phát biểu nào sau đây sai?
A. Ba ion trên có cấu hình electron nguyên tử giống nhau.
B. Ba ion trên có số nơtron khác nhau.
C. Ba ion trên có số electron bằng nhau.
D. Ba ion trên có số proton bằng nhau.
Đáp án: D
Câu 24: Ion nào sau đây có 32 electron?
A. CO32- B. SO42- C. NH4+ D. NO3-
Đáp án: A
Câu 25: Trong các phản ứng sau, phản ứng nào NH3 không đóng vai trò là chất khử?
A. 4NH3 + 5O2 → 4NO + 6H2O
B. 2NH3 + 3Cl2 → N2 + 6HCl
C. 2NH3 + 3CuO → 3Cu + N2 + 3H2O
D. 2NH3 + H2O2 + MnSO4 → MnO2 + (NH4)2SO4
Đáp án: D
Câu 26: Cho phương trình phản ứng:
aAl + bHNO3 → cAl(NO3)3 + dNO + eH2O
Tỉ lệ a : b là
A. 2:3
B. 2:5
C. 1:3
D. 1:4
Đáp án: D
Câu 27: Cho phản ứng hóa học:
As2S3 + HNO3 + H2O → H3AsO4 + H2SO4 + NO
Sau khi cân bằng phương trình hóa học của phản ứng với hệ số tối giản, tổng hệ số của các chất tham gia phản ứng là
A. 43 B. 35 C. 31 D. 28
Đáp án: B
Câu 28: Hai nguyên tố X và Y thuộc cùng một chu kì trong bảng tuần hoàn các nguyên tố hóa học, X thuộc nhóm IIA, Y thuộc nhóm IIIA (ZX + ZY = 51).
Phát biểu nào sau đây đúng?
A. Ở nhiệt độ thường, X không khử được H2O
B. Kim loại X không khử được ion Cu2+ trong dung dịch
C. Hợp chất với oxi của X có công thức hóa học X2O7
D. Nguyên tử của nguyên tố Y có 26 proton
Đáp án: B
Theo đề ZX + ZY = 51 (1)
X và Y thuộc cùng một chu kì và hai nhóm liên tiếp (nhóm IIA và IIIA) nên ta có các trường hợp sau
ZX - ZY = 1 (2)
Hoặc ZX - ZY = 11 (3)
Kết hợp (1) và (2) ZX = 25 ZY = 26 là các nguyên tố không thuộc nhóm A (loại).
Kết hợp (1) và (3) ZX = 20 (Ca, nhóm IIA) ZY = 31 (Ga, nhóm IIIA), (chọn).
Ở nhiệt độ thường X khử được nước, không khử được ion Cu2+ trong dung dịch (do sẽ phản ứng với nước trước), hợp chất với oxi có dạng CaO, trong X có 20proton.
Câu 29: Trong phân tử M2X có tổng số hạt (proton, nơtron, electron) là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M+ lớn hơn số khối của ion X2- là 23. Tổng số hạt proton, nowtron, electron trong ion M+ nhiều hơn trong ion X2- là 31 hạt. Nhận xét nào sau đây không đúng?
A. M2X tan trong nước tạo thành dung dịch kiềm.
B. Trong các phản ứng hóa học, M chỉ thể hiện tính khử.
C. X vừa có tính oxi hóa vừa có tính khử.
D. M2X là hợp chất ion.
Đáp án: C
2(2pM + nM) + (2pX + nX) = 140
(2.2pM + 2pX) - (2nM + nX) = 44
(pM + nM) - (pX + nX) = 23
(2pM + nM -1) - (2pX + nX + 2) = 31
⇒ pM = 19 (K); pX = 8 (oxi), M2X là K2O
Câu 30: Đốt cháy hàn toàn 7,2 gam kim loại M (có hóa trị hai không đổi trong hợp chất) trong hỗn hợp khí Cl2 và O2. Sau phản ứng thu được 23,0 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (đktc). Kim loại M là
A. Mg B. Ca C. Be D. Cu
Đáp án: A
M + Cl2 → MCl2
2M + O2 → 2MO
Ta có M(x+y) = 7,2 (1)
x + 0,5y = 0,25 (2)
(M + 71)x + (M + 16)y = 23 (3)
Từ (1), (2) và (3) ⇒ x = 0,2 ; y = 0,1 và M = 24 (Mg)


