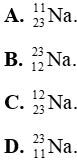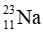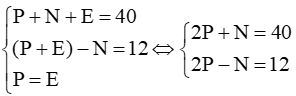Đề thi Giữa kì 1 Hóa Học lớp 10 năm 2023 có đáp án (10 đề - Sách mới)
Đề thi Giữa kì 1 Hóa Học lớp 10 năm 2023 có đáp án (10 đề - Sách mới)
Haylamdo biên soạn và sưu tầm Đề thi Giữa kì 1 Hóa Học lớp 10 năm 2023 sách mới Kết nối tri thức, Cánh diều, Chân trời sáng tạo có đáp án được tổng hợp chọn lọc từ đề thi môn Hoá học 10 của các trường trên cả nước sẽ giúp học sinh có kế hoạch ôn luyện từ đó đạt điểm cao trong các bài thi Hoá học lớp 10.
- Ma trận Đề thi Giữa kì 1 Hóa Học lớp 10 Kết nối tri thức
- Ma trận Đề thi Giữa kì 1 Hóa Học lớp 10 Cánh diều
- Ma trận Đề thi Giữa kì 1 Hóa Học lớp 10 Chân trời sáng tạo
- Đề Đề thi Giữa kì 1 Hóa Học lớp 10 (Đề 1)
- Đề Đề thi Giữa kì 1 Hóa Học lớp 10 (Đề 2)
- Đề Đề thi Giữa kì 1 Hóa Học lớp 10 (Đề 3)
- Đề Đề thi Giữa kì 1 Hóa Học lớp 10 (Đề 4)
- Đề Đề thi Giữa kì 1 Hóa Học lớp 10 (Đề 5)
- Đề Đề thi Giữa kì 1 Hóa Học lớp 10 (Đề 6)
Đề thi Giữa kì 1 Hóa học 10 Kết nối tri thức có đáp án (4 đề)
Đề thi Giữa kì 1 Hóa học 10 Chân trời sáng tạo có đáp án (4 đề)

Ma trận đề kiểm tra giữa kì I – Hóa học 10 – bộ sách KNTT
TT |
Chủ đề |
Nội dung/đơn vị kiến thức |
Mức độ nhận thức |
Tổng số câu |
Tổng % điểm |
||||||||
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
||||||||||
|
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
TN |
TL |
||||
(1) |
(2) |
(3) |
(4) |
(5) |
(6) |
(7) |
(8) |
(9) |
(10) |
(11) |
(12) |
(13) |
(14) |
1 |
Mở đầu |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 (0,25đ) |
0 |
2,5% |
|
2 |
Cấu tạo nguyên tử |
Thành phần của nguyên tử |
2 |
0 |
1 |
0 |
0 |
1 |
0 |
0 |
3 (0,75đ) |
1 (1đ) |
17,5% |
Nguyên tố hóa học |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
4 (1đ) |
0 |
10% |
||
Cấu trúc lớp vỏ electron nguyên tử |
3 |
0 |
3 |
0 |
0 |
0 |
0 |
0 |
6 (1,5đ) |
0 |
15% |
||
3 |
Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn |
Cấu tạo của bảng tuần hoàn các nguyên tố hóa học |
2 |
0 |
2 |
0 |
0 |
1 |
0 |
0 |
4 (1đ) |
1 (1đ) |
20% |
Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và nhóm |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
1 |
4 (1đ) |
1 (1đ) |
20% |
||
Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì |
2 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
3 (0,75đ) |
0 |
7,5% |
||
Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học |
2 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
3 (0,75đ) |
0 |
7,5% |
||
Tổng (câu/ điểm) |
16 (4đ) |
0 |
12 (3đ) |
0 |
0 |
2 (2đ) |
0 |
1 (1đ) |
31 (10đ) |
||||
Tỉ lệ % điểm |
40 |
0 |
30 |
0 |
0 |
20 |
0 |
10 |
100% |
||||
Tổng hợp chung |
40% |
30% |
20% |
10% |
100% |
||||||||
Lưu ý:
- Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 70% trắc nghiệm, 30% tự luận).
- Cấu trúc:
+ Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao.
+ Phần trắc nghiệm: 28 câu, 7,0 điểm (gồm 16 câu ở mức độ nhận biết;12 câu ở mức độ thông hiểu), mỗi câu 0,25 điểm;
+ Phần tự luận: 3,0 điểm (Vận dụng: 02 câu, 2,0 điểm; Vận dụng cao: 1-2 câu, 1,0 điểm).
- Các câu hỏi ở mức độ nhận biết và thông hiểu là các câu hỏi trắc nghiệm khách quan 4 lựa chọn, trong đó có duy nhất 1 lựa chọn đúng; các câu hỏi ở mức độ vận dụng và vận dụng cao là các câu hỏi tự luận.
- Với các câu hỏi TNKQ ở mức độ nhận biết và mức độ thông hiểu, mỗi câu hỏi kiểm tra, đánh giá 01 yêu cầu cần đạt của chương trình.
- Không chọn câu ở mức độ vận dụng và câu ở mức độ vận dụng cao trong cùng một đơn vị kiến thức.
Ma trận đề kiểm tra giữa kì I – Hóa học 10 – bộ sách Cánh Diều
TT |
Chủ đề |
Nội dung/đơn vị kiến thức |
Mức độ nhận thức |
Tổng số câu |
Tổng % điểm |
||||||||
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
||||||||||
|
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
TN |
TL |
||||
(1) |
(2) |
(3) |
(4) |
(5) |
(6) |
(7) |
(8) |
(9) |
(10) |
(11) |
(12) |
(13) |
(14) |
1 |
Nhập môn Hóa học |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
4 (1đ) |
0 |
10% |
|
2 |
Cấu tạo nguyên tử |
Thành phần của nguyên tử |
4 |
0 |
3 |
0 |
0 |
1 |
0 |
0 |
7 (1,75đ) |
1 (1đ) |
27,5% |
Nguyên tố hóa học |
3 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
5 (1,25đ) |
0 |
12,5% |
||
Cấu trúc lớp vỏ electron của nguyên tử |
4 |
0 |
2 |
0 |
0 |
1 |
0 |
0 |
6 (1,5đ) |
1 (1đ) |
25% |
||
3 |
Bảng tuần hoàn các nguyên tố hóa học |
Cấu tạo của bảng tuần hoàn các nguyên tố hóa học |
3 |
0 |
3 |
0 |
0 |
0 |
0 |
1 |
6 (1,5đ) |
1 (1đ) |
25% |
Tổng (câu/ điểm) |
16 (4đ) |
0 |
12 (3đ) |
0 |
0 |
2 (2đ) |
0 |
1 (1đ) |
31 (10đ) |
||||
Tỉ lệ % điểm |
40 |
0 |
30 |
0 |
0 |
20 |
0 |
10 |
100% |
||||
Tổng hợp chung |
40% |
30% |
20% |
10% |
100% |
||||||||
Lưu ý:
- Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 70% trắc nghiệm, 30% tự luận).
- Cấu trúc:
+ Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao.
+ Phần trắc nghiệm: 28 câu, 7,0 điểm (gồm 16 câu ở mức độ nhận biết;12 câu ở mức độ thông hiểu), mỗi câu 0,25 điểm;
+ Phần tự luận: 3,0 điểm (Vận dụng: 02 câu, 2,0 điểm; Vận dụng cao: 1-2 câu, 1,0 điểm).
- Các câu hỏi ở mức độ nhận biết và thông hiểu là các câu hỏi trắc nghiệm khách quan 4 lựa chọn, trong đó có duy nhất 1 lựa chọn đúng; các câu hỏi ở mức độ vận dụng và vận dụng cao là các câu hỏi tự luận.
- Với các câu hỏi TNKQ ở mức độ nhận biết và mức độ thông hiểu, mỗi câu hỏi kiểm tra, đánh giá 01 yêu cầu cần đạt của chương trình.
- Không chọn câu ở mức độ vận dụng và câu ở mức độ vận dụng cao trong cùng một đơn vị kiến thức.
Ma trận đề kiểm tra giữa kì I – Hóa học 10 – bộ sách Chân trời sáng tạo
TT |
Chủ đề |
Nội dung/đơn vị kiến thức |
Mức độ nhận thức |
Tổng số câu |
Tổng % điểm |
||||||||
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
||||||||||
|
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
TN |
TL |
||||
(1) |
(2) |
(3) |
(4) |
(5) |
(6) |
(7) |
(8) |
(9) |
(10) |
(11) |
(12) |
(13) |
(14) |
1 |
Nhập môn Hóa học |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
4 (1đ) |
0 |
10% |
|
2 |
Cấu tạo nguyên tử |
Thành phần của nguyên tử |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
4 (1đ) |
0 |
10% |
Nguyên tố hóa học |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
1 |
4 (1đ) |
1 (1đ) |
20% |
||
Mô hình nguyên tử và orbital nguyên tử |
4 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
6 (1,5đ) |
0 |
15% |
||
Lớp, phân lớp và cấu hình electron |
4 |
0 |
2 |
0 |
0 |
1 |
0 |
0 |
6 (1,5đ) |
1 (1đ) |
25% |
||
3 |
Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn |
Cấu tạo của bảng tuần hoàn các nguyên tố hóa học |
2 |
0 |
2 |
0 |
0 |
1 |
0 |
0 |
4 (1đ) |
1 (1đ) |
20% |
Tổng (câu/ điểm) |
16 (4đ) |
0 |
12 (3đ) |
0 |
0 |
2 (2đ) |
0 |
1 (1đ) |
31 (10đ) |
||||
Tỉ lệ % điểm |
40 |
0 |
30 |
0 |
0 |
20 |
0 |
10 |
100% |
||||
Tổng hợp chung |
40% |
30% |
20% |
10% |
100% |
||||||||
Lưu ý:
- Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 70% trắc nghiệm, 30% tự luận).
- Cấu trúc:
+ Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao.
+ Phần trắc nghiệm: 28 câu, 7,0 điểm (gồm 16 câu ở mức độ nhận biết;12 câu ở mức độ thông hiểu), mỗi câu 0,25 điểm;
+ Phần tự luận: 3,0 điểm (Vận dụng: 02 câu, 2,0 điểm; Vận dụng cao: 1-2 câu, 1,0 điểm).
- Các câu hỏi ở mức độ nhận biết và thông hiểu là các câu hỏi trắc nghiệm khách quan 4 lựa chọn, trong đó có duy nhất 1 lựa chọn đúng; các câu hỏi ở mức độ vận dụng và vận dụng cao là các câu hỏi tự luận.
- Với các câu hỏi TNKQ ở mức độ nhận biết và mức độ thông hiểu, mỗi câu hỏi kiểm tra, đánh giá 01 yêu cầu cần đạt của chương trình.
- Không chọn câu ở mức độ vận dụng và câu ở mức độ vận dụng cao trong cùng một đơn vị kiến thức.
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Kết nối tri thức
Năm học 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 1)
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Nội dung thuộc đối tượng nghiên cứu của hóa học là
A.quỹ đạo chuyển động của Trái đất.
B.tốc độ ánh sáng trong chân không.
C. sựtiến hóa của loài người.
D. sự biến đổi của các chất.
Câu 2: Một loại nguyên tử hydrogen có cấu tạo đơn giản nhất, chỉ tạo nên từ 1 electron và 1 proton (không chứa neutron). Phát biểu nào sau đây là đúng khi nói về nguyên tử hydrogen này?
A. Đây là nguyên tử nặng nhất trong số các nguyên tử được biết cho đến nay.
B. Khối lượng nguyên tử xấp xỉ 2 amu.
C. Hạt nhân nguyên tử có khối lượng gấp khoảng 1818 lần khối lượng lớp vỏ.
D. Kích thước của nguyên tử bằng kích thước của hạt nhân.
Câu 3: Nguyên tử gồm
A.hạt nhân chứa proton, neutron và vỏ nguyên tử chứa electron.
B.hạt nhân chứa proton, electron.
C.hạt nhân chứa proton, electron và vỏ nguyên tử chứa neutron.
D.hạt nhân và vỏ nguyên tử chứa proton.
Câu 4: Hạt nhân nguyên tử X có chứa 15 proton và 16 neutron. Số khối của hạt nhân nguyên tử X là
A. 30. B. 31. C. 32. D. 46.
Câu 5: Cho các nguyên tử sau: A (Z = 8, A = 16), B (Z = 9, A = 19), C (Z = 8, A = 17), D (Z = 7, A = 17). Trong các nguyên tử trên, các nguyên tử thuộc cùng một nguyên tố hóa học là
A. nguyên tử A và nguyên tử B.
B. nguyên tử C và nguyên tử D.
C. nguyên tử A và nguyên tử C.
D. nguyên tử B và nguyên tử C.
Câu 6: Nguyên tử nitrogen có 7 electron. Điện tích hạt nhân của nguyên tử này là
A.+7. B.-7. C.7+. D.7.
Câu 7: Một nguyên tử có chứa 11 electron và 12 neutron. Kí hiệu nguyên tử này là
Câu 8: Trong tự nhiên, lithium có 2 đồng vị là 7Li và 6Li. Nguyên tử khối trung bình của Li là 6,93. Phần trăm số nguyên tử của đồng vị 7Li là
A.93%. B.7%. C.78%. D.22%.
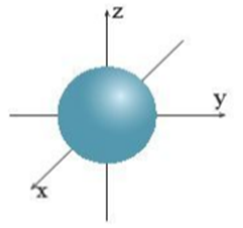
Câu 9: Hình ảnh dưới đây chỉ hình dạng của orbital nào?
A.Orbital s.
B.Orbital p.
C.Orbital d.
D.Orbital f.
Câu 10: Sự phân bố electron vào các lớp và phân lớp căn cứ vào
A. số khối.
B. điện tích hạt nhân.
C. nguyên tử khối.
D. mức năng lượng electron.
Câu 11: Lớp M chứa số electron tối đa là
A. 3. B.6. C. 9. D. 18.
Câu 12: Lớp electron thứ 4 còn được gọi là
A. Lớp K.
B. Lớp M.
C. Lớp N.
D. Lớp L.
Câu 13: Cấu hình electron của nguyên tử sulfur (Z = 16) là
A. 1s22s22p63s23p3.
B. 1s22s22p63s23p5.
C. 1s22s22p63s23p4.
D. 1s22s22p63s23p6.
Câu 14: Ở trạng thái cơ bản, nguyên tử của nguyên tố phosphorus (Z = 15) có số electron độc thân là
A. 1. B. 2. C. 3. D. 4.
Câu 15: Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là 3s2. Số hiệu nguyên tử của nguyên tố X là
A. 12. B. 13. C. 11. D. 14.
Câu 16: Số hiệu nguyên tử của nguyên tố hoá học bằng
A. số thứ tự của nhóm.
B. số thứ tự của chu kì.
C. số thứ tự của ô nguyên tố.
D. số electron lớp ngoài cùng của nguyên tử.
Câu 17: Cấu hình electron của nguyên tử oxygen là 1s22s22p4. Vị trí của oxygen trong bảng tuần hoàn là
A. ô số 6, chu kì 2, nhóm VIA.
B. ô số 6, chu kì 3, nhóm VIB.
C. ô số 8, chu kì 2, nhóm VIB.
D. ô số 8, chu kì 2, nhóm VIA.
Câu 18: Nguyên tố aluminium (Al) có số hiệu nguyên tử là 13. Al thuộc khối nguyên tố
A.s. B.p. C.d. D.f.
Câu 19: Nguyên tử của nguyên tố nào sau đây có tính phi kim mạnh nhất?
A. Fluorine.
B. Bromine.
C. Phosphorus.
D. Iodine.
Câu 20: Phát biểu nào sau đây là đúng về xu hướng biến đổi tính kim loại trong bảng tuần hoàn các nguyên tố hóa học?
A. Tính kim loại của các nguyên tố tăng theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
B. Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
C. Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
D. Tính kim loại tăng dần theo chiều từ trái sang phải trong một chu kì và giảm dần từ trên xuống dưới trong một nhóm.
Câu 21: Độ âm điện là
A. đại lượng đặc trưng cho khả năng nhường electron của nguyên tử một nguyên tố khi tạo thành liên kết hóa học.
B. đại lượng đặc trưng cho khả năng tạo thành phân tử.
C. đại lượng đặc trưng cho khả năng tạo thành nguyên tử.
D. đại lượng đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố khi tạo thành liên kết hóa học.
Câu 22: Sulfur là nguyên tố hóa học thuộc nhóm VIA của bảng tuần hoàn. Công thức oxide cao nhất của sulfur là
A. S2O6. B. SO3. C. SO6. D. SO2.
Câu 23: Oxide nào sau đây có tính base mạnh nhất?
A. MgO.
B. Cl2O7.
C. SO3.
D. Na2O.
Câu 24: Trong các chất dưới đây, chất nào có tính acid yếu nhất?
A. H3PO4.
B. H2SiO3.
C. H2SO4.
D. HClO4.
Câu 25: Các nguyên tố kim loại thuộc nhóm IA còn được gọi là
A. nhóm kim loại kiềm.
B. nhóm kim loại kiềm thổ.
C. nhóm halogen.
D. nhóm nguyên tố khí hiếm.
Câu 26: Nguyên tố M thuộc chu kì 3, nhóm VA của bảng tuần hoàn. Số hiệu nguyên tử của nguyên tố M là
A. 16. B. 14. C. 15. D. 13.
Câu 27: Cấu hình eletron lớp ngoài cùng của nguyên tố X là 3s1. Oxide cao nhất của X có tính chất nào sau đây?
A. Tính kim loại.
B. Tính phi kim.
C. Tính acid.
D. Tính base.
Câu 28: Sắp xếp tính base của NaOH, Mg(OH)2, Al(OH)3 theo chiều giảm dần là
A.NaOH, Mg(OH)2, Al(OH)3.
B.Al(OH)3, Mg(OH)2, NaOH.
C.Mg(OH)2, Al(OH)3, NaOH.
D.Mg(OH)2, NaOH, Al(OH)3.
Phần II: Tự luận (3 điểm)
Câu 1 (1 điểm): Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn và có tổng số đơn vị điện tích hạt nhân là 25. Xác định vị trí (ô, chu kì, nhóm) của hai nguyên tố A và B trong bảng tuần hoàn (có giải thích ngắn gọn cách xác định).
Câu 2 (1 điểm): Nguyên tử của nguyên tố X có tổng số hạt (proton, electron, neutron) là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12.
Tính số hạt mỗi loại (proton, electron, neutron) trong nguyên tử X.
Câu 3 (1 điểm): Cho các nguyên tố sau: Li (Z = 3), O (Z = 8), F (Z = 9), Na (Z = 11).
Sắp xếp các nguyên tố trên theo chiều tăng dần bán kính nguyên tử, có giải thích ngắn gọn cách sắp xếp.
Hướng dẫn giải:
Phần I: Trắc nghiệm
1-D |
2-C |
3-A |
4-B |
5-C |
6-A |
7-D |
8-A |
9-A |
10-D |
11-D |
12-C |
13-C |
14-C |
15-A |
16-C |
17-D |
18-B |
19-A |
20-B |
21-D |
22-B |
23-D |
24-B |
25-B |
26-C |
27-D |
28-A |
Câu 1:
Đáp án đúng là: D
Hóa học nghiên cứu về thành phần, cấu trúc, tính chất, sự biến đổi của các chất và các hiện tượng kèm theo.
Câu 2:
Đáp án đúng là: C
Nguyên tử hydrogen này có:
Khối lượng hạt nhân = khối lượng hạt proton ≈ 1 amu
Khối lượng lớp vỏ = khối lượng hạt electron ≈ 0,00055 amu
⇒ Khối lượng hạt nhân nguyên tử lớn hơn khối lượng lớp vỏ là ≈ 1818 lần.
Phát biểu Asai vì:Khối lượng nguyên tử xấp xỉ 1 amu, là nguyên tử nhẹ nhất trong số các nguyên tử được biết cho đến nay.
Phát biểu B sai vì:Khối lượng nguyên tử xấp xỉ 1 amu.
Phát biểu D sai vì: Kích thước của hạt nhân rất nhỏ so với kích thước của nguyên tử.
Câu 3:
Đáp án đúng là: A
Nguyên tử gồm hạt nhân chứa proton, neutron và vỏ nguyên tử chứa electron.
Câu 4:
Đáp án đúng là: B
Số khối của hạt nhân nguyên tử X là: A = Z + N = 15 + 16 = 31.
Câu 5:
Đáp án đúng là: C
Các nguyên tử thuộc cùng một nguyên tử hóa học khi có cùng số đơn vị điện tích hạt nhân (Z) ⇒ Các nguyên tử A và C thuộc cùng một nguyên tố hóa học (đều có Z = 8).
Câu 6:
Đáp án đúng là: A
Nguyên tử nitrogen có số proton = số electron = 7.
Điện tích hạt nhân nguyên tử là: +7.
Câu 7:
Đáp án đúng là: D
Số hiệu nguyên tử (Z) = số proton = số electron = 11.
Số khối (A) = Z + N = 11 + 12 = 23.
Vậy kí hiệu của nguyên tử X là
Câu 8:
Đáp án đúng là: A
Gọi phần trăm số nguyên tử của đồng vị 7Li là x% ⇒ phần trăm số nguyên tử của đồng vị 6Li là (100 − x)%
Ta có: ⇒ x = 93
Phần trăm số nguyên tử của đồng vị 7Li là 93%.
Câu 9:
Đáp án đúng là: A
AO s là orbital có dạng hình cầu.
Câu 10:
Đáp án đúng là: D
Sự phân bố electron vào các lớp và phân lớp căn cứ vàomức năng lượng electron.
Câu 11:
Đáp án đúng là: D
Lớp M (n = 3) chứa số electron tối đa là: 2.32 =18 electron.
Câu 12:
Đáp án đúng là: C
Số thứ tự lớp và tên gọi là các chữ cái in hoa như bảng sau:
n |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
Tên lớp |
K |
L |
M |
N |
O |
P |
Q |
Câu 13:
Đáp án đúng là: C
Nguyên tử sulfur có Z = 16 nên nguyên tử có 16 electron.
⇒ Cấu hình electron là 1s22s22p63s23p4.
Câu 14:
Đáp án đúng là: C
Cấu hình electron nguyên tử P (Z = 15): 1s22s22p63s23p3.
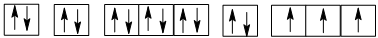
Sự phân bố các electron vào AO:
Nguyên tử của nguyên tố phosphorus (Z = 15) có số electron độc thân là 3.
Câu 15:
Đáp án đúng là: A
Cấu hình electron của X là: 1s22s22p63s2.
Vậy số hiệu nguyên tử X = số electron = 12.
Câu 16:
Đáp án đúng là: C
Số hiệu nguyên tử của nguyên tố hoá học bằng số thứ tự của ô nguyên tố.
Câu 17:
Đáp án đúng là: D
Oxygen có 8 electron nên số hiệu nguyên tử là 8, oxygen ở ô số 8 trong bảng tuần hoàn.
Oxygen ở chu kì 2 (do có 2 lớp electron); nhóm VIA (do 6 electron hóa trị, nguyên tố p).
Câu 18:
Đáp án đúng là: B
Cấu hình electron nguyên tử của Al là: 1s22s22p63s23p1 ⇒ Al thuộc khối nguyên tố p.
Câu 19:
Đáp án đúng là: A
Trong bảng tuần hoàn, fluorine có độ âm điện lớn nhất nên có tính phi kim mạnh nhất.
Câu 20:
Đáp án đúng là: B
Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
Câu 21:
Đáp án đúng là: D
Độ âm điện là đại lượng đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố khi tạo thành liên kết hóa học.
Câu 22:
Đáp án đúng là: B
Sulfur là nguyên tố nhóm VIA nên có hóa trị cao nhất trong hợp chất là VI.
Công thức oxide cao nhất của sulfur là SO3.
Câu 23:
Đáp án đúng là: D
Na, Cl, S, Mg đều thuộc chu kì 3 trong bảng tuần hoàn. Na thuộc nhóm IA (hay kim loại ở đầu chu kì 3) nên Na2O có tính base mạnh nhất trong số các oxide đề bài cho.
Câu 24:
Đáp án đúng là: B
Nhóm |
IVA |
VA |
VIA |
VIIA |
Nguyên tố |
Si |
P |
S |
Cl |
Công thức hydroxide |
H2SiO3 |
H3PO4 |
H2SO4 |
HClO4 |
Theo quy luật biến đổi tính chất trong một chu kì ta có acid H2SiO3 có tính acid yếu nhất.
Câu 25:
Đáp án đúng là: B
Các nguyên tố kim loại thuộc nhóm IA còn được gọi là nhóm kim loại kiềm.
Câu 26:
Đáp án đúng là: C
Nguyên tố M thuộc chu kì 3, nhóm VA.
Cấu hình electron của nguyên tố M là: 1s22s22p63s23p3
Vậy số hiệu nguyên tử của nguyên tố M là: Z = 15.
Câu 27:
Đáp án đúng là: D
Cấu hình eletron lớp ngoài cùng của nguyên tố X là 3s1 suy ra X ở nhóm IA trong bảng tuần hoàn.
Oxide cao nhất của X là Na2O, có tính base mạnh.
Câu 28:
Đáp án đúng là: A
Na, Mg, Al cùng thuộc chu kì 3 trong bảng tuần hoàn, theo chiều tăng dần của điện tích hạt nhân, tính base của hydroxide có xu hướng giảm dần theo thứ tự NaOH, Mg(OH)2, Al(OH)3.
Phần II: Tự luận
Câu 1:
a) Gọi số đơn vị điện tích hạt nhân nguyên tử của nguyên tố A là Z.
Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn nên số đơn vị điện tích hạt nhân của nguyên tố B là Z + 1.
Theo bài: Z + (Z + 1) = 25 ⇒ Z = 12
⇒ Nguyên tử A có 12 electron, nguyên tử B có 13 electron.
+ Cấu hình electron của A là 1s22s22p63s2.
Nguyên tố A thuộc ô số 12 (do Z = 12), chu kì 3 (do có 3 lớp electron), nhóm IIA (do 2 electron hóa trị, nguyên tố s).
+ Cấu hình electron của B là 1s22s22p63s23p1.
Nguyên tố B thuộc ô số 13 (do Z =13), chu kì 3 (do có 3 lớp electron), nhóm IIIA (do 3 electron hóa trị, nguyên tố p).
Câu 2:
Gọi số hạt proton, neutron và electron trong X lần lượt là P, N và E.
Nguyên tử trung hòa về điện nên P = E.
Theo bài ra ta có hệ phương trình:
Giải hệ phương trình được:
P = E = 13 và N = 14.
Câu 3:
Ta có:
+ Li, O, F cùng thuộc chu kì 2 trong bảng tuần hoàn. Trong một chu kì theo chiều tăng dần điện tích hạt nhân nguyên tử, bán kính nguyên tử giảm dần ⇒ bán kính nguyên tử:
F < O < Li (1)
+ Li và Na cùng thuộc nhóm IA. Trong một nhóm, theo chiều tăng dần điện tích hạt nhân nguyên tử, bán kính nguyên tử tăng dần ⇒ bán kính nguyên tử: Li < Na (2)
Vậy dãy gồm các nguyên tố được sắp xếp theo chiều tăng dần bán kính nguyên tử là:
F, O, Li, Na.
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Cánh Diều
Năm học 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 2)
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Nội dung nào dưới đây là đối tượng nghiên cứu của hóa học?
A. Sự lớn lên và sinh sản của tế bào.
B. Tốc độ của ánh sáng trong chân không.
C. Ứng dụng của chất.
D. Sự hình thành hệ Mặt Trời.
Câu 2: Phương pháp nghiên cứu lí thuyết là
A. sử dụng những định luật, nguyên lí, quy tắc, cơ chế, mô hình … để tiếp tục làm rõ những vấn đề của lí thuyết hóa học.
B. nghiên cứu những vấn đề dựa trên kết quả thí nghiệm, khảo sát, thu thập số liệu, phân tích, định lượng…
C. giải quyết các vấn đề hóa học được ứng dụng trong các lĩnh vực khác nhau.
D. nghiên cứu thành phần, cấu trúc, tính chất và sự biến đổi của chất.
Câu 3: Trong các chất: magnesium, nitrogen, oxygen, sodium chloride. Hợp chất là
A.magnesium.
B.nitrogen.
C.oxygen.
D.sodium chloride.
Câu 4: Thứ tự các bước trong phương pháp nghiên cứu hóa học là
A.xác định vấn đề nghiên cứu; nêu giả thuyết khoa học; thực hiện nghiên cứu; viết báo cáo: thảo luận kết quả và kết luận vấn đề.
B.nêu giả thuyết khoa học; xác định vấn đề nghiên cứu; thực hiện nghiên cứu; viết báo cáo: thảo luận kết quả và kết luận vấn đề.
C.xác định vấn đề nghiên cứu; nêu giả thuyết khoa học; viết báo cáo: thảo luận kết quả và kết luận vấn đề; thực hiện nghiên cứu.
D.nêu giả thuyết khoa học; xác định vấn đề nghiên cứu; viết báo cáo: thảo luận kết quả và kết luận vấn đề; thực hiện nghiên cứu.
Câu 5: Các hạt cấu tạo nên hạt nhân của hầu hết các nguyên tử là
A. electron và neutron.
B. proton và neutron.
C. neutron và electron.
D. electron, proton và neutron.
Câu 6: Phát biểu nào sai khi nói về neutron?
A. Tồn tại trong hạt nhân nguyên tử.
B. Có khối lượng bằng khối lượng proton.
C. Có khối lượng lớn hơn khối lượng electron.
D. Không mang điện.
Câu 7: Nguyên tử aluminium có 13 proton và 14 neutron. Số hạt mang điện có trong nguyên tử này là
A. 13. B. 14. C. 27. D. 26.
Câu 8: Hạt electron có điện tích là
A. 1,602 × 10-19 C.
B. -1,602 × 10-19 C.
C. +1,602 × 10-19 C.
D. -1,602 × 1019 C.
Câu 9: Nguyên tử carbon có điện tích hạt nhân là +6. Số electron của nguyên tử này là
A. 6. B. 12. C. 18. D. 24.
Câu 10: Nếu xem nguyên tử như một quả cầu, có bán kính khoảng 10-10 m thì bán kính hạt nhân nguyên tử vào khoảng
A. 10-8 m.
B. 10-14 m.
C. 10-12 m.
D. 104 m.
Câu 11: Đơn vị khối lượng nguyên tử kí hiệu là
A. meV.
B. amu.
C. nanometre.
D. angstrom.
Câu 12: Số đơn vị điện tích hạt nhân nguyên tử (kí hiệu là Z) của một nguyên tố gọi là
A. số khối.
B. nguyên tử khối.
C. số hiệu nguyên tử.
D. số neutron.
Câu 13: Số hạt electron của nguyên tử có kí kiệu 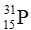
A. 31. B. 16. C. 15. D. 30.
Câu 14: Cho các nguyên tử sau: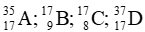
A. A và B.
B. B và C
C. C và D.
D. A và D.
Câu 15: Từ hai đồng vị hydrogen (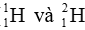
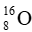
A. 1. B. 2. C. 3. D. 4.
Câu 16: Nguyên tử carbon có hai đồng vị bền: 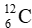
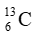
A. 12,50.
B. 12,02.
C. 12,01.
D. 12,06.
Câu 17: Orbital s có dạng
A. hình tròn.
B. hình số 8 nổi.
C. hình cầu.
D. hình bầu dục.
Câu 18: Lớp M có số electron tối đa bằng
A. 3. B. 4. C. 9. D. 18.
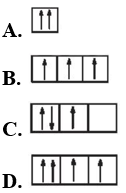
Câu 19: Sự phân bố electron theo ô orbital nào dưới đây là đúng?
Câu 20: Cấu hình electron của nguyên tử Cl (Z = 17) là
A. 1s22s22p63s23p6.
B. 1s22s22p63s23p5.
C. 1s22s22p63s23p3.
D. 1s22s22p63s23p4.
Câu 21: Nguyên tố X có số hiệu nguyên tử bằng 14. Electron cuối cùng của nguyên tử nguyên tố X điền vào lớp, phân lớp nào sau đây?
A. K, s.
B. L, p.
C. M, p.
D. N, d.
Câu 22: Phân lớp chứa đủ số electron tối đa được gọi là
A. phân lớp bão hòa.
B. phân lớp bán bão hòa.
C. phân lớp nửa bão hòa.
D. phân lớp chưa bão hòa.
Câu 23: Ô nguyên tố trong bảng tuần hoàn không cho biết thông tin nào sau đây?
A. Kí hiệu nguyên tố.
B. Tên nguyên tố.
C.Số hiệu nguyên tử.
D. Số khối của hạt nhân.
Câu 24: Chu kì 4 của bảng tuần hoàn có số nguyên tố là
A. 2 nguyên tố.
B. 18 nguyên tố.
C. 32 nguyên tố.
D. 8 nguyên tố.
Câu 25: Nguyên tử X có cấu hình electron [Ne]3s23p1. Vị trí của X trong bảng hệ thống tuần hoàn là
A. số thứ tự 3, chu kì 3, nhóm IIIA.
B. số thứ tự 11, chu kì 3, nhóm IIIA.
C. số thứ tự 13, chu kì 2, nhóm IA.
D. số thứ tự 13, chu kì 3, nhóm IIIA.
Câu 26: Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố X là 3s2. Số thứ tự nguyên tố X trong bảng tuần hoàn là
A. 12. B. 13. C. 11. D. 14.
Câu 27: Cho cấu hình electron các nguyên tố sau đây: Na: [Ne]3s1; Cr: [Ar]3d54s1;Br: [Ar]3d104s24p5; F: 1s22s22p5; Cu: [Ar]3d104s1. Số nguyên tố thuộc khối s trong các nguyên tố trên là
A. 0. B. 1. C. 2. D. 3.
Câu 28: Bảng tuần hoàn hiện nay có số cột, số nhóm A và số nhóm B lần lượt là
A. 18, 8, 8.
B. 18, 8, 10.
C. 18, 10, 8.
D. 16, 8, 8.
Phần II: Tự luận (3 điểm)
Câu 1 (1 điểm): Nguyên tử X có tổng số các loại hạt bằng 52, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt.
a) Xác định thành phần các hạt cấu tạo nên nguyên tử X.
b) Viết kí hiệu nguyên tử X.
Câu 2 (1 điểm): Nguyên tử của nguyên tố A có electron ở mức năng lượng cao nhất là 3p. Nguyên tử của nguyên tố B có một electron ở lớp ngoài cùng 4s. Nguyên tử A và B có số electron hơn kém nhau là 3.
a) Viết cấu hình electron nguyên tử A, B.
b) Biểu diễn cấu hình electron A, B theo ô orbital và cho biết số electron độc thân có trong mỗi nguyên tử này.
Câu 3 (1 điểm): Hai nguyên tố X và Y đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn, có tổng số điện tích hạt nhân bằng 25. Biết ZX < ZY, hãy xác định vị trí của X, Y trong bảng tuần hoàn (có giải thích ngắn gọn cách xác định).
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Chân trời sáng tạo
Năm học 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 3)
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Nội dung nào dưới đây thuộc đối tượng nghiên cứu của Hóa học?
A. Sự bài tiết mồ hôi qua da.
B. Sự tự quay của Trái Đất quanh trục riêng.
C. Tốc độ của ánh sáng trong chân không.
D. Sự phân hủy của đá vôi.
Câu 2: Loại liên kết trong phân tử nước là
A. liên kết ion.
B. liên kết cộng hóa trị.
C. liên kết kim loại.
D. liên kết pi.
Câu 3: Khí thải chứa SO2, SO3, NO2, … cũng như nước thải chứa ion kim loại nặng như Fe3+, Cu2+, … ở một số nhà máy thường được xử lí bằng cách cho qua dung dịch nào sau đây?
A. CaCl2.
B. Ca(OH)2.
C. NaCl.
D. K2SO4.
Câu 4: Hiện tượng nào sau đây là hiện tượng hóa học?
A. Mở nút chai nước giải khát loại có gas thấy có bọt sủi lên.
B. Sắt bị nam châm hút ra khỏi hỗn hợp gồm bột sắt (iron) và lưu huỳnh (sulfur).
C. Đun nóng hỗn hợp gồm sắt và lưu huỳnh trong ống nghiệm, hỗn hợp nóng sáng lên và chuyển dần thành chất rắn màu đen.
D. Thủy tinh nóng chảy được thổi thành bình cầu.
Câu 5: Hạt mang điện trong hạt nhân nguyên tử là
A. Electron.
B. Proton.
C. Neutron.
D. Neutron và electron.
Câu 6: Trường hợp nào sau đây có sự tương ứng giữa hạt cơ bản với khối lượng và điện tích của chúng?
A. Proton, m ≈ 0,00055 amu, q = +1.
B. Neutron, m ≈ 1 amu, q = 0.
C. Electron, m ≈ 1 amu, q = -1.
D. Proton, m≈ 1 amu, q = -1.
Câu 7: Nguyên tử oxygen có 8 electron, hạt nhân nguyên tử này có điện tích là
A.8+. B.+ 8. C.8. D.-8.
Câu 8: Khẳng định nào sau đây đúng?
A.Kích thước nguyên tử xấp xỉ bằng kích thước hạt nhân.
B.Kích thước nguyên tử bằng khoảng 3 đến 5 lần kích thước hạt nhân.
C.Kích thước nguyên tử bằng khoảng 10 lần kích thước hạt nhân.
D.Kích thước nguyên tử bằng khoảng 10000 đến 100000 lần kích thước hạt nhân.
Câu 9: Nguyên tố hóa học là tập hợp những nguyên tử có cùng
A. số neutron và proton.
B. số neutron.
C. số proton.
D. số khối.
Câu 10: Số đơn vị điện tích hạt nhân của nguyên tử có kí hiệu 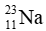
A. 23. B. 24. C. 25. D. 11.
Câu 11: Nhóm các nguyên tử nào dưới đây thuộc cùng một nguyên tố hóa học ?
Câu 12: Oxygen có ba đồng vị với tỉ lệ % số nguyên tử tương ứng là 16O (99,757%), 17O (0,038%), 18O (0,205%). Nguyên tử khối trung bình của oxygen là
A. 16,0. B. 16,2. C. 17,0. D. 18,0.
Câu 13: Nguyên tố lưu huỳnh (sulfur) nằm ở ô thứ 16 trong bảng hệ thống tuần hoàn. Biết rằng các electron của nguyên tử lưu huỳnh được phân bố trên 3 lớp electron (K, L, M). Số electron ở lớp L trong nguyên tử lưu huỳnh là
A. 6. B. 8. C. 10. D. 4.
Câu 14: Electron thuộc lớp nào sau đây liên kết chặt chẽ với hạt nhân nhất?
A.Lớp K.
B. Lớp L.
C. Lớp N.
D. Lớp M.
Câu 15: Orbital nguyên tử là
A. Đám mây chứa electron dạng hình cầu.
B. Đám mây chứa electron có dạng hình số 8 nổi.
C. Khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron lớn nhất.
D. Quỹ đạo chuyển động của electron quay quanh hạt nhân có kích thước và năng lượng xác định.
Câu 16: Orbital p có dạng hình gì?
A. Hình cầu.
B. Hình tròn.
C. Hình thoi.
D. Hình số tám nổi.
Câu 17: Các electron của nguyên tố X được phân bố trên 2 lớp, lớp thứ 2 có 7 electron. Số hiệu nguyên tử của nguyên tố X là
A. 7. B. 8. C. 9. D.10.
Câu 18: Electron thuộc lớp nào sau đây liên kết chặt chẽ với hạt nhân nhất?
A. lớp K.
B. lớp L.
C. lớp N.
D. lớp M.
Câu 19: Số electron tối đa trong phân lớp p là
A. 2. B. 10. C. 6. D. 14.
Câu 20: Cấu hình electron nào sau đây là của nguyên tử nguyên tố phi kim?
A. 1s2 2s2 2p6 3s2 3p5.
B. 1s2 2s2 2p6 3s2 3p1.
C. 1s2 2s2 2p6 3s2 3p6.
D. 1s2 2s2 2p6 3s2.
Câu 21: Chọn phát biểu đúng về electron s?
A.Electron s là electron chuyển động chủ yếu trong khu vực không gian hình cầu;
B.Electron s là electron chỉ chuyển động trên một mặt cầu;
C.Electron s là electron chỉ chuyển động trên một đường tròn;
D.Electron s là electron chỉ chuyển động trong khu vực không gian hình cầu.
Câu 22: Số electron tối đa ở lớp thứ n (n ≤ 4) là
A.n. B.2n. C.n2. D.2n2.
Câu 23: Lớp N có các phân lớp được kí hiệu lần lượt là
A.3s, 3p, 3d.
B.4s, 4p, 4d.
C.4s, 4p, 4d, 4f.
D.1s, 2s, 3s, 4s.
Câu 24: Hạt nhân nguyên tử X có 17 proton, 18 neutron. Cấu hình electron nguyên tử X là
A. 1s22s22p63s23p6
B. 1s22s22p63s23p63d1.
C. 1s22s22p63s23p64s1.
D. 1s22s22p63s23p5.
Câu 25: Số nguyên tố trong chu kì 3 và chu kì 5 của bảng tuần hoàn lần lượt là
A. 8 và 18.
B. 8 và 8.
C. 18 và 18.
D. 18 và 32.
Câu 26: Chu kì là tập hợp các nguyên tố, mà nguyên tử của các nguyên tố này có cùng
A. số electron.
B. số lớp electron.
C. số electron hóa trị
D. số electron ở lớp ngoài cùng.
Câu 27: Nguyên tố A có số hiệu nguyên tử là 18, vị trí của A trong bảng tuần hoàn là
A. chu kì 3, nhóm VIB.
B. chu kì 3, nhóm VIIIA.
C. chu kì 3, nhóm VIA.
D. chu kì 3, nhóm VIIIB.
Câu 28: Một nguyên tố hóa học X ở chu kì 3, nhóm VA. Cấu hình electron của nguyên tử X là
A.1s22s22p63s23p2.
B. 1s22s22p63s23p4.
C. 1s22s22p63s23p3.
D. 1s22s22p63s23p5.
Phần II: Tự luận (3 điểm)
Câu 1 (1 điểm): Cho các nguyên tử nguyên tố sau: Na (Z = 11); Cl (Z = 17).
a) Viết cấu hình electron, biểu diễn cấu hình electron theo ô orbital và xác định số electron độc thân của mỗi nguyên tử trên.
b) Từ cấu hình electron, dự đoán tính chất hóa học của Mg; S (có giải thích ngắn gọn).
Câu 2 (1 điểm): Hai nguyên tố A, B (ZB > ZA) đứng liên tiếp nhau trong một chu kì của bảng tuần hoàn, có tổng số đơn vị điện tích hạt nhân là 17. Xác định vị trí nguyên tố A, B trong bảng tuần hoàn (có giải thích ngắn gọn cách xác định).
Câu 3 (1 điểm): Nguyên tử iron (kí hiệu là Fe) ở 20oC có khối lượng riêng là 7,87 g/cm3. Với giả thiết, tinh thể nguyên tử Fe là những hình cầu chiếm 75% thể tích tinh thể, phần còn lại là những khe rỗng giữa các quả cầu, hãy tính bán kính nguyên tử gần đúng của Fe. Cho biết khối lượng nguyên tử của Fe là 55,847 amu.
Phòng Giáo dục và Đào tạo .....
Đề thi Giữa Học kì 1
Năm học 2023
Bài thi môn: Hóa Học lớp 10
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 4)
Câu 1. Trong nguyên tử, loại hạt có mặt ở lớp vỏ nguyên tử là
A. proton. B. nơtron và electron.
C. nơtron. D. electron.
Câu 2. Hạt mang điện tích trong nguyên tử là
A. electron và nơtron. B. electron và proton.
C. nơtron và proton. D. electron, notron, proton.
Câu 3. Số proton và số nơtron trong hạt nhân nguyên tử ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26506.png) là
là
A. 201; 80. B. 121; 80. C. 80; 201. D. 80; 121.
Câu 4. Cấu hình electron nào sau đây là của nguyên tố phi kim ?
A. 1s22s1. B. 1s22s22p6.
C. 1s2. D. 1s22s22p63s23p5.
Câu 5. Cho các nguyên tử: ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26507.png) Các nguyên tử nào là đồng vị của cùng một nguyên tố hóa học?
Các nguyên tử nào là đồng vị của cùng một nguyên tố hóa học?
A. X và Z. B. Y và Z. C. T và Z. D. Y, Z,T.
Câu 6. Trong các cấu hình electron nào dưới đây sai?
A. 1s22s22p63s23p63d54s2 B. 1s22s22p63s23p6
C. 1s22s22p63s23p63d104s1. D. 1s22s22p63s23p64s24p4.
Câu 7. Số electron tối đa trong lớp M là
A. 32. B. 2. C. 18. D. 8.
Câu 8. Cho kí hiệu nguyên tử ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26508.png) . Phát biểu đúng là
. Phát biểu đúng là
A. Trong hạt nhân có 38 hạt mang điện.
B. Số hiệu nguyên tử là 39.
C. Số nơtron trong hạt nhân hơn số proton là 2.
D. Có lớp electron ngoài cùng là N.
Câu 9. Số p, n, e của ion ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26509.png) lần lượt là
lần lượt là
A. 26, 26, 23. B. 26, 30, 23. C. 26, 30, 26. D. 30, 26, 23.
Câu 10. Số p, n, e của ion ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26510.png) lần lượt là
lần lượt là
A. 17, 18, 20. B. 17, 17, 18. C. 17, 20, 18. D. 17, 20, 17.
Câu 11. Phát biểu nào dưới đây là đúng?
A. Electron ở phân lớp 4p có mức năng lượng thấp hơn phân lớp 4s.
B. Những electron ở lớp K có mức năng lượng thấp nhất.
C. Các electron trong cùng một lớp có năng lượng bằng nhau.
D. Những electron ở gần hạt nhân có mức năng lượng cao nhất.
Câu 12. Cho các nguyên tử có kí hiệu sau: ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26511.png) . Nhận định nào sau đây đúng khi nói về 3 nguyên tử trên?
. Nhận định nào sau đây đúng khi nói về 3 nguyên tử trên?
A. X, T là 2 đồng vị của cùng một nguyên tố hoá học.
B. X và T có cùng số khối.
C. X và Y có cùng số nơtron.
D. X, Y thuộc cùng một nguyên tố hoá học.
Câu 13. Ion X− có tổng số hạt proton, electron, nơtron là 53 trong X số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt. Cấu hình electron của nguyên tử X là
A. [Ne]3s23p5. B. [Ar]3d104s24p5.
C.[Ne]3s23p6. D. [Ar]3d54s2.
Câu 14. Nguyên tử khối trung bình của nguyên tố Br là 79,91; R có 2 đồng vị là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26515.jpeg) và
và ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26513.png) , Biết
, Biết ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26514.jpeg) chiếm 54,5%. Số khối (A1) của đồng vị thứ 2 có giá trị là
chiếm 54,5%. Số khối (A1) của đồng vị thứ 2 có giá trị là
A. 80. B. 82. C. 81. D. 85.
Câu 15. Nguyên tử khối trung bình của Cl là 35,5. Cl có 2 đồng vị là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26516.png) . Nếu có 50 nguyên tử
. Nếu có 50 nguyên tử ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26535.jpeg) thì có bao nhiêu nguyên tử
thì có bao nhiêu nguyên tử ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26534.jpeg) ?
?
A. 300 B. 150 C. 75 D. 100
Câu 16. Trong tự nhiên, nguyên tố đồng có hai đồng vị là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26519.png) . Nguyên tử khối trung bình của đồng là 63,54. Thành phần phần trăm tổng số nguyên tử của đồng vị
. Nguyên tử khối trung bình của đồng là 63,54. Thành phần phần trăm tổng số nguyên tử của đồng vị ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26522.png) là
là
A. 27%. B. 50%. C. 54%. D. 73%.
Câu 17. Trong tự nhiên clo có hai đồng vị bền: ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26523.png) chiếm 24,23% tổng số nguyên tử, còn lại là
chiếm 24,23% tổng số nguyên tử, còn lại là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26524.png) . Coi nguyên tử khối trung bình của oxy là 16, natri là 23. Thành phần % theo khối lượng của
. Coi nguyên tử khối trung bình của oxy là 16, natri là 23. Thành phần % theo khối lượng của ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26525.jpeg) trong NaClOn là 8,42 %. (Cho Na = 23, O = 16). Giá trị của n là
trong NaClOn là 8,42 %. (Cho Na = 23, O = 16). Giá trị của n là
A. 4. B. 3. C. 1. D. 2.
Câu 18. Cho m gam kim loại Na tác dụng với dung dịch HCl dư. Sau phản ứng thu được 6,72 lít H2 (đktc). Giá trị m là
A. 4,5. B. 13,5. C. 2,7. D. 13,8.
Câu 19. Các đồng vị được phân biệt bởi yếu tố nào sau đây?
A. Số electron hoá trị. B. Số nơtron.
C. Số proton. D. Số lớp electron.
Câu 20: Nguyên tố X có số hiệu nguyên tử là 29. Cấu hình e của X là
A. 1s22s22p63s23p64s23d9. B. 1s22s22p63s23p63d104s1.
C. 1s22s22p63s23p63d94s2. D. 1s22s22p63s23p64s13d10.
Câu 21. Một nguyên tử của nguyên tố X có tổng số hạt cơ bản (p, n, e) là 34. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10. Phát biểu nào dưới đây sai về X?
A.X là nguyên tố s. B. X là nguyên tố phi kim.
C. X có 3 lớp electron. D. số khối của X bằng 23.
Câu 22. Nguyên tử X có Z = 17, Số electron ở trên lớp ngoài cùng là
A. 4. B. 3. C. 7. D. 5.
Câu 23. Các electron của nguyên tử nguyên tố X được phân bố trên ba lớp. Phân lớp ngoài cùng có 4e. Điện tích của hạt nhân nguyên tử nguyên tố là
A. 16+. B. 14+ C. 17+. D. 15+.
Câu 24. Nguyên tử M có electron ở phân mức năng lượng cao nhất là 3d4 . Cấu hình electron nguyên tử M là
A. [Ar]3d4. B. [Ar]3d44s2. C. [Ar]3d54s2. D. [Ar]3d54s1.
Câu 25. Các nguyên tố kim loại kiềm thổ là nhóm IIA trong bảng tuần hoàn, vậy nó thuộc họ
A. d. B. s. C. f. D. p.
Câu 26. Nguyên tố nào sau đây là phi kim?
A. 1s22s22p4. B. 1s22s22p63s2.
C.1s22s22p63s23p63d64s2. D. 1s22s22p6.
Câu 27. Cấu hình electron của nguyên tố X là 1s22s22p63s23p64s2. Phát biểu sai là
A. Lớp N có 2e. B. Lớp K có 2e.
C. Lớp L có 8e. D. Lớp M có 6e.
Câu 28. Cấu hình electron của nguyên tố X là [Ne] 3s2. Vậy X là
A. Á kim. B. Khí hiếm. C. Kim loại. D. Phi kim.
Câu 29. Nguyên tử X có Z = 9. Vị trí của X trong bảng tuần hoàn là
A. Chu kì 2, nhóm VIA. B. Chu kì 3, nhóm IVA.
C. Chu kì 2, nhóm VIIA. D. Chu kì 3, nhóm IIA.
Câu 30. Một nguyên tử kim loại M khi nhường 2e ở lớp ngoài nó trở thành cation mang điện M2+. Biết M2+ có phân mức năng lượng cao nhất là 3p6. Vậy M có cấu hình e là
A. [Ne]3s23p5. B. [Ar]3d104s2. C. [Ne]3s23p6. D. [Ar]4s2.
Đáp án và hướng dẫn giải
1 - D |
2 - B |
3 - D |
4 - D |
5 - A |
6 - D |
7 - C |
8 - D |
9 - B |
10 - C |
11 - B |
12 - B |
13 - A |
14 - C |
15 - B |
16 - A |
17 - B |
18 - D |
19 - C |
20 - B |
21 - B |
22 - C |
23 - A |
24 - D |
25 - B |
26 - A |
27 - C |
28 - C |
29 – C |
30 - A |
Câu 3. D
Số proton = z = 80
Số nơtron = A – z = 201 – 80 = 121.
Câu 4. D
Nguyên tử có 5, 6, 7 electron lớp ngoài cùng thường là nguyên tử của nguyên tố phi kim.
1s22s22p63s23p5: có 7 electron ở lớp ngoài cùng là cấu hình electron nguyên tử nguyên tố phi kim.
Câu 5. A
X và Z có cùng số proton trong hạt nhân nên là đồng vị của cùng một nguyên tố hóa học.
Câu 6. D
D sai vì trât tự phân mức năng lượng là 1s 2s 2p 3s 3p 4s 3d …
Câu 7. C
Lớp M là lớp thứ 3, số electron tối đa trên lớp thứ 3 là 2.32 = 18.
Câu 8. D
A sai vì hạt mang điện trong hạt nhân là proton, số hạt proton = z = 19.
B sai vì số hiệu nguyên tử là 19.
C sai vì số nơtron 39 – 19 = 20 ; hơn số proton là 1.
D đúng vì cấu hình electron của K là [Ar]4s1 → lớp ngoài cùng là lớp thứ 4 hay lớp N.
Câu 9. B
Số proton = z = 26 = số electron trong nguyên tử.
Có M → M3+ + 3e
Vậy số electron của ion là 26 – 3 = 23.
Số nơtron = A – z = 56 – 26 = 30.
Câu 10. C
Số proton = z = 17 = số electron trong nguyên tử.
Có Cl + 1e → Cl-
Vậy số electron của ion là 17 + 1 = 18.
Số nơtron = A – z = 37 – 17 = 20.
Câu 11. B
A sai electron ở phân lớp 4p có mức năng lượng cao hơn phân lớp 4s.
B đúng.
C sai các electron trong cùng một lớp có năng lượng gần bằng nhau.
D sai vì những electron ở gần hạt nhân có mức năng lượng thấp nhất.
Câu 12. B
X và T có cùng số khối là 26.
Câu 13. A
X + 1e → X-
Tổng số hạt proton, electron, nơtron trong X là 53 – 1 = 52.
Gọi các hạt proton, electron, nơtron trong X lần lượt là p; e và n.
Theo bài ra, ta có hệ phương trình:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26527.jpeg)
Vậy cấu hình electron của X là [Ne]3s23p5.
Câu 14. C
Ta có:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26528.png) .
.
Bài 15. B
Gọi % số nguyên tử của hai đồng vị ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26529.jpeg) lần lượt là x và y. Theo bài ra ta có:
lần lượt là x và y. Theo bài ra ta có:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26531.jpeg)
Nếu có 50 nguyên tử ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26533.jpeg) thì có tất cả số nguyên tử Cl là:
thì có tất cả số nguyên tử Cl là:
Vậy số nguyên tử ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26536.jpeg) là 200 – 50 = 150.
là 200 – 50 = 150.
Câu 16. A
Gọi % số nguyên tử của hai đồng vị ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26538.jpeg) lần lượt là x và y. Ta có:
lần lượt là x và y. Ta có:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26540.jpeg)
Câu 17. B
Nguyên tử khối trung bình của Cl là:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26542.jpeg)
Giả sử có 1 mol Cl, vậy số mol ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26544.jpeg) là 0,2423.
là 0,2423.
Thành phần % theo khối lượng của ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26545.jpeg) trong NaClOn là 8,42 % nên:
trong NaClOn là 8,42 % nên:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26547.jpeg)
Câu 18. D
2Na + 2HCl → 2NaCl + H2
0,6 0,3 mol
→ m = 0,6.23 = 13,8 gam.
Câu 21. B
Theo bài ra ta có hệ phương trình:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26550.jpeg)
Cấu hình electron nguyên tử X là: [Ne]3s1
Vậy X có 3 lớp electron, là nguyên tố s, là nguyên tử của nguyên tố kim loại.
Số khối của X là 11 + 12 = 23.
Câu 22. C
Cấu hình electron của Z là [Ne]3s23p5. Vậy X có 7 electron ở lớp ngoài cùng.
Câu 23. A
Cấu hình electron nguyên tử X là 1s22s22p63s23p4.
Nguyên tử X có số p = số e = 16.
Điện tích hạt nhân nguyên tử là 16+.
Câu 25. B
Cấu hình electron tổng quát của các nguyên tố nhóm IIA là ns2 → thuộc họ s.
Câu 26. A
Các nguyên tử có 5, 6, 7 electron lớp ngoài cùng thường là nguyên tử của nguyên tố phi kim.
1s22s22p4 → 6 electron lớp ngoài cùng, là cấu hình electron nguyên tử nguyên tố phi kim.
Câu 27. D
Lớp K, lớp thứ 1 có 2e
Lớp L, lớp thứ 2 có 8e
Lớp M, lớp thứ 3 có 8e
Lớp N, lớp thứ 4 có 2e.
Câu 28. C
X có 2e lớp ngoài cùng nên là nguyên tử của nguyên tố kim loại.
Câu 29. C
Cấu hình electron của X là 1s22s22p5
→ X thuộc chu kỳ 2 (do có 2 lớp e); nhóm VIIA (do 7e hóa trị, nguyên tố p).
Câu 30. D
Cấu hình electron của M2+ là 1s22s22p63s23p6
Có M → M2+ + 2e
Vậy cấu hình electron của M là 1s22s22p63s23p64s2 hay [Ar]4s2.

Phòng Giáo dục và Đào tạo .....
Đề thi Giữa Học kì 1
Năm học 2023
Bài thi môn: Hóa Học lớp 10
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 5)
(Cho C=12, O=16, H=1, Na=23,K=39,Mg =24, Ca=40, P=31, Cl =35,5, F=9, Si =27, N=14, S=32)
I- TRẮC NGHIỆM (7 Điểm)
Câu 1: Tính số p và n trong hạt nhân nguyên tử
A. 92p, 235n. B. 92p,143n. C. 92p, 143p. D. 92n, 235p.
Câu 2: Trong tự nhiên Gali có 2 đồng vị là 69Ga (60,1%) và 71Ga (39,9%). Nguyên tử khối trung bình của Gali là:
A. 70 B. 71,20 C. 69,80 D. 70,20
Câu 3: Nguyên tố hoá học là
A. tập hợp các nguyên tử có khối lượng giống nhau
B. tập hợp các nguyên tử có số nơtron giống nhau.
C. tập hợp các nguyên tử có cùng số khối.
D. tập hợp các nguyên tử có cùng điện tích hạt nhân.
Câu 4: Nguyên tố R có công thức hợp chất khí với hiđro cao nhất là RH2. Vậy công thức oxit cao nhất là
A. RO B. RO2 C. RO3 D. R2O3
Câu 5: Trong các hạt sau, hạt nào không mang điện tích?
A. nơtron B. electron C. Nơtron và electron D. proton
Câu 6: Các hạt cấu tạo nên hầu hết các nguyên tử là
A. electron, nơtron, proton. B. nơtron, electron.
C. electron, proton. D. proton, nơtron.
Câu 7: Chu kì là tập hợp các nguyên tố, mà nguyên tử của các nguyên tố này có cùng
A. số electron. B. số electron ở lớp ngoài cùng
C. số lớp electron. D. số electron hóa trị.
Câu 8: Biết rằng nguyên tố cacbon thuộc chu kỳ 2, nhóm VIA. Cấu hình electron của cacbon là :
A. 1s22s22p2. B. 1s22s22p3. C. 1s22s22p63s23p64s2 D. 1s22s22p4
Câu 9: Khối lượng nguyên tử hầu như tập trung ở
A. hạt nhân. B. hạt proton. C. hạt nơtron. D. vỏ nguyên tử.
Câu 10: Cấu hình electron của nguyên tử X: 1s22s22p63s23p5. Hợp chất khí với hiđro và oxi cao nhất có dạng
A. HX, X2O7. B. H2X, XO3. C. XH4, XO2. D. H3X, X2O5.
Câu 11: Cấu hình electron đầy đủ cho các nguyên tử có cấu hình electron lớp ngoài cùng 3s23p4 là:
A. 1s22s22p53s23p4 B. 1s22s22p63s23p6 C. 1s22s22p63s23p4 D. 1s22s23s23p4
Câu 12: Nguyên tử của nguyên tố nào sau đây có cấu hình electron 1s22s22p63s23p64s2 ?
A. Mg B. Ca C. Na D. K
Câu 13: Một nguyên tử A có tổng số electron là 10, nguyên tố Y thuộc loại:
A. Nguyên tố s. B. Nguyên tố p. C. Nguyên tố D. D. Nguyên tố f.
Câu 14: Trong bảng tuần hoàn các nguyên tố, số chu kỳ nhỏ và chu kỳ lớn là:
A. 4 và 4. B. 3 và 3. C. 4 và 3. D. 3 và 4.
Câu 15: Vỏ nguyên tử gồm các electron chuyển động như thế nào xung quanh hạt nhân?
A. Chuyển động rất nhanh theo những quỹ đạo xác định.
B. Chuyển động rất nhanh không theo những quỹ đạo xác định.
C. Chuyển động rất chậm và không theo những quỹ đạo xác định.
D. Chuyển động rất không nhanh và không theo những quỹ đạo xác định.
Câu 16: Nguyên tử Na (Z=11) bị mất đi 1e thì cấu hình e tương ứng của nó là:
A. 1s22s22p6 B. 1s22s22p63s1 C. 1s22s22p63s3 D. 1s22s22p63s23p64s1
Câu 17: Các nguyên tố thuộc nhóm VIIA trong bảng tuần hoàn có tên gọi là
A. nhóm kim loại kiềm. B. nhóm halogen.
C. nhóm khí hiếm. D. nhóm kim loại kiềm thổ.
Câu 18: Cho các phát biểu sau
(a) Trong một chu kì, theo chiều tăng của điện tích hạt nhân thì tính kim loại giảm dần
(b) Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân thì tính phi kim tăng dần
(c) Các nguyên tố nhóm IA đều có tính kim loại mạnh
(d) Flo là phi kim mạnh nhất
(e) Chỉ có nguyên tử K mới chứa phân lớp electron 4s1.
Số phát biểu sai là:
A. 1. B. 2. C. 3. D. 4.
Câu 19: Trong một chu kì theo chiều tăng của điện tích hạt nhân nguyên tử
A. Bán kính nguyên tử tăng và độ âm điện giảm
B. Bán kính nguyên tử và độ âm điện tăng
C. Bán kính nguyên tử và độ âm điện giảm
D. Bán kính nguyên tử giảm và độ âm điện tăng
Câu 20: Nguyên tố canxi có số hiệu nguyên tử là 20, thuộc chu kỳ 4, nhóm IIA. Điều khẳng định nào sau đây về canxi là sai ?
A. Số electron ở vỏ nguyên tử của nguyên tố canxi là 20 .
B. Vỏ nguyên tử canxi có 4 lớp và lớp ngoài cùng có 2 electron.
C. Hạt nhân nguyên tử canxi có 20 proton.
D. Nguyên tố hóa học này là một phi kim.
Câu 21: Cho biết cấu hình electron của các nguyên tố X: 1s22s22p63s2; Y: 1s22s22p63s23p64s1; Z: 1s22s22p63s23p5. Nguyên tố nào là kim loại?
A. X. B. Z. C. X và Y. D. Y.
Câu 22: Tổng các hạt cơ bản trong một nguyên tử là 82 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Số khối của nguyên tử đó là
A. 57 B. 65 C. 56 D. 55
Câu 23: Một nguyên tố R có Z =13. Công thức oxit cao nhất có dạng.
A. R2O3 B. RO2 C. R2O5 D. RO3
Câu 24: Nguyên tố M có số hiệu nguyên tử là 17, vị trí của M trong bảng tuần hoàn là
A. chu kì 3, nhóm VIIIA. B. chu kì 3, nhóm VA.
C. chu kì 3, nhóm VIA. D. chu kì 3, nhóm VIIA.
Câu 25: Ý nào sau đây không biến đổi tuần hoàn?
A. Số lớp electron B. Số electron lớp ngoài cùng
C. Tính kim loại, tính phi kim D. Hóa trị cao nhất với oxi
Câu 26: Nguyên tử của nguyên tố Y có số electron là 13. Điện tích hạt nhân của nguyên tử Y là:
A. 13 B. 13- C. 13+ D. +13
Câu 27: Số electron tối đa chứa trong các phân lớp s, p, d, f lần lượt là:
A. 2, 8, 18, 32. B. 2, 4, 6, 8. C. 2, 6, 8, 18. D. 2, 6, 10, 14.
Câu 28: Nguyên tắc sắp xếp các nguyên tố vào bảng tuần hoàn:
(a) Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử;
(b) Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp vào cùng một hàng;
(c) Các nguyên tố có cùng số electron hóa trị được xếp vào một cột;
(d) Các nguyên tố có cùng số phân lớp electron trong nguyên tử được xếp vào cùng một hàng;
Số nguyên tắc đúng là
A. 2. B. 3. C. 1. D. 4.
--------------------
II- TỰ LUẬN (3 Điểm)
Câu 1 : (2 điểm) Xác định vị trí (STT, Chu kì, Nhóm) ; Tính chất hóa học ( Kim loại, Phi kim, Khí hiếm) của các nguyên tố sau ? (có giải thích cách xác định)
a) O (Z = 8)
b) Mg (Z = 12)
Câu 2: (1 điểm) Nguyên tố R có dạng R2O5. Trong hợp chất khí của R với hiđro chứa 91,18% R về khối lượng. Xác định tên nguyên tố R?
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
I – TRẮC NGHIỆM
1 – B |
2 - C |
3 -D |
4 - C |
5 - A |
6 - A |
7 - C |
8 - D |
9 - A |
10 – A |
11 - C |
12 - B |
13 - B |
14 - D |
15 - B |
16 - A |
17 - B |
18 - B |
19 - D |
20 - D |
21 - C |
22 - C |
23 - A |
24 - D |
25 - A |
26 - C |
27 - D |
28 - B |
Câu 1:
Số proton = Z = 92;
Số nơtron = A – Z = 235 – 92 = 143.
Câu 2:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26478.png)
Câu 4:
Nguyên tố R có công thức hợp chất khí với hiđro cao nhất là RH2 → R thuộc nhóm VIA, công thức oxit cao nhất là RO3.
Câu 10:
X thuộc nhóm VIIA (do có 7 electron lớp ngoài cùng, nguyên tố p); vậy công thức oxit cao nhất là X2O7; công thức hợp chất khí với hiđro là HX.
Câu 13:
Cấu hình electron nguyên tử Y: 1s22s22p6. Vậy Y thuộc nguyên tố p.
Câu 16:
Na: 1s22s22p63s1
Vậy khi mất đi một electron thì cấu hình electron tương ứng là: 1s22s22p6.
Câu 18:
Phát biểu sai là: b và e.
Câu 20:
D sai vì Ca là kim loại.
Câu 21:
X có 2 electron lớp ngoài cùng; Y có 1 electron lớp ngoài cùng nên X và Y là kim loại.
Câu 22:
Theo bài ra có hệ phương trình:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26480.png)
Số khối A = Z + N = 26 + 30 = 56.
Câu 23:
Cấu hình electron của R: [Ne]3s23p1
R thuộc nhóm IIIA, công thức oxit cao nhất có dạng R2O3.
Câu 24:
Cấu hình electron nguyên tử M: [Ne]3s23p5
Vậy M ở chu kỳ 3 (do có 3 lớp electron); nhóm VIIA (do có 7 electron hóa trị, nguyên tố p).
Câu 28:
Các nguyên tắc a, b, c đúng.
II – TỰ LUẬN
Câu 1:
a) O (Z = 8)
Cấu hình electron : 1s22s22p4
Oxi ở ô thứ 8 (Z = 8) ; chu kỳ 2 (do có 2 lớp electron) ; nhóm VIA (6 e hóa trị, nguyên tố p) ;
Oxi là phi kim do có 6 electron lớp ngoài cùng.
b) Mg (Z = 12)
Cấu hình electron : [Ne]3s2
Mg ở ô thứ 12 (Z = 12) ; chu kỳ 3 (do có 3 lớp electron) ; nhóm IIA (do có 2 e hóa trị, nguyên tố s)
Mg là kim loại do có 2 electron ở lớp ngoài cùng.
Câu 2 :
Công thức hợp chất khí với hiđro là RH3
%mR = 91,18%, ta có :
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26484.png)
Vậy R là photpho (P).

Phòng Giáo dục và Đào tạo .....
Đề thi Giữa Học kì 1
Năm học 2023
Bài thi môn: Hóa Học lớp 10
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 6)
(Cho C=12, O=16, H=1, Na=23,K=39,Mg =24, Ca=40, P=31, Cl =35,5, F=9, Si =27, N=14, S=32)
A. PHẦN TRẮC NGHIỆM: (28 câu – 7 điểm)
Câu 1. Cấu hình electron của nguyên tử X: 1s22s22p63s23p5. Hợp chất khí với hiđro và oxi cao nhất của X có dạng
A. XH4, XO2. B. H3X, X2O5. C. H2X, XO3. D. HX, X2O7.
Câu 2. X và Y là hai nguyên tố thuộc cùng một chu kỳ, hai nhóm A liên tiếp. Số proton của nguyên tử Y nhiều hơn số proton của nguyên tử X. Tổng số hạt proton trong nguyên tử X và Y là 33. Phát biểu nào sau đây về X, Y là đúng?
A. Độ âm điện của X lớn hơn độ âm điện của Y.
B. Phân lớp ngoài cùng của nguyên tử X (ở trạng thái cơ bản) có 4 electron.
C. Lớp ngoài cùng của nguyên tử Y (ở trạng thái cơ bản) có 5 electron.
D. Đơn chất X là chất khí ở điều kiện thường.
Câu 3. Vỏ nguyên tử gồm các electron chuyển động như thế nào xung quanh hạt nhân?
A. Chuyển động rất không nhanh và không theo những quỹ đạo xác định.
B. Chuyển động rất chậm và không theo những quỹ đạo xác định.
C. Chuyển động rất nhanh không theo những quỹ đạo xác định.
D. Chuyển động rất nhanh theo những quỹ đạo xác định.
Câu 4. Cho các phát biểu sau:
(a) Các electron ở lớp L có mức năng lượng gần bằng nhau
(b) Các electron ở lớp M (n=3) liên kết chặt chẽ với hạt nhân hơn các electron ở lớp K (n=1)
(c) Các electron ở lớp L có mức năng lượng cao hơn các electron ở lớp K
(d) Các electron ở lớp K có mức năng lượng bằng nhau
(e) Các electron ở phân lớp 3s có mức năng lượng thấp hơn các electron ở phân lớp 2p
Số phát biểu đúng là
A. 5 . B. 3. C. 2. D. 4.
Câu 5. Các hạt cấu tạo nên hầu hết các nguyên tử là:
A. electron, proton. B. electron, nơtron, proton
C. nơtron, electron. D. proton, nơtron.
Câu 6. Cho 4,6 gam kim loại X (thuộc nhóm IA) tác dụng hết với 95,6 ml nước (d = 1g/ml), thu được 2,24 lit khí H2 (đktc). Kim loại X là :
A. K B. Li C. Na D. Rb
Câu 7. Nguyên tố X có phân lớp electron ngoài cùng là 3p4. Nhận định nào sai khi nói về X?
A. X là nguyên tố thuộc nhóm IVA
B. X là nguyên tố thuộc chu kì 3 .
C. Lớp ngoài cùng của nguyên tử nguyên tố X có 6 electron
D. Hạt nhân nguyên tử của X có 16 proton .
Câu 8. Cho ba nguyên tử có kí hiệu là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26487.png) . Phát biểu nào sau đây là sai?
. Phát biểu nào sau đây là sai?
A. Hạt nhân của mỗi nguyên tử đều có 12 proton.
B. Ba nguyên tử trên đều thuộc nguyên tố Mg.
C. Đây là 3 đồng vị.
D. Số hạt electron của các nguyên tử lần lượt là: 12, 13, 14.
Câu 9. Các electron của nguyên tử nguyên tố X được phân bố trên 3 lớp, lớp thứ ba có 6 electron. Số đơn vị điện tích hạt nhân của nguyên tử nguyên tố X là
A. 8. B. 16. C. 14. D. 6.
Câu 10. Nguyên tử của nguyên tố X có tổng số hạt mang điện trong hạt nhân là 13. Vị trí của X trong bảng tuần hoàn là
A. Chu kì 3, nhóm IIIA. B. Chu kì 2, nhóm IIIA.
C. Chu kì 3, nhóm VIIA. D. Chu kì 3, nhóm IIA.
Câu 11. Cấu hình electron của nguyên tử có số hiệu Z = 17 là
A. 1s22s22p63s23p44s1. B. 1s22s22p63s23p5.
C. 1s22s22p63s23d5. D. 1s22s22p63s23p34s2.
Câu 12. Oxit X có công thức R2O. Tổng số hạt cơ bản (p, n, e) trong X là 92, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28. X là chất nào dưới đây (biết rằng trong hạt nhân nguyên tử oxi có 8 proton và 8 nơtron) ?
A. N2O. B. Cl2O. C. K2O. D. Na2O.
Câu 13. Nguyên tố A có Z = 18, vị trí của A trong bảng tuần hoàn là
A. chu kì 3, phân nhóm VIIIB. B. chu kì 3, phân nhóm VIA.
C. chu kì 3, phân nhóm VIIIA. D. chu kì 3, phân nhóm VIB.
Câu 14. Nguyên tử của một nguyên tố R có lớp ngoài cùng là lớp M trên lớp M chứa 2 electron. Cấu hình electron của R và tính chất của R là
A. 1s22s22p63s23p2, phi kim. B. 1s22s22p63s2, phi kim.
C. 1s22s22p63s2, kim loại. D. 1s22s22p63s23p6, khí hiếm.
Câu 15. Ở trạng thái cơ bản, nguyên tử X có 3 lớp electron và có 3 electron ở phân lớp ngoài cùng. Vị trí của nguyên tố X trong bảng tuần hoàn là
A. chu kì 3, nhóm IIIA. B. chu kì 3, nhóm VIIA.
C. chu kì 3, nhóm VIA. D. chu kì 3, nhóm VA.
Câu 16. Phát biểu nào sau đây sai?
A. Một nguyên tử có số hạt proton bằng số hạt nơtron thì số khối là số lẻ.
B. Trong nguyên tử, số đơn vị điện tích hạt nhân bằng số proton.
C. Dãy gồm các phân lớp e đã bão hòa: s2, p6, d10, f14.
D. Nguyên tố có cấu hình e ngoài cùng: 3s2 có số hạt mang điện tích dương là 12.
Câu 17. Nguyên tử của nguyên tố X có số proton là 13. Điện tích hạt nhân của nguyên tử X là
A. 13+. B. +13. C. 13. D. 13-.
Câu 18. Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì và có tổng số proton trong hai hạt nhân là 25. X và Y thuộc chu kì và nhóm nào trong bảng tuần hoàn ?
A. Chu kì 2, nhóm IIA B. Chu kì 3, các nhóm IIA và IIIA .
C. Chu kì 3, các nhóm IA và IIA . D. Chu kì 2, các nhóm IIIA và IVA .
Câu 19. Trong tự nhiên magie có 3 đồng vị bền 24Mg chiếm 78,99%, 25Mg chiếm 10,00% và 26Mg. Nguyên tử khối trung bình của Mg là
A. 24,89. B. 24,00. C. 24,32. D. 24,11.
Câu 20. Nguyên tử của nguyên tố X có tổng số electron ở phân lớp p là 5. Vị trí của nguyên tố X trong bảng tuần hoàn là
A. Nhóm VA,chu kì 3. B. VIIA, chu kì 2.
C. VIIB, chu kì 2. D. VIA, chu kì 3.
Câu 21. Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt. Nguyên tố X có số khối là
A. 28. B. 26. C. 27. D. 23.
Câu 22. Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là ns2np4.Trong hợp chất khí của nguyên tố X với hiđro, X chiếm 94,12% khối lượng. Phần trăm khối lượng của nguyên tố X trong oxit cao nhất là
A. 27,27%. B. 50,00%. C. 40,00%. D. 60,00%.
Câu 23. Số proton và số nơtron trong hạt nhân nguyên tử là
A. 24p, 28n. B. 52p, 24n. C. 28p, 24n. D. 24p, 52n.
Câu 24. Cho các phát biểu sau:
(a) Bảng tuần hoàn có 7 chu kì,trong đó có 3 chu kì nhỏ và 4 chu kì lớn;
(b) Bảng tuần hoàn có 8 nhóm, số thứ tự của nhóm bằng số electron lớp ngoài cùng;
(c) Các nhóm A có số electron lớp ngoài cùng bằng số thứ tự của nhóm;
(d) Các nguyên tố s và p thuộc về các nhóm A;
(e) Các chu kì nhỏ (1,2,3) bao gồm các nguyên tố s,p;
Số phát biểu đúng là :
A. 5. B. 2. C. 3. D. 4.
Câu 25. Số nguyên tố trong chu kì 3 và chu kì 5 lần lượt là
A. 8 và 18. B. 8 và 8. C. 18 và 18. D. 18 và 8.
Câu 26. Lớp thứ 3 (n = 3) có số phân lớp là
A. 4. B. 5. C. 7. D. 3.
Câu 27. Cho các nguyên tố M (Z = 11), X (Z = 17), Y (Z = 9) và R (Z = 19). Độ âm điện của các nguyên tố tăng dần theo thứ tự
A. R < M < X < Y. B. Y < M < X < R. C. M < X < Y < R. D. R < M < Z< Y.
Câu 28. Cho kí hiệu nguyên tử , phát biểu nào sau đây là sai?
A. Tổng số hạt mang điện trong nguyên tử P là 30.
B. Điện tích hạt nhân của nguyên tử P là 15+.
C. Hạt nhân nguyên tử P có 15 proton và 16 nơtron.
D. Lớp vỏ của nguyên tử P có 16 electron.
B. PHẦN TỰ LUẬN: (3 điểm)
Câu 1: (1,5 điểm) Cho nguyên tố X ở chu kỳ 3, nhóm VIIA trong bảng tuần hoàn các nguyên tố hóa học. Hỏi:
a) Viết cấu hình e của nguyên tử X? Xác định tên nguyên tố X?
b) Viết công thức oxit cao nhất, công thức hiđroxit tương ứng. Chúng có tính axit hay bazơ?
c) Viết công thức hợp chất khí với hiđro?
Câu 2: (1,5 điểm)
Trong tự nhiên, Cu có hai đồng vị bền là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26489.png) , nguyên tử khối trung bình của Cu là 63,54. Tính phần trăm khối lượng
, nguyên tử khối trung bình của Cu là 63,54. Tính phần trăm khối lượng ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26490.png) trong CuS (biết nguyên tử khối của S là 32).
trong CuS (biết nguyên tử khối của S là 32).
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
PHẦN TRẮC NGHIỆM
1 - D |
2 - B |
3 - C |
4 - B |
5 - B |
6 - C |
7 - A |
8 - D |
9 - B |
10 - A |
11 - B |
12 - D |
13 - C |
14 - C |
15 - D |
16 - A |
17 - A |
18 - B |
19 - C |
20 - B |
21- C |
22 - C |
23 - A |
24 - D |
25 - A |
26 - D |
27 - A |
28 - D |
Câu 1:
X thuộc nhóm VIIA (do có 7 electron lớp ngoài cùng, nguyên tố p), nên công thức hợp chất khí với hidro có dạng HX, công thức oxit cao nhất: X2O7.
Câu 2:
Theo bài ra có hệ phương trình:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26491.png)
A sai do độ âm điện của Y lớn hơn độ âm điện của X.
B đúng vì cấu hình e của X là [Ne]3s23p4 hay phân lớp ngoài cùng có 4 electron.
C sai vì lớp ngoài cùng của Y có 7 electron.
D sai vì X là S, là chất rắn ở điều kiện thường.
Câu 4:
Các phát biểu đúng là: a, c và d.
Câu 6:
2X + 2H2O → 2X(OH)2 + H2
Có nX = 2.nkhí = 0,2 mol
MX = 4,6/0,2 = 23. Vậy X là Na.
Câu 7:
Cấu hình electron của X: [Ne]3s23p4
Vậy A sai vì X thuộc nhóm VIA.
Câu 8:
D sai vì các nguyên tử đều có 12 electron.
Câu 9:
Cấu hình electron nguyên tử X: [Ne]3s23p4
Vậy số đơn vị điện tích hạt nhân X là 16.
Câu 10:
Cấu hình electron nguyên tử X: [Ne]3s23p1
Vậy X ở chu kì 3, nhóm IIIA.
Câu 12:
Tổng số hạt cơ bản (p, n, e) trong X là 92
→ 2. (2pR + nR) + 2pO + nO = 92 → 2. (2pR + nR) = 68
Số hạt mang điện nhiều hơn số hạt không mang điện là 28
→ (2.2pR +2.nO )- (2nR + nO) = 28
→ 4pR - 2nR = 20
Giải hệ → pR= 11, nR = 12 → R là Na
Vậy công thức của X là Na2O.
Câu 13:
Cấu hình electron nguyên tử A: [Ne]3s23p6
Vậy A ở chu kì 3 (do có 3 lớp electron); nhóm VIIIA (do có 8e hóa trị, nguyên tố p).
Câu 14:
Lớp M – lớp thứ 3
Cấu hình electron của R: [Ne]3s2
Vậy R là kim loại do có 2 electron ở lớp ngoài cùng.
Câu 15:
Cấu hình electron của X là: [Ne]3s23p3
Vậy X ở chu kỳ 3, nhóm VA.
Câu 16:
A sai, vì tổng của 2 số lẻ là một số chẵn.
Câu 18:
Giả sử X đứng trước Y ta có hệ phương trình:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26494.png)
Cấu hình electron của X và Y lần lượt là: [Ne]3s2 và [Ne]3s23p1
Vậy X và Y đều thuộc chu kì 3, X thuộc nhóm IIA và Y thuộc nhóm IIIA.
Câu 19:
Nguyên tử khối trung bình của Mg là
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26495.png)
Câu 20:
Cấu hình electron của X: 1s22s22p5
Vậy X ở chu kỳ 2 (do có 2 lớp electron); nhóm VIIA (do có 7 e hóa trị, nguyên tố p).
Câu 21:
Theo bài ra ta có hệ phương trình:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26497.png)
Số khối A = 13 + 14 = 27.
Câu 22:
Theo bài ra, X thuộc nhóm VIA, công thức hợp chất khí với hidro: H2S
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26498.png)
Vậy X là lưu huỳnh, công thức oxit cao nhất là SO3.
%mS trong oxit cao nhất là ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26499.png)
Câu 23:
Số proton = Z = 24;
Số nơtron = A – Z = 52 – 24 = 28.
Câu 24:
Các phát biểu đúng: a, c, d, e.
Câu 26:
Lớp thứ n có n phân lớp. Vậy lớp thứ 3 có 3 phân lớp.
Câu 27:
Y là Flo, có độ đâm điện lớn nhất → loại B và C.
Loại D do không có nguyên tố Z.
Câu 28:
D sai vì P có 15 electron.
Phần tự luận
Câu 1:
a) X ở chu kì 3 nên có 3 lớp electron, X thuộc nhóm VIIA nên có 7 electron lớp ngoài cùng.
Cấu hình electron của X là: [Ne]3s23p5. Vậy X là Clo.
b) Công thức oxit cao nhất là Cl2O7, là oxit axit.
Công thức hiđroxit tương ứng là HClO4 là axit.
c) Công thức hợp chất khí với hidro là HCl.
Câu 2:
Gọi % số nguyên tử của ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26500.png) lần lượt là x và y. Theo bài ra ta có:
lần lượt là x và y. Theo bài ra ta có:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26501.png)
Giả sử có 1 mol CuS → Số mol Cu = 1 mol, số mol ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26503.png) = 0,73 mol.
= 0,73 mol.
Phần trăm khối lượng ![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26504.jpeg) trong CuS là:
trong CuS là:
![[Năm 2023] Đề thi Giữa kì 1 Hóa Học lớp 10 có đáp án (10 đề)](../de-thi-lop-10/images/de-thi-giua-ki-1-hoa-hoc-lop-10-co-dap-an-2021-26505.png)
..........................
..........................
..........................
Tải xuống để xem tài liệu đề thi Hóa học lớp 10 Giữa học kì 1 năm 2023 đầy đủ!