Giáo án Hóa học 12 Bài: Luyện tập: Sự ăn mòn kim loại mới nhất
Giáo án Hóa học 12 Bài: Luyện tập: Sự ăn mòn kim loại mới nhất
Haylamdo biên soạn và sưu tầm Với mục đích giúp các Thầy / Cô giảng dạy môn Hóa học dễ dàng biên soạn Giáo án Hóa học lớp 12, VietJack biên soạn Giáo án Hóa học 12 Bài: Luyện tập: Sự ăn mòn kim loại phương pháp mới theo hướng phát triển năng lực theo 5 bước bám sát mẫu Giáo án môn Hóa học chuẩn của Bộ Giáo dục. Hi vọng tài liệu Giáo án Hóa học 12 này sẽ được Thầy/Cô đón nhận và đóng góp những ý kiến quí báu.
A. CHUẨN KIẾN THỨC – KĨ NĂNG
I. KIẾN THỨC – KĨ NĂNG
1. Kiến thức: Củng cố kiến thức về bản chất của sự ăn mòn kim loại, các kiểu ăn mòn kim loại và chống ăn mòn.
2. Kĩ năng: Kĩ năng tính toán lượng kim loại điều chế theo các phương pháp hoặc các đại lượng có liên quan.
3. Thái độ: Nhận thức được tác hại nghiêm trọng của sự ăn mòn kim loại, nhất là nước ta ở vào vùng nhiệt đới gió mùa, nóng nhiều và độ ẩm cao. Từ đó, có ý thức và hành động cụ thể để bảo vệ kim loại, tuyên truyền và vận động mọi người cùng thực hiện nhiệm vụ này.
II. PHÁT TRIỂN NĂNG LỰC
* Các năng lực chung
1. Năng lực tự học
2. Năng lực hợp tác
3. Năng lực phát hiện và giải quyết vấn đề
4. Năng lực giao tiếp
* Các năng lực chuyên biệt
1. Năng lực sử dụng ngôn ngữ
2. Năng lực tư duy
3. Năng lực giải quyết vấn đề thông qua hóa học
4. Năng lực tính toán
* Phẩm chất: Trung thực, tự trọng, chí công, vô tư; Tự lập, tự tin, tự chủ; Có trách nhiệm với bản thân, cộng đồng, đất nước, nhân loại; Nghĩa vụ công dân.
B. CHUẨN BỊ
* Giáo viên: Lựa chọn bài tập
* Học sinh: Học bài cũ, làm bài tập.
C. PHƯƠNG PHÁP VÀ KĨ THUẬT DẠY HỌC:
Dạy học hợp tác theo nhóm, đàm thoại
Kĩ thuật khăn trải bàn
D. TIẾN TRÌNH BÀI DẠY
1. Hoạt động khởi động
1.1. Ổn định lớp: Kiểm tra sĩ số, đồng phục...
1.2. Kiểm tra bài cũ: không
2. Hoạt động luyện tập
Hoạt động của giáo viên |
Hoạt động của Học sinh – Phát triển năng lực |
Nội dung |
|
GV chia lớp thành 3 nhóm GV phát phiếu học tập số 1, yêu cầu HS thảo luận Bài 1: Khi điều chế H2 từ Zn và dung dịch H2SO4 loãng, nếu thêm một vài giọt dung dịch CuSO4 vào dung dịch axit thì thấy khí H2 thoát ra nhanh hơn hẳn. Hãy giải thích hiện tượng trên. Bài 2: Ngâm 9g hợp kim Cu – Zn trong dung dịch HCl dư thu được 896 ml H2 (đkc). Xác định % khối lượng của hợp kim. Bài 3: Ngâm 1 cây đinh sắt sạch trong 200ml dd CuSO4. Sau khi kết thúc phản ứng, lấy đinh sắt ra khỏi dd thấy khối lượng đinh sắt tăng 0,8g. Xác định vai trò các chất tham gia phản ứng và nồng độ mol/lit của dd CuSO4. - Gv: Chấm phiếu học tập của một số hs - Gv gọi 3 hs bất kỳ của các nhóm lên bảng, hs khác nhận xét, bổ sung - Gv nhận xét, đánh giá Phiếu số 2. Hoạt động riêng rẽ từng HS |
Hs: thảo luận nhóm hoàn thành 1 trong 3 bài tập trong phiếu (Mỗi học sinh 1 phiếu) Hs: đại diện lên bảng trình bày, hs nhóm khác nhận xét, bổ sung Phát triển năng lực giao tiếp, năng lực tư duy, năng lực phát hiện và giải quyết vấn đề, năng lực tính toán và năng lục sử dụng ngôn ngữ hóa học |
Phiếu học tập số 1 Bài 1: Giải
Zn + H2SO4 → ZnSO4 + H2↑ Khí H2 sinh ra bám vào bề mặt lá Zn, ngăn cản sự tiếp xúc giữa Zn và H2SO4 nên phản ứng xảy ra chậm.
Zn + CuSO4 → ZnSO4 + Cu Cu tạo thành bám vào Fe tạo thành cặp điện cực và Fe bị ăn mòn điện hoá. - Ở cực âm (Fe): Kẽm bị oxi hoá. Zn – 2e → Zn2+ - Ở cực dương (Cu): Các ion H+ của dung dịch H2SO4 loãng bị khử thành khí H2. 2H+ + 2e → H2↑ H2 thoát ra ở cực đồng, nên Zn bị ăn mòn nhanh hơn, phản ứng xảy ra mạnh hơn. Bài 2: Giải Ngâm hợp kim Cu – Zn trong dung dịch HCl dư, chỉ có Zn phản ứng. Zn + 2HCl → ZnCl2 + H2↑ → nZn = nH2 = → %Zn = → %Cu = 71,11% Bài 3: Gọi số mol Fe phản ứng vói x mol. Fe + CuSO4 FeSO4 + Cu → mtăng = 64x - 56x = 8 ↔ x = 1 mol → nCuSO4 = x = 1 mol → CM(CuSO4) = Phiếu học tập số 2 (Nội dung đính kèm bên dưới) |
..........................................
Tài liệu còn nhiều, mời bạn tải xuống để xem đầy đủ!

 Ban đầu Zn tiếp xúc trực tiếp với dung dịch H2SO4 loãng và bị ăn mòn hoá học.
Ban đầu Zn tiếp xúc trực tiếp với dung dịch H2SO4 loãng và bị ăn mòn hoá học.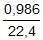 = 0,04
= 0,04 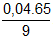 .100 = 28,89%
.100 = 28,89%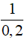 = 5M
= 5M