Giáo án KHTN 7 Bài 2: Nguyên tử - Kết nối tri thức
Giáo án KHTN 7 Bài 2: Nguyên tử - Kết nối tri thức
Chỉ 400k mua trọn bộ Giáo án KHTN 7 Kết nối tri thức bản word chuẩn kiến thức, trình bày đẹp mắt:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
Thời gian thực hiện: 4 tiết
I. MỤC TIÊU
1. Kiến thức
- Trình bày được mô hình nguyên tử của Rutherford – Bohr (mô hình sắp xếp electron trong các lớp electron ở vỏ nguyên tử).
- Nêu được khối lượng nguyên tử theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử).
2. Năng lực
a) Năng lực chung
- Tự chủ, tự học: Chủ động, tự tìm hiểu về nguyên tử, cấu tạo nguyên tử và giải thích tính trung hòa về điện của nguyên tử.
- Giao tiếp và hợp tác:
+ Sử dụng ngôn ngữ khoa học để diễn đạt về nguyên tử, các hạt tạo thành nguyên tử (proton, electron và neutron).
+ Hoạt động nhóm hiệu quả đúng theo yêu cầu của giáo viên trong khi thảo luận về nguyên tử, đảm bảo các thành viên đều được tham gia, trình bày và báo cáo.
- Giải quyết vấn đề và sáng tạo: Giải quyết vấn đề kịp thời với các thành viên khác trong nhóm để thảo luận hiệu quả, giải quyết các vấn đề trong bài học và hoàn thành các nhiệm vụ học tập.
b) Năng lực khoa học tự nhiên
- Nhận thức khoa học tự nhiên: Trình bày được mô hình nguyên tử Rutherford – Bohr (mô hình sắp xếp electron các lớp electron ở vỏ nguyên tử). Nêu được khối lượng nguyên tử theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử).
- Tìm hiểu tự nhiên: Quan sát về hình ảnh nguyên tử, mô hình nguyên tử để tìm hiểu cấu trúc đơn giản về nguyên tử trong bài.
- Vận dụng kiến thức, kĩ năng đã học: Giải thích được nguyên tử trung hòa về điện, sử dụng mô hình nguyên tử Rutherford – Bohr để xác định các loại hạt tạo thành của một số nguyên tử trong bài học. Tính được khối lượng nguyên tử theo đơn vị amu dựa vào số lượng hạt cơ bản trong nguyên tử.
3. Phẩm chất
- Tham gia tích cực hoạt động nhóm phù hợp với khả năng bản thân.
- Cẩn thận, trung thực và thực hiện các yêu cầu của chủ đề bài học.
- Có niềm say mê, hứng thú với việc khám phá và học tập khoa học tự nhiên.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên
- Mô hình nguyên tử.
- Các hình ảnh theo sách giáo khoa.
- Giấy màu và các viên bi nhựa.
2. Học sinh
- Ôn tập bài cũ và chuẩn bị bài mới.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
Hoạt động 1. Mở đầu
a) Mục tiêu: Tạo được húng thú cho học sinh, dẫn dắt giới thiệu vấn đề, để học sinh biết được chất được tạo nên từ đâu, từ đó hình thành mục tiêu bài học.
b) Nội dung: HS kể tên một số vật thể xung quanh ta. Chọn 1 vật thể và nêu chất tạo nên vật thể đó. Cho biết chất được tạo nên từ những hạt nào?
c) Sản phẩm: HS bước đầu nói lên suy nghĩ của bản thân và có hướng điều chỉnh đúng trong nghiên cứu vấn đề.
d) Tổ chức thực hiện
HOẠT ĐỘNG CỦA GIÁO VIÊN |
HOẠT ĐỘNG CỦA HỌC SINH |
|
* Chuyển giao nhiệm vụ học tập Yêu cầu HS làm việc cá nhân, trả lời một số câu hỏi: 1. Kể tên 1 số vật thể xung quanh ta. 2. Từ những vật thể đơn giản như bút chì, quyển vở, chai nước đến những công trình nổi tiếng như cầu Long Biên ….đều được cấu tạo nên từ chất. Mỗi chất đều được cấu tạo nên từ những hạt vô cùng bé. Những hạt đó là gì? * Thực hiện nhiệm vụ học tập - GV theo dõi, hỗ trợ học sinh khi cần. * Báo cáo kết quả và thảo luận - GV gọi ngẫu nhiên 2 HS trình bày đáp án, mỗi HS trả lời 1 câu hỏi. * Đánh giá kết quả thực hiện nhiệm vụ - GV nhận xét và nêu vấn đề cần tìm hiểu trong bài. |
- Nhận nhiệm vụ - Trả lời câu hỏi. - 2 HS trình bày; Các HS khác lắng nghe và bổ sung. - HS hình thành mục tiêu bài học. |
B. HÌNH THÀNH KIẾN THỨC
Hoạt động 2: Tìm hiểu quan niệm ban đầu về nguyên tử
a) Mục tiêu: HS nêu được khái niệm ban đầu về nguyên tử.
b) Nội dung:
- Học sinh làm việc nhóm đôi, thực hành và trả lời các câu hỏi từ đó hình thành nên kiến thức.
c) Sản phẩm
- Câu trả lời của học sinh.
d) Tổ chức thực hiện
HOẠT ĐỘNG CỦA GV VÀ HS |
NỘI DUNG |
|
* Chuyển giao nhiệm vụ học tập - GV yêu cầu HS hoạt động cặp đôi, theo bàn. + Trong 2 phút, cắt giấy thành những mẩu thật nhỏ. Nhóm nào cắt được mẩu nhỏ nhất sẽ giành chiến thắng. - Trả lời câu hỏi: + Mẩu giấy có cắt được nhỏ mãi không? + Theo Đê – mô crit và Đan – tơn, nguyên tử được quan niệm như thế nào? |
I. Quan niệm ban đầu về nguyên tử - Theo Democritus: “Nguyên tử là những hạt rất nhỏ bé, không thể phân chia đươc nữa”. - Theo Dalton: “Các đơn vị chất tối thiểu (nguyên tử) kết hợp với nhau vừa đủ theo các lượng xác định trong phản ứng hóa học”. |
|
* Thực hiện nhiệm vụ - Thực hành cắt giấy theo nhóm. - Thảo luận nhóm trả lời 2 câu hỏi. - Sau khi thảo luận xong, rút ra kết luận. | |
|
* Báo cáo, thảo luận - Mời đại diện các nhóm trình bày kết quả của mình. - Các nhóm lắng nghe, nhận xét, bổ sung. | |
|
* Đánh giá kết quả thực hiện nhiệm vụ - GV kết luận về nội dung kiến thức mà các nhóm đưa ra. |
Hoạt động 3:
Tìm hiểu mô hình nguyên tử của Rutherford – Bohr (Rơ-dơ-pho – Bo)
a) Mục tiêu: Trình bày được mô hình nguyên tử của Rutherford – Bohr (mô hình sắp xếp electron trong các lớp electron ở vỏ nguyên tử).
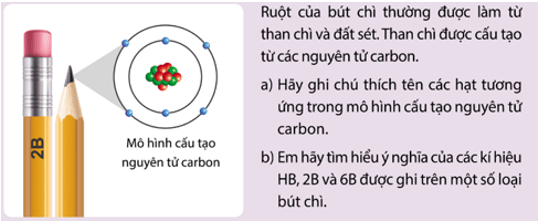
b) Nội dung: Tổ chức HS làm mô hình nguyên tử carbon theo Bohr và trả lời các câu hỏi SGK.
c) Sản phẩm
- Mô hình nguyên tử carbon.
d) Tổ chức thực hiện
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH |
NỘI DUNG |
|
* Chuyển giao nhiệm vụ học tập 1. - GV chiếu hình ảnh nguyên tử, dựa vào thông tin sách giáo khoa: + Theo Rơ-dơ-pho, nguyên tử có cấu tạo như thế nào? * Thực hiện nhiệm vụ 1 - HS đọc sách giáo khoa và trả lời câu hỏi của GV. * Báo cáo, thảo luận 1 - GV gọi ngẫu nhiên 1 HS trả lời. - Các HS khác lắng nghe, nhận xét, bổ sung. * Chốt kiến thức - GV chiếu slide mô hình nguyên tử theo theo Rơ-dơ-pho. |
II. Mô hình nguyên tử của Rơ- dơ-pho – Bo - Mô hình nguyên tử Rutherford: - Nguyên tử cấu tạo rỗng. - Cấu tạo nguyên tử: + Hạt nhân ở tâm mang điện tích dương. + Electron ở lớp vỏ mang điện tích âm. + Electron chuyển động xung quanh hạt nhân như các hành tinh quay quanh Mặt Trời. - Mô hình nguyên tử của Bohr: Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau. + Lớp trong cùng có 2 electron, bị hạt nhân hút mạnh nhất. + Các lớp khác chứa tối đa 8 electron hoặc nhiều hơn, bị hạt nhân hút yếu hơn |
|
* Chuyển giao nhiệm vụ học tập 2. - GV chiếu slide, yêu cầu HS đọc sách giáo khoa và trả lời + Theo Bohr các electron chuyển động xung quanh hạt nhân như thế nào? + Số electron ở mỗi lớp bao nhiêu? * Thực hiện nhiệm vụ 2 - Đọc thông tin SGK và trả lời câu hỏi. * Báo cáo, thảo luận 2 - GV gọi ngẫu nhiên 1 HS trả lời. - Các HS khác lắng nghe, nhận xét, bổ sung. * Chốt kiến thức - GV chiếu slide mô hình nguyên tử theo theo Bohr. * GV yêu cầu HS mô tả cấu tạo nguyên tử hydrogen và nguyên tử carbon. | |
|
* Chuyển giao nhiệm vụ 3: Làm mô hình nguyên tử carbon theo Bohr - GV chia lớp thành 4 nhóm. Chiếu slide phần chuẩn bị, cách tiến hành và trả lời câu hỏi sách giáo khoa. - Chuẩn bị: Bìa carton, giấy màu vàng, các viên bi nhựa to màu đỏ và các viên bi nhỏ màu xanh. - Tiến hành: + Gắn bi đỏ vào bìa carton làm hạt nhân nguyên tử carbon. + Cắt giấy màu vàng thành 2 đường tròn có bán kính khác nhau và mỗi đường tròn có độ dài khoảng 1 cm. + Dán các đường tròn lên bìa carton sao cho tâm của hai đường tròn là viên bi màu đỏ. + Gắn các viên bi màu xanh lên hai đường tròn màu vàng. - Thảo luận nhóm và trả lời câu hỏi ?1. Các đường tròn bằng giấy màu vàng biểu diễn gì? ?2. Em hãy cho biết số electron có trong lớp electron thứ nhất và thứ hai của nguyên tử carbon và chỉ ra lớp electron đã chứa tối đa electron. + Quan sát Hình 2.1 và cho biết các thành phần cấu tạo nên nguyên tử. + Quan sát Hình 2.2, áp dụng mô hình nguyên tử của Bohr, mô tả cấu tạo nguyên tử hydrogen và nguyên tử carbon. * Thực hiện nhiệm vụ 3 - HS làm mô hình nguyên tử carbon theo nhóm. - GV quan sát, hỗ trợ HS. * Báo cáo, thảo luận 3 - Các nhóm treo mô hình nguyên tử carbon lên bảng. - Đại diện 1 nhóm trình bày và trả lời câu hỏi. - Các nhóm khác lắng nghe, nhận xét, bổ sung. * Đánh giá kết quả thực hiện nhiệm vụ 3 - GV nhận xét và chiếu một số mô hình nguyên tử Carbon. |
Hoạt động 4. Tìm hiểu cấu tạo nguyên tử
a) Mục tiêu: Hiểu và vận dụng kiến thức về mô hình nguyên tử theo Rutherford – Bohr.
b) Nội dung: Từ nội dungkiến thức mô hình nguyên tử theo Rutherford – Bohr, học sinh làm việc cặp đôi đọc thông tin sách giáo khoa tìm hiểu cấu tạo hạt nhân nguyên tử và vỏ nguyên tử, quan sát các hình 2.4, 2.6, trả lời các câu hỏi trang 16,18.
- HS làm việc theo nhóm thực hiện hoạt động trang 17 hoàn thành bảng 2.1 và trả lời câu hỏi.
PHIẾU HỌC TẬP 1
Quan sát hình 2.4 – SGK trang 16 và cho biết:
1. Hạt nhân nguyên tử được cấu tạo gồm một hay nhiều hạt? Các hạt đó thuộc cùng một loại hay nhiều loại hạt?
2. Số đơn vị điện tích hạt nhân của Helium bằng bao nhiêu?
PHIẾU HỌC TẬP SỐ 2
Quan sát hình 2.6 – SGK trang 18 và cho biết:
1. Thứ tự sắp xếp các electron ở vỏ của nguyên tử chlorine.
2. Số electron trên từng lớp ở vỏ nguyên tử clorine
PHIẾU HỌC TẬP SỐ 3
Quan sát hình 2.5 – SGK – trang 17 và hoàn thành bảng sau:
Nguyên tử |
Số proton trong hạt nhân |
Số electron trong vỏ nguyên tử |
Số lớp electron |
Số electron ở lớp electron ngoài cùng |
Carbon |
? |
? |
? |
? |
Oxygen |
? |
? |
? |
? |
Nitrogen |
? |
? |
? |
? |
c. Sản phẩm:
Bài làm của học sinh trong các phiếu học tập:
PHIẾU HỌC TẬP 1
1. Hạt nhân nguyên tử có nhiều hạt. Các hạt này thuộc hai loại hạt là proton và neutron.
2. Số đơn vị điện tích hạt nhân của helium bằng 2 (bằng tổng số hạt proton có trong hạt nhân).
PHIẾU HỌC TẬP SỐ 2
1. - Các electron sắp xếp thành từng lớp:
+ Lớp electron thứ nhất (ở trong cùng), gần hạt nhân nhất;
+ Lớp electron thứ hai ở bên ngoài lớp thứ nhất;
+ Lớp electron thứ ba ở ngoài cùng.
- Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
2. Lớp thứ nhất có 2 electron, lớp thứ 2 có 8 electron, lớp thứ 3 có 7 electron.
PHIẾU HỌC TẬP SỐ 3
Nguyên tử |
Số proton trong hạt nhân |
Số electron trong vỏ nguyên tử |
Số lớp electron |
Số electron ở lớp electron ngoài cùng |
Carbon |
6 |
6 |
2 |
4 |
Oxygen |
8 |
8 |
2 |
6 |
Nitrogen |
7 |
7 |
2 |
5 |
d) Tổ chức thực hiện
Hoạt động của giáo viên và học sinh |
Nội dung |
|
* Chuyển giao nhiệm vụ học tập GV giới thiệu kích thước nguyên tử và kích thước hạt nhân, vị trí vỏ nguyên tử. -Yêu cầu HS hoạt động cặp đôi bàn 1,3,5,... đọc SGK, hoàn thành phiếu học tập số 1, bàn 2,4,6,... đọc SGK, hoàn thành phiếu học tập 2.Thời gian cho mỗi cặp đôi là 5 phút (Chiếu 2 phiếu học tập) * Thực hiện nhiệm vụ HS: Thực hiện nhiệm vụ tự trả lời câu hỏi vào phiếuhọc tập. GV: Quan sát giúp đỡ HS khi cần thiết. Sau 5 phút tiến hành cho các bàn (cặp đôi) cạnh nhau trao đổi phiếu học tập và tìm hiểu phần còn lại (bàn 1,3,5,... làm phiếu 2, bàn 2,4,6,... đọc SGK, hoàn thành phiếu học tập 1) trong thời gian 5 phút. HS: Thực hiện nhiệm vụ,hoàn thành phiếu học tập. * Báo cáo, thảo luận GV: yêu cầu đại diện 1 cặp đôi bàn chẵn và 1 cặp đôi bàn lẻ trả lời trước lớp, các nhóm khác cho ý kiến chia sẻ. HS: Thực hiện trả lời và chia sẻ. *Đánh giá kết quả thực hiện nhiệm vụ - Học sinh nhận xét, bổ sung, đánh giá. - GV nhận xét và chốt nội dung GV:Chiếu slide đáp án và lưu ý có một loại hạt nhân của nguyên tử hydrogen chỉ có 1proton, không có neutron. GV: Đưa ra kết luận * Chuyển giao nhiệm vụ học tập số 2 GV: Chia lớp làm 4- 6 nhóm yêu cầu học sinh quan sát mô hình nguyên tử trong hình 2.5 và hoàn thành phiếu học tập số 3 sau trong thời gian 7 phút. * Thực hiện nhiệm vụ 2. HS: Thực hiện thảo luận nhóm. GV: Quan sát giúp đỡ các em khi cần. *Báo cáo kết quả và thảo luận GV gọi ngẫu nhiên một HS đại diện cho một nhóm trình bày, các nhóm khác bổ sung (nếu có). *Đánh giá kết quả thực hiện nhiệm vụ - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. - GV nhận xét và chốt nội dung |
III. Cấu tạo nguyên tử 1. Hạt nhân nguyên tử - Hạt nhân gồm 2 loại hạt là proton(p) mang điện tích dương và neutron(n) không mang điện. - Mỗi hạt proton mang 1 đơn vị điện tích dương, kí hiệu +1. Tổng số điện tích(kí hiệu Z) bằng tổng số hạt proton. 2. Vỏ nguyên tử - Vỏ nguyên tử được tạo nên bởi các electron (e) . Mỗi electron mang 1 đơn vị điện tích âm, kí hiệu -1. - Các electron sắp xếp thành từng lớp từ trong ra ngoài cho đến hết. Lớp thứ nhất (trong cùng gần hạt nhân nhất) có tối đa 2e, lớp thứ hai có tối đa 8e... Kết luận Nguyên tử là hạt vô cùng nhỏ gồm hạt nhân mang điện tích dương và vỏ mang điện tích âm. Nguyên tử trung hòa về điện nên tổng số proton = tổng số electron. |
Hoạt động 5. Tìm hiểu khối lượng nguyên tử
a) Mục tiêu: Học sinh hiểu được khối lượng của nguyên tử tập trung hầu hết ở hạt nhân. Vận dụng tính được khối lượng của nguyên tử khi biết số hạt proton, neutron trong hạt nhân.
b) Nội dung:
-HS đọc SGK và trả lời câu hỏi 1,2 SGK trang 18.
c. Sản phẩm: Câu trả lời của học sinh:
Câu hỏi 1:
Khối lượng 1 proton ≈ khối lượng 1 neutron ≈ 1 amu.
Khối lượng 1 electron ≈ 0,00055 amu nhỏ hơn rất nhiều so với khối lượng của proton và neutron.
⇒ Coi khối lượng hạt nhân nguyên tử là khối lượng của nguyên tử.
Câu hỏi 2
Khối lượng hạt nhân nguyên tử có thể coi là khối lượng của nguyên tử.
Khối lượng của nguyên tử nhôm bằng 13.1 amu + 14.1 amu = 27 amu
Khối lượng của nguyên tử đồng bằng 29.1 amu + 36.1 amu = 64 amu
⇒ Khối lượng của nguyên tử nhôm nhỏ hơn khối lượng của nguyên tử đồng.
d) Tổ chức thực hiện
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH |
NỘI DUNG |
|
* Chuyển giao nhiệm vụ học tập GV: Giới thiệu khối lượng nguyên tử (đơn vị là amu) sẽ bằng tổng khối lượng của các hạt trong nguyên tử. -Yêu cầu học sinh đọc SGK và trả lời câu hỏi trang 18. * Thực hiện nhiệm vụ HS: Thực hiện nhiệm vụ tự trả lời câu hỏi vào phiếu học tập. GV: Quan sát giúp đỡ khi cần thiết. * Báo cáo, thảo luận GV: Yêu cầu đại diện 1 HS trả lời trước lớp, Các HS khác cho ý kiến chia sẻ. HS: Thực hiện trả lời và chia sẻ. *Đánh giá kết quả thực hiện nhiệm vụ - Học sinh nhận xét, bổ sung, đánh giá. - GV nhận xét và chốt nội dung. |
IV. Khối lượng nguyên tử Khối lượng nguyên tử = Khối lượng hạt nhân = Tổng số p + tổng số n (aum) |
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu
- Ôn tập, củng cố kiến thức sau khi học xong bài.
b) Nội dung
- HS thảo luận nhóm hoàn thành phiếu học tập 4.
|
PHIẾU HỌC TẬP 4 Bài 1. Hoàn thành thông tin trong bảng sau
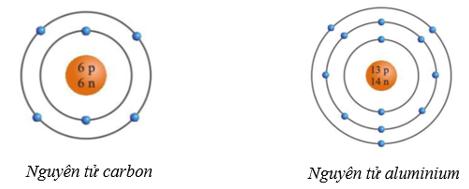
Bài 2. Nguyên tử nitrogen và silicon có số electron lần lượt là 7 và 14. Hãy cho biết nguyên tử nitrogen và silicon có bao nhiêu lớp electron và có bao nhiêu electron ở lớp ngoài cùng. Bài 3. Quan sát hình hãy cho biết: a) Số proton, neutron, electron trong mỗi nguyên tử carbon và aluminium. b) Khối lượng nguyên tử carbon và aluminium. Bài 4. Aluminium là kim loại có nhiều ứng dụng trong thực tiễn, được dùng làm dây dẫn điện, chế tạo các thiết bị, máy móc trong công nghiệp và nhiều đồ dùng sinh hoạt. Cho biết tổng số hạt trong hạt nhân nguyên tử aluminium là 27, số đơn vị điện tích hạt nhân là 13. Nêu cách tính số hạt mỗi loại trong nguyên tử aluminium và cho biết điện tích hạt nhân của aluminium. |
c) Sản phẩm
- Dự kiến sản phẩm của HS:
|
PHIẾU HỌC TẬP 4 Bài 1. Hoàn thành thông tin trong bảng sau
Bài 2. - Đối với nguyên tử nitrogen có 7 electron được sắp xếp vào 2 lớp + Lớp thứ nhất có 2 electron. + Lớp thứ hai có 5 electron. ⇒Nguyên tử nitrogen có 5 electron ở lớp ngoài cùng. - Đối với nguyên tử silicon có 14 e được sắp xếp vào 3 lớp. + Lớp thứ nhất có 2 electron. + Lớp thứ hai có 8 electron. + Lớp thứ ba có 4 electron. ⇒ Nguyên tử silicon có 4 electron lớp ngoài cùng. Bài 3. * Nguyên tử carbon a. Trong nguyên tử carbon có 6 proton; 6 neutron; 6 electron. b. Trong nguyên tử carbon có 6 proton; 6 neutron nên khối lượng của một nguyên tử carbon là: 6.1 + 6.1 = 12 (amu) * Nguyên tử aluminium a. Trong nguyên tử aluminium có 13 proton; 14 neutron; 13 electron. b. Trong nguyên tử aluminium có 13 proton; 14 neutron nên khối lượng của một nguyên tử aluminium là: 13.1 + 14.1 = 27 (amu) Bài 4. Số đơn vị điện tích hạt nhân = Số proton = Số electron = 13 Số hạt trong hạt nhân nguyên tử = số proton + số neutron ⇒ 27 = 13 + số neutron ⇒ số neutron = 27 - 13 = 14. Aluminium có 13 proton ⇒ Điện tích hạt nhân của aluminium: +13. |
d) Tổ chức thực hiện
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH |
NỘI DUNG |
|
* Chuyển giao nhiệm vụ học tập GV chia lớp thành 4 nhóm. Phát phiếu học tập số 3. + Nhóm 1: Câu 1 + Nhóm 2: Câu 2 + Nhóm 3: Câu 3 + Nhóm 4: Câu 4. * Thực hiện nhiệm vụ HS thảo luận nhóm và hoàn thành phiếu học tập 3 *Báo cáo kết quả và thảo luận - GV gọi các nhóm trình bày bài làm của nhóm mình. - Các nhóm khác nhận xét và đối chiếu với kết quả của GV chiếu trên slide. * Đánh giá kết quả thực hiện nhiệm vụ GV đánh giá bài làm của các nhóm. |
- Dự kiến sản phẩm của HS (mục 3) |
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu
- Vận dụng kiến thức đã học vào cuộc sống.
b) Nội dung
- HS làm việc cá nhân, tại nhà.
c) Sản phẩm
- Báo cáo của HS.
d) Tổ chức thực hiện
* Chuyển giao nhiệm vụ
- GV chiếu slide câu hỏi vận dụng:
- Yêu cầu HS làm cá nhân tại nhà và hoàn thành.
* Thực hiện nhiệm vụ
- HS làm việc tại nhà.
* Báo cáo, thảo luận
- HS nộp sản phẩm vào buổi học sau.
* Tổng kết, chốt kiến thức
- GV tổng kết và có thể chấm điểm.
................................
................................
................................
Trên đây tóm tắt một số nội dung có trong bộ Giáo án Khoa học tự nhiên 7 Kết nối tri thức năm 2023 mới nhất, để mua tài liệu đầy đủ, Thầy/Cô vui lòng: