Trắc nghiệm Hóa học 10 Bài 4 (có đáp án): Mô hình nguyên tử và orbital nguyên tử - Cánh diều
Haylamdo biên soạn và sưu tầm 10 bài tập trắc nghiệm Hóa học 10 Bài 4: Mô hình nguyên tử và orbital nguyên tử sách Cánh diều có đáp án và lời giải chi tiết đầy đủ các mức độ sẽ giúp học sinh ôn luyện trắc nghiệm để biết cách làm các dạng bài tập Hóa 10
Trắc nghiệm Hóa học 10 Bài 4 (có đáp án): Mô hình nguyên tử và orbital nguyên tử - Cánh diều
Câu 1. Mô hình nguyên tử theo Rutherford – Bohr không có nội dung nào sau đây?
A. Khối lượng nguyên tử tập trung chủ yếu ở hạt nhân.
B. Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
C. Electron mang điện tích âm nên bị hút vào hạt nhân.
D. Năng lượng của electron phụ thuộc vào khoảng cách từ electron đó tới hạt nhân nguyên tử. Electron ở càng xa hạt nhân thì có năng lượng càng cao.
Câu 2. Theo mô hình nguyên tử Rutherford – Bohr, electron thuộc lớp nào sau đây có năng lượng thấp nhất?
A. Lớp N.
B. Lớp L.
C. Lớp M.
D. Lớp K.
Câu 3. Phát biểu nào sau đây không đúng?
A. Các electron được phân bố vào lớp gần hạt nhân trước.
B. Số electron tối đa trong mỗi lớp là 2n (n là số thứ tự lớp electron, n ≤ 4).
C. Năng lượng của các electron ở lớp trong thấp hơn năng lượng electron ở lớp ngoài.
D. Sự liên kết giữa electron trên lớp K với hạt nhân là bền chặt nhất.
Câu 4. Số electron tối đa trên lớp L là
A. 4.
B. 6.
C. 2.
D. 8.
Câu 5. Cho cấu trúc nguyên tử aluminium theo mô hình Rutherford – Bohr như sau:
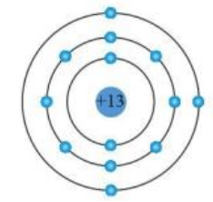
Lớp ngoài cùng của nguyên tử aluminium có bao nhiêu electron?
A. 2.
B. 3.
C. 5.
D. 8.
Câu 6. Sự khác biệt cơ bản giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử là
A. Electron được phân bố vào các lớp (mô hình Rutherford – Bohr) và electron chuyển động tập trung tại một góc gần hạt nhân (mô hình hiện đại).
B. Electron chuyển động bị hút vào hạt nhân (mô hình Rutherford – Bohr) và electron chuyển động không thể bị hút vào hạt nhân (mô hình hiện đại).
C. Electron chuyển động rất nhanh (mô hình Rutherford – Bohr) và electron chuyển động rất chậm (mô hình hiện đại).
D. Electron chuyển động theo quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời (mô hình Rutherford – Bohr) và electron chuyển động không theo quỹ đạo cố định (mô hình hiện đại).
Câu 7. Khu vực không gian xung quanh hạt nhân nguyên tử mà xác xuất tìm thấy electron ở khu vực đó là lớn nhất (khoảng 90%) gọi là
A. lớp vỏ electron.
B. orbital nguyên tử.
C. cấu hình nguyên tử.
D. trọng tâm nguyên tử.
Câu 8. Phát biểu nào sau đây là đúng khi nói về hình dạng của orbital nguyên tử?
A. AO s hình số tám nổi; AO p hình cầu.
B. AO s hình vuông; AO p hình cầu.
C. AO s hình cầu; AO p hình số tám nổi.
D. AO s hình cầu; AO p hình vuông.
Câu 9. Một AO chỉ chứa tối đa
A. 1 electron.
B. 2 electron.
C. 3 electron.
D. 4 electron.
Câu 10. Electron chuyển từ lớp gần hạt nhân ra lớp xa hạt nhân thì phải
A. giải phóng năng lượng.
B. vừa giải phóng năng lượng và vừa thu năng lượng.
C. thu năng lượng.
D. va chạm vào hạt nhân rồi bắn ra.
Câu 11. Nguyên tử nguyên tố sodium có 11 electron. Nguyên tử này có
A. 1 electron.
B. 2 electron.
C. 3 electron.
D. 4 electron.
Câu 12. Nguyên tử nguyên tố magnesium có 3 lớp electron, trong đó lớp ngoài cùng có 2 electron. Số proton trong nguyên tử magnesium là
A. 10.
B. 13.
C. 11.
D. 12.
Câu 13. Nguyên tử nguyên tố X có 8 neutron và có số khối là 16. Lớp ngoài cùng của nguyên tử X có
A. 2 electron.
B. 3 electron.
C. 1 electron.
D. 6 electron.
Câu 14. Cho mô hình nguyên tử của nguyên tố nitrogen (N) như sau:
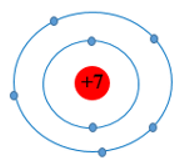
Số proton và số electron lớp ngoài cùng của nguyên tử N lần lượt là
A. 7 và 7.
B. 7 và 2.
C. 6 và 5.
D. 7 và 5.
Câu 15. Nguyên tử nguyên tố Y có tổng số hạt cơ bản là 48, trong đó số hạt mang điện gấp đôi số hạt không mang điện. Nguyên tố Y là
A. sodium (Na).
B. calcium Ca).
C. boron (B).
D. magnesium (Mg).
Câu 1:
Mô hình nguyên tử theo Rutherford – Bohr không có nội dung nào sau đây?
A. Khối lượng nguyên tử tập trung chủ yếu ở hạt nhân.
B. Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
C. Electron mang điện tích âm nên bị hút vào hạt nhân.
D. Năng lượng của electron phụ thuộc vào khoảng cách từ electron đó tới hạt nhân nguyên tử. Electron ở càng xa hạt nhân thì có năng lượng càng cao.
Câu 2:
Theo mô hình nguyên tử Rutherford – Bohr, electron thuộc lớp nào sau đây có năng lượng thấp nhất?
A. Lớp N.
B. Lớp L.
C. Lớp M.
D. Lớp K.
Câu 3:
Phát biểu nào sau đây không đúng?
A. Các electron được phân bố vào lớp gần hạt nhân trước.
B. Số electron tối đa trong mỗi lớp là 2n (n là số thứ tự lớp electron, n ≤ 4).
C. Năng lượng của các electron ở lớp trong thấp hơn năng lượng electron ở lớp ngoài.
D. Sự liên kết giữa electron trên lớp K với hạt nhân là bền chặt nhất.
Câu 5:
Cho cấu trúc nguyên tử aluminium theo mô hình Rutherford – Bohr như sau:
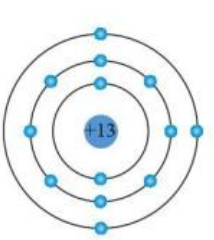
Lớp ngoài cùng của nguyên tử aluminium có bao nhiêu electron?
A. 2.
B. 3.
C. 5.
D. 8.
Câu 6:
Sự khác biệt cơ bản giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử là
A. Electron được phân bố vào các lớp (mô hình Rutherford – Bohr) và electron chuyển động tập trung tại một góc gần hạt nhân (mô hình hiện đại).
B. Electron chuyển động bị hút vào hạt nhân (mô hình Rutherford – Bohr) và electron chuyển động không thể bị hút vào hạt nhân (mô hình hiện đại).
C. Electron chuyển động rất nhanh (mô hình Rutherford – Bohr) và electron chuyển động rất chậm (mô hình hiện đại).
D. Electron chuyển động theo quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời (mô hình Rutherford – Bohr) và electron chuyển động không theo quỹ đạo cố định (mô hình hiện đại).
Câu 7:
Khu vực không gian xung quanh hạt nhân nguyên tử mà xác xuất tìm thấy electron ở khu vực đó là lớn nhất (khoảng 90%) gọi là
A. lớp vỏ electron.
B. orbital nguyên tử.
C. cấu hình nguyên tử.
D. trọng tâm nguyên tử.
Câu 8:
Phát biểu nào sau đây là đúng khi nói về hình dạng của orbital nguyên tử?
A. AO s hình số tám nổi; AO p hình cầu.
B. AO s hình vuông; AO p hình cầu.
C. AO s hình cầu; AO p hình số tám nổi.
D. AO s hình cầu; AO p hình vuông.
Câu 10:
Electron chuyển từ lớp gần hạt nhân ra lớp xa hạt nhân thì phải
A. giải phóng năng lượng.
B. vừa giải phóng năng lượng và vừa thu năng lượng.
C. thu năng lượng.
D. va chạm vào hạt nhân rồi bắn ra.
Câu 11:
Nguyên tử nguyên tố sodium có 11 electron. Nguyên tử này có
A. 1 lớp electron.
B. 2 lớp electron.
C. 3 lớp electron.
D. 4 lớp electron.
Câu 12:
Nguyên tử nguyên tố magnesium có 3 lớp electron, trong đó lớp ngoài cùng có 2 electron. Số proton trong nguyên tử magnesium là
A. 10.
B. 13.
C. 11.
D. 12.
Câu 13:
Nguyên tử nguyên tố X có 8 neutron và có số khối là 16. Lớp ngoài cùng của nguyên tử X có
A. 2 electron.
B. 3 electron.
C. 1 electron.
D. 6 electron.
Câu 14:
Cho mô hình nguyên tử của nguyên tố nitrogen (N) như sau:
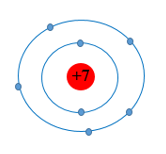
Số proton và số electron lớp ngoài cùng của nguyên tử N lần lượt là
A. 7 và 7.
B. 7 và 2.
C. 6 và 5.
D. 7 và 5.
Câu 15:
Nguyên tử nguyên tố Y có tổng số hạt cơ bản là 48, trong đó số hạt mang điện gấp đôi số hạt không mang điện. Nguyên tố Y là
A. sodium (Na).
B. calcium Ca).
C. boron (B).
D. magnesium (Mg).

