Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Điều kiện phản ứng
- Điều kiện thường.
Cách thực hiện phản ứng
- Cho Al2O3 phản ứng với dung dịch axit H2SO4 đặc tạo muối nhôm sunfat và nước.
Hiện tượng nhận biết phản ứng
- Phản ứng hoà tan chất rắn nhôm oxit và tạo dung dịch trong suốt.
Bạn có biết
- Các oxit kim loại khác đạt hóa trị cao nhất cũng tác dụng với dung dịch axit H2SO4 tạo muối mới có hóa trị cao nhất và nước.
- Oxit kim loại chưa đạt hóa trị cao nhất tác dụng với H2SO4 đặc xảy ra phản ứng oxi hóa khử tạo muối có hóa trị cao nhất và sản phẩm khử.

Ví dụ minh họa
Ví dụ 1:Dung dịch H2SO4 loãng phản ứng được với tất cả các chất trong dãy nào sau đây?
A. BaCl2, Na2CO3, Al2O3.
B. FeCl3, Al2O3, Cu.
C. CuO, NaCl, CuS.
D. Al2O3, Ba(OH)2, Ag.
Hướng dẫn giải
Chọn A.
B sai, Cu không tác dụng với dung dịch H2SO4 loãng.
C sai, CuO không tác dụng với dung dịch H2SO4 loãng.
D sai, Ag không tác dụng với dung dịch H2SO4 loãng.
Ví dụ 2:Trong các chất dưới đây chất nào không tác dụng với H2SO4?
A. Cu.
B. Al2O3.
C. Fe.
D. BaCl2.
Hướng dẫn giải
Chọn A.
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Fe + H2SO4 → FeSO4 + H2↑
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ví dụ 3:Khối lượng Al2O3 bị hòa tan trong 300 ml dung dịch H2SO4 0,5M là bao nhiêu?
A. 3,1 gam.
B. 5,2 gam.
C. 6,1 gam.
D. 5,1 gam.
Hướng dẫn giải
Chọn D.
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
nH2SO4=0,5.0,3=0,15 mol
⇒ nAl2O3=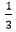
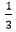
Vậy mAl2O3=0,05.102=5,1 gam

 4Al + 3O2↑
4Al + 3O2↑