C3H4 + 4O2 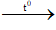 3CO2 + 2H2O - Cân bằng phương trình hoá học
3CO2 + 2H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
C3H4 + 4O2 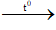
Điều kiện phản ứng
- Nhiệt độ cao.
Cách thực hiện phản ứng
- Đốt cháy propin trong oxi ở điều kiện nhiệt độ cao.
Hiện tượng nhận biết phản ứng
- Khi đốt cháy propin trong oxi ở nhiệt độ cao thì thấy có khí thoát ra (CO2).
Bạn có biết
- Phản ứng trên là phản ứng oxi hóa hoàn toàn.
- Phản ứng cháy của propin tỏa nhiều nhiệt.
- Số mol CO2 > H2O và số mol ankin phản ứng bằng hiệu số mol của CO2 và H2O.

Ví dụ minh họa
Ví dụ 1: Đốt cháy 4g C3H4. Sản phẩm cháy cho đi qua nước vôi trong dư. Khối lượng kết tủa thu được là?
A. 30g
B. 40g
C. 20g
D. 50g
Hướng dẫn
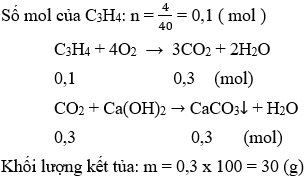
Đáp án A
Ví dụ 2: Đốt cháy 4g C3H4. Sản phẩm cháy cho đi qua nước vôi trong dư. Khối lượng bình tăng hay giảm bao nhiêu?
A. 10g
B. 12,6g
C. 13,2g
D. 10,6g
Hướng dẫn:
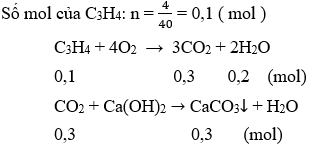
Khối lượng bình: m = 0,3 x 100 - 0,3 x 44 + 0,2 x 18 = 13,2 (g)
Đáp án C
Ví dụ 3: Đốt cháy hoàn toàn khí propin rồi sục hỗn hợp khí thu được qua dung dịch nước vôi trong. Hiện tượng thu được là gì?
A. Kết tủa trắng
B. Có khí thoát ra
C. Không có hiện tượng
D. Dung dịch nước vôi có màu vàng
Hướng dẫn:
C3H4 + 4O2 → 3CO2 + 2H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Đáp án A

