CH2=CH–CH3 + Br2 → CH2Br–CHBr–CH3 - Cân bằng phương trình hoá học
Phản ứng hoá học:
CH2=CH–CH3 + Br2 → CH2Br–CHBr–CH3
Điều kiện phản ứng
- Phản ứng xảy ra ở điều kiện thường,
Cách thực hiện phản ứng
- Dẫn khí propilen từ từ qua dung dịch brom thấy màu nâu đỏ của dung dịch nhạt dần.
Hiện tượng nhận biết phản ứng
- Màu nâu đỏ của dung dịch nhạt dần.
Bạn có biết
- Phản ứng trên gọi là phản ứng cộng.
- Các đồng đẳng của propilen đều làm mất màu dung dịch brom.
- Phản ứng trên dung để phân biệt anken với ankan.

Ví dụ minh họa
Ví dụ 1: Dẫn 3,36 lít (đktc) hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7g. CTPT của 2 anken là
A. C2H4 và C3H6.
B. C3H6 và C4H8.
C. C4H8 và C5H10.
D. C5H10 và C6H12.
Hướng dẫn
nX = 0,15 mol
mbình tăng = manken = 7,7g
Gọi 2 anken là CnH2n và CmH2m mol tương ứng là a và b mol
⇒ a + b = 0,15 mol và 14na + 14mb = 7,7g
Chọn n = 2; m = 3 ⇒ a = -0,1 loại
n = 2; m = 4 ⇒ a = 0,025 mol b = 0,125 mol
⇒ 2 anken là C2H4 và C4H8
n = 3; m = 4 ⇒ a = 0,05 và b = 0,1 mol
⇒ 2 anken là C3H6 và C4H8
Đáp án B.
Ví dụ 2: Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 4,2 g. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,1.
B. 0,1 và 0,05.
C. 0,12 và 0,03.
D. 0,03 và 0,12.
Hướng dẫn
nhh = 0,15 mol; mtăng = mpropilen = 4,2 g
⇒ npropilen = 0,1 mol ⇒ npropan = 0,05 mol
Đáp án A.
Ví dụ 3: Một hỗn hợp X có thể tích 11,2 lít (đktc), X gồm 2 anken đồng đẳng kế tiếp nhau. Khi cho X qua nước Br2 dư thấy khối lượng bình Br2 tăng 15,4g. Xác định CTPT và số mol mỗi anken trong hỗn hợp X.
A. 0,2 mol C2H4 và 0,3 mol C3H6
B. 0,2 mol C3H6 và 0,2 mol C4H8
C. 0,4 mol C2H4 và 0,1 mol C3H6
D. 0,3 mol C2H4 và 0,2 mol C3H6
Hướng dẫn
nX = 0,5 mol; mX = mtăng = 15,4
MX = 15,4/0,5 = 30,8 ⇒ hai anken lần lượt là C2H4 và C3H6
Sơ đồ đường chéo:
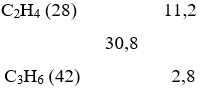
⇒ netilen/npropilen = ¼ ⇒ netilen = 0,4 mol ; npropilen = 0,1 mol
Đáp án C.

