Mg(OH)2 + H2SO4 → MgSO4 + 2H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
Mg(OH)2 + H2SO4 → MgSO4 + 2H2O
Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
Cách thực hiện phản ứng
- Nhỏ từ từ H2SO4 vào ống nghiệm chứa Mg(OH)2
Hiện tượng nhận biết phản ứng
- Mg(OH)2 tan dần tạo dung dịch.
Bạn có biết
- Các bazơ đều phản ứng với dung dịch axit tạo thành muối và nước.

Ví dụ minh họa
Ví dụ 1:
Cho 0,01 mol Mg(OH)2 phản ứng vừa đủ với 100ml H2SO4 aM. Giá trị của a là
A. 0,1. B. 0,01. C. 0,05. D. 0,2.
Hướng dẫn giải:
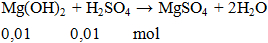
a = 0,01 : 0,1 = 0,1M.
Đáp án A.
Ví dụ 2:
Cần bao nhiêu ml H2SO4 0,2M để hòa tan hoàn toàn 5,8 gam Mg(OH)2?
A. 100 ml. B. 200 ml. C. 500 ml. D. 150 ml.
Hướng dẫn giải:
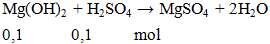
V = 0,1 : 0,2 = 0,5 lít = 500ml.
Đáp án C.
Ví dụ 3:
Cho 100ml H2SO4 0,2M phản ứng vừa đủ với Mg(OH)2 thu được dung dịch X. Khối lượng muối tan có trong dung dịch X là
A. 2,40g. B. 1,45g. C. 5,85g. D. 9,20g.
Hướng dẫn giải:
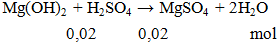
mmuối = 0,02.120 = 2,4 gam.
Đáp án A.

