3Na2CO3 + 2AlCl3 + 3H2O → 6NaCl + 2Al(OH)3↓ + 3CO2↑ - Cân bằng phương trình hoá học
Phản ứng hoá học:
3Na2CO3 + 2AlCl3 + 3H2O → 6NaCl + 2Al(OH)3↓ + 3CO2↑
Điều kiện phản ứng
- điều kiện thường,
Cách thực hiện phản ứng
- Nhỏ Na2CO3 vào ống nghiệm chứa AlCl3.
Hiện tượng nhận biết phản ứng
- Có kết tủa trắng và sủi bọt khí.
Bạn có biết
- Khi cho dung dịch muối của nhôm phản ứng với Na2CO3 đều thấy có sủi bọt khí và xuất hiện kết tủa trắng.

Ví dụ minh họa
Ví dụ 1:
Khi cho AlCl3 vào ống nghiệm chứa Na2CO3 thu được hiện tượng là
A. Có kết tủa trắng thoát ra và sủi bọt khí.
B. Có khí màu nâu đỏ thoát ra.
C. Có kết tủa vàng.
D. Không có hiện tượng gì.
Hướng dẫn giải
3Na2CO3 + 2AlCl3 + 3H2O → 6NaCl + 2Al(OH)3↓ + 3CO2↑
2Al(OH)3: kết tủa trắng.
CO2: khí không màu,
Đáp án A.
Ví dụ 2:
Thể tích khí CO2 ở dktc thoát ra khi cho 10,6g Na2CO3 phản ứng hoàn toàn với lượng dung dịch AlCl3 là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Hướng dẫn giải
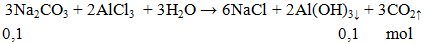
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Ví dụ 3:
Khối lượng kết tủa thu được khi cho 15,9g Na2CO3 phản ứng hoàn toàn với lượng dung dịch AlCl3 là
A. 0,78g. B. 7,8g. C. 0,87g. D. 8,7g.
Hướng dẫn giải
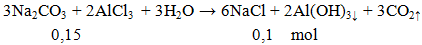
m = 0,1.78 = 7,8g.
Đáp án B.

