Lý thuyết Hóa học 12 Bài 16: Hợp kim – Sự ăn mòn kim loại - Chân trời sáng tạo
Haylamdo biên soạn tóm tắt lý thuyết Hóa 12 Bài 16: Hợp kim – Sự ăn mòn kim loại sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh lớp 12 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 12.
Lý thuyết Hóa 12 Bài 16: Hợp kim – Sự ăn mòn kim loại - Chân trời sáng tạo
I. HỢP KIM
1. Khái niệm hợp kim và việc sử dụng phổ biến hợp kim
- Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim.
- Hợp kim có nhiều tính chất cơ học, tính chất vật lí vượt trội so với kim loại, ngày càng được sử dụng phổ biến trong các ngành kinh tế quốc dân.
2. Một số tính chất của hợp kim
Hợp kim có nhiều tính chất hoá học tương tự tính chất hoá học của các đơn chất thành phần, tuy nhiên tính chất vật lí và tính chất cơ học của hợp kim khác so với tính chất của các đơn chất thành phần.
Ví dụ: Inox (hợp kim của Fe với C, Cr, Ni … ) hay còn gọi là thép không gỉ, ít bị ăn mòn nên được dùng để chế tạo các dụng cụ y tế, dụng cụ nhà bếp, ...
3. Thành phần, tính chất và ứng dụng một số hợp kim quan trọng của sắt và nhôm
a) Hợp kim của sắt
Sắt có độ tinh khiết cao ít được sử dụng trong thực tế nhưng các hợp kim của sắt là gang và thép được sử dụng rất phổ biến trong sản xuất và đời sống.
- Gang là hợp kim của Fe và C, trong đó C chiếm khoảng từ 2 – 5 % về khối lượng. Trong gang có một lượng nhỏ các nguyên tố khác như: Si, S, Mn, P, ...
- Thép là hợp kim của Fe và C, trong đó C chiếm dưới 2% về khối lượng. Trong thép còn có thể có một số nguyên tố khác như: Si, Mn, Cr, Ni …
Thành phần, tính chất và ứng dụng của một số loại thép
|
Loại thép |
Thành phần |
Tính chất |
Ứng dụng |
|
Thép carbon |
Fe, C |
Cứng |
Thép tấm, xây dựng nhà cửa, vật dụng trong đời sống, .. |
|
Thép manganese |
Fe, C, Mn |
Cứng, chống mài mòn |
Đường ray xe lửa, két sắt, máy nghiền đá, ... |
|
Thép không gỉ |
Fe, C, Cr, Ni |
Chống ăn mòn |
Dụng cụ y tế, nhà bếp; vòng bi, vỏ xe bọc thép; ... |
b) Hợp kim của nhôm
Một trong những hợp kim quan trọng của nhôm được sử dụng phổ biến trong nhiều lĩnh vực là dural (duralumin), với thành phần chính là Al, Cu và một số nguyên tố khác như Mg, Mn, Fe, Si … Hợp kim này có nhiều ưu điểm như nhẹ, bền trong không khí và nước nên được sử dụng làm vật liệu chế tạo máy bay, ô tô, tên lửa, tàu vũ trụ, ... Hợp kim nhôm có màu trắng bạc, đẹp nên được sử dụng làm khung cửa và trang trí nội thất.
II. ĂN MÒN KIM LOẠI
1. Khái niệm ăn mòn kim loại
- Sự ăn mòn kim loại là sự phá huỷ kim loại hoặc hợp kim do tác dụng của các chất trong môi trường.
- Hằng năm, sự ăn mòn kim loại làm tổn thất nhiều về kinh tế, thậm chí gây nguy hiểm cho người lao động khi vận hành các thiết bị máy móc tại các công trình dân dụng, công nghiệp, nông nghiệp, viễn thông, điện lực, dầu khí, quân sự, quốc phòng và đặc biệt là các công trình ven biển, ...
2. Phân loại ăn mòn kim loại
Có hai loại ăn mòn chính: ăn mòn hoá học và ăn mòn điện hoá.
a. Ăn mòn hoá học
- Ăn mòn hoá học là quá trình oxi hoá - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn hoá học thường xảy ra ở các chi tiết bằng kim loại của máy móc dùng trong các nhà máy sản xuất hoá chất, những bộ phận của thiết bị lò đốt, nồi hơi, các chi tiết của động cơ đốt tronghoặc những thiết bị thường xuyên phải tiếp xúc với hơi nước, khí oxygen, ... - Nhiệt độ càng cao, tốc độ ăn mòn kim loại càng nhanh.
Ví dụ:
3Fe + 2O2 Fe3O4
3Fe + 4H2O Fe3O4 + 4H2
b. Ăn mòn điện hoá
- Ăn mòn điện hoá là quá trình ăn mòn kim loại do sự tạo thành pin điện hoá. Ăn mòn điện hoá là loại ăn mòn kim loại rất phổ biến và gây hậu quả nghiêm trọng trong đời sống.
- Ví dụ: Sự ăn mòn điện hoá kim loại trong không khí ẩm.
Trong không khí ẩm, trên bề mặt của gang thép luôn có một lớp nước mỏng đã hoà tan khí oxygen và carbon dioxide tạo thành dung dịch chất điện li. Sắt và các thành phần khác (chủ yếu là carbon) cùng tiếp xúc với dung dịch đó, tạo nên vô số pin điện hoá rất nhỏ mà anode là sắt và cathode là carbon.
+ Ở anode, xảy ra quá trình oxi hoá:
Fe(s) Fe2+(aq) + 2e
+ Ở cathode, xảy ra quá trình khử:
Fe2+ tiếp tục bị oxi hoá bởi oxygen không khí, tạo thành gỉ sắt có thành phần chính là Fe2O3.nH2O.
- Điều kiện xảy ra ăn mòn điện hoá:Hai kim loại khác nhau (hoặc kim loại và phi kim) tiếp xúc trực tiếp hoặc gián tiếp với nhau thông qua dây dẫn và cùng tiếp xúc với một dung dịch chất điện li.
Chú ý: Thực tế, các quá trình ăn mòn kim loại diễn ra rất phức tạp, thường gồm cả ăn mòn hoá học và ăn mòn điện hoá. Tuy nhiên, ăn mòn điện hoá thường xảy ra phổ biến hơn.
III. CHỐNG ĂN MÒN KIM LOẠI
Có nhiều phương pháp chống ăn mòn kim loại, trong đó phổ biến là phương pháp bảo vệ bề mặt và phương pháp điện hoá.
1. Phương pháp bảo vệ bề mặt
Trong phương pháp bảo vệ bề mặt, người ta phủ lên bề mặt kim loại những chất bền với môi trường hoặc tráng, mạ bằng một kim loại khác.
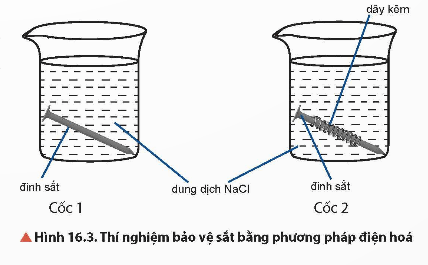
2. Phương pháp điện hoá
Phương pháp điện hoá được thực hiện bằng cách nối kim loại cần được bảo vệ với một kim loại hoạt động hoá học mạnh hơn để tạo thành pin điện hoá. Khi đó, kim loại có tính khử mạnh hơn bị ăn mòn, kim loại có tính khử yếu hơn được bảo vệ.