2C2H6 + 7O2 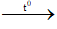 4CO2 + 6H2O - Cân bằng phương trình hoá học
4CO2 + 6H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
2C2H6 + 7O2 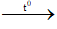
Điều kiện phản ứng
- Nhiệt độ
Cách thực hiện phản ứng
- Đốt cháy hoàn toàn khí etan (C2H6) trong không khí thì thu được khí cacbonic và nước.
Hiện tượng nhận biết phản ứng
- Dẫn sản phẩm cháy qua bình đựng nước vôi trong dư thấy có kết tủa trắng xuất hiện.
Bạn có biết
- Phản ứng trên được gọi là phản ứng đốt cháy.
- Tương tự etan, các ankan khi bị đốt đều cháy và tỏa nhiều nhiệt.
- Nếu thiếu oxi, phản ứng cháy của ankan xảy ra không hoàn toàn: sản phẩm cháy ngoài CO2, H2O còn có C, CO...
- Khi đốt cháy ankan, số mol H2O thu được sau phản ứng luôn lớn hơn số mol CO2.

Ví dụ minh họa
Ví dụ 1: Hỗn hợp khí A gồm etan và propan. Đốt cháy hoàn toàn 16,2g hỗn hợp khí A thu được khí CO2 và hơi H2O theo tỉ lệ mol 11:15. Tính thành phần % theo khối lượng của khí etan trong hỗn hợp khí A là bao nhiêu?
A. 18,51%
B. 37,04%
C. 27,78%
D. 46,29%
Hướng dẫn:.
Đặt nC2H6 = x mol ; nC3H8 = y mol
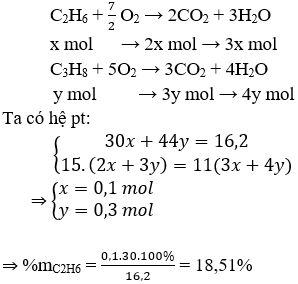
Đáp án A.
Ví dụ 2: Đốt cháy hoàn toàn 2,24 lít hỗn hợp A (đktc) gồm : CH4, C2H6 và C3H8 thu được V lít khí CO2(đktc) và 7,2 g nước. Giá trị của V là:
A. 5,6 l
B. 6,72 l
C. 4,48 l
D. 2,24 l
Hướng dẫn:
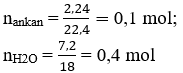
Ta có:
nankan = nH2O – nCO2
⇒ nCO2 = 0,4 – 0,1 = 0,3 mol
⇒ VCO2 = 0,3.22,4 = 6,72 l
Đáp án B.
Ví dụ 3: Đốt cháy hoàn toàn hỗn hợp X gồm 2 ankan đồng đẳng kế tiếp , khối lượng 4,6 gam thu được 6,72 lít CO2(đktc). Tìm CTPT của 2 ankan.
A. CH4 và C2H6
B. C2H6 và C3H8
C. C3H8 và C4H10
D. C4H10 và C5H10
Hướng dẫn:
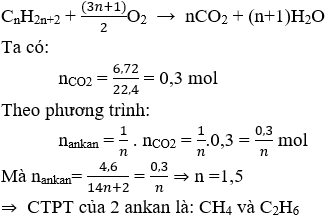
Đáp án A.

