CH2=CH–CH2–CH3 + H2 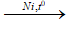 CH3–CH2–CH2–CH3 - Cân bằng phương trình hoá học
CH3–CH2–CH2–CH3 - Cân bằng phương trình hoá học
Phản ứng hoá học:
CH2=CH–CH2–CH3 + H2 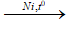
Điều kiện phản ứng
- Đun nóng, xúc tác niken (hoặc platin hoặc palađi).
Cách thực hiện phản ứng
- Đun nóng hỗn hợp but-1-en và H2 với xúc tác niken, but -1-en kết hợp với H2 thành butan (C4H10).
Hiện tượng nhận biết phản ứng
- Sản phẩm sinh ra không làm mất màu dung dịch brom.
Bạn có biết
- Phản ứng trên gọi là phản ứng cộng.
- Tỉ lệ phản ứng luôn là 1:1
- Khối lượng trước và sau phản ứng luôn bằng nhau
- Số mol sau phản ứng luôn giảm → Số mol H2 phản ứng = nđ - ns

Ví dụ minh họa
Ví dụ 1: Hỗn hợp khí X gồm H2 và một anken có khả năng cộng HBr cho 2 sản phẩm hữu cơ. Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của anken là
A. CH2=CH2.
B. CH2=CH-CH2-CH3.
C. CH3-CH=CH-CH3.
D. CH2=CH-CH3.
Hướng dẫn :

X cho 2 sản phẩm hữu cơ ⇒ X là CH2=CH-CH2-CH3.
Ví dụ 2: Cho chất X có công thức sau: CH2=CH-CH2-CH3. X có tên gọi theo danh pháp IUPAC là:
A. But – 1 – en
B. But – 2- en
C. Buten
D. 2 – metylbut-1-en
Đáp án B
Ví dụ 3: Cho H2 và 1 olefin có thể tích bằng nhau qua Niken đun nóng ta được hỗn hợp A. Biết tỉ khối hơi của A đối với H2 là 23,2. Hiệu suất phản ứng hiđro hoá là 75%. Công thức phân tử olefin là
A. C2H4.
B. C3H6.
C. C4H8.
D. C5H10.
Hướng dẫn
Gọi CT của olefin là CnH2n có số mol là x
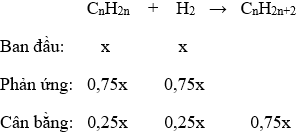
⇒ nA = 1,25x mol
⇒ mA = 2 × 23,2 × 1,25x = mhỗn hợp đầu = 14nx + 2x
⇒ n = 4 ⇒ Olefin là C4H8
Đáp án C

