Trắc nghiệm Hóa học 10 Chủ đề 1 (có đáp án): Cấu tạo nguyên tử - Cánh diều
Haylamdo biên soạn và sưu tầm 50 bài tập trắc nghiệm Hóa học 10 Chủ đề 1: Cấu tạo nguyên tử sách Cánh diều có đáp án và lời giải chi tiết đầy đủ các mức độ sẽ giúp học sinh ôn luyện trắc nghiệm để biết cách làm các dạng bài tập Hóa 10
Trắc nghiệm Hóa học 10 Chủ đề 1 (có đáp án): Cấu tạo nguyên tử - Cánh diều
Trắc nghiệm Hóa học 10 Bài 4: Mô hình nguyên tử và orbital nguyên tử
Trắc nghiệm Hóa học 10 Bài 5: Lớp, phân lớp và cấu hình electron
Câu 1:
Nguyên tử được tạo nên từ các hạt cơ bản là
A. proton, neutron và electron.
B. proton và neutron.
C. proton và electron.
D. neutron và electron.
Câu 2:
Trong một nguyên tử, số proton
A. bằng số neutron.
B. luôn lớn hơn số electron.
C. bằng số electron.
D. luôn gấp đôi số electron.
Câu 3:
Phát biểu nào sau đây là đúng?
A. Nguyên tử mang điện tích âm.
B. Nguyên tử mang điện tích dương.
C. Không xác định được điện tích của nguyên tử.
D. Nguyên tử trung hòa về điện.
Câu 4:
Trong nguyên tử, hạt nào không mang điện tích?
A. Proton.
B. Electron.
C. Neutron.
D. Neutron và proton.
Câu 5:
Nguyên tử nguyên tố carbon (C) có 6 proton. Số electron trong nguyên tử carbon là
A. 5.
B. 6.
C. 12.
D. 8.
Câu 6:
Hạt nhân nguyên tử được tạo nên bởi các hạt
A. proton và electron.
B. proton và neutron.
C. electron và neutron.
D. proton, neutron và electron.
Câu 7:
X là nguyên tố phổ biến nhất trong Mặt Trời, chiếm khoảng 74% khối lượng Mặt Trời. Biết một loại nguyên tử của nguyên tố X chỉ tạo nên bởi proton và electron (không có neutron). Nguyên tố X là
A. Lithium.
B. Carbon.
C. Helium.
D. Hydrogen.
Câu 8:
Một cách gần đúng, có thể coi khối lượng nguyên tử bằng khối lượng của
A. hạt nhân.
B. hạt proton.
C. electron.
D. neutron.
Câu 9:
Phát biểu nào sau đây không đúng?
A. Kích thước của hạt nhân rất nhỏ so với kích thước của nguyên tử.
B. Nguyên tử của các nguyên tố khác nhau có khối lượng khác nhau nhưng kích thước giống nhau.
C. Phần không gian rỗng chiếm chủ yếu trong nguyên tử
D. Kích thước hạt nhân bằng khoảng 10-5 đến 10-4 lần kích thước nguyên tử.
Câu 10:
Biết một hạt proton có khối lượng gần đúng là 1 amu. Hãy cho biết bao nhiêu hạt proton thì có tổng khối lượng bằng 1 gam?
A. 1,6605×1023.
B. 6,022×1022.
C. 6,022×1023.
D. 1,6605×1024.
Câu 11:
Cho biết khối lượng của các hạt cấu tạo nên nguyên tử như sau:
Loại hạt | Electron (e) | Proton (p) | Neutron (n) |
Khối lượng (amu) | 0,00055 | 1 | 1 |
Nguyên tử lithium (Li) có 3p, 4n và 3e. Khối lượng lớp vỏ của Li bằng khoảng bao nhiêu phần trăm khối lượng của cả nguyên tử Li?
A. 0,2081%
B. 1,2334%.
C. 0,0812%.
D. 0,0236%.
Câu 12:
Nguyên tử nguyên tố Potassium (K) có 19 proton và 20 nơtron. Khối lượng gần đúng của nguyên tử K là (biết me = 0,00055 amu; mp = 1 amu; mn = 1 amu)
A. 29,01 amu.
B. 38,02 amu.
C. 39,01 amu.
D. 32,10 amu.
Câu 13:
Tính tổng số proton, neutron và electron trong một phân tử carbon dioxide (CO2). Biết trong phân tử này, nguyên tử C có 6 proton và 6 neutron; nguyên tử O có 8 proton và 8 neutron.
A. 42 hạt.
B. 66 hạt.
C. 60 hạt.
D. 55 hạt.
Câu 14:
Nguyên tử nguyên tố X có tổng số hạt cơ bản là 34 và 12 hạt neutron. Số electron trong nguyên tử X là
A. 12.
B. 11.
C. 13.
D. 22.
Câu 15:
Nguyên tử nguyên tố X có tổng số hạt cơ bản là 40. Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Số proton trong nguyên tử nguyên tố X là
A. 13.
B. 14.
C. 15.
D. 16.
Câu 1:
Các nguyên tử thuộc cùng về một nguyên tố hóa học khi
A. có cùng số hạt proton.
B. có cùng số hạt neutron.
C. có cùng số hạt electron và neutron.
D. có cùng khối lượng nguyên tử.
Câu 2:
Hạt nhân nguyên tử Lithium (Li) có 3 proton. Số hiệu nguyên tử của Li là
A. 4.
B. 3.
C. 2.
D. 1.
Câu 3:
Số khối (A) của một nguyên tử bằng
A. tổng số proton và số electron.
B. tổng số proton và neutron.
C. tổng số neutron và electron.
D. tổng số proton, neutron và electron.
Câu 4:
Nguyên tử Helium (He) có 2 proton và 2 neutron. Số khối của He là
A. 2.
B. 6.
C. 4.
D. 8.
Câu 5:
Nguyên tử nguyên tố X có số hiệu nguyên tử là 8. Phát biểu nào sau đây không đúng?
A. X là nguyên tố oxygen.
B. Nguyên tử X có 8 proton.
C. X là nguyên tố phổ biến nhất ở lớp vỏ Trái Đất.
D. Nguyên tử nguyên tố X có 16 neutron.
Câu 6:
Nguyên tử sodium (Na) có 11 proton trong hạt nhân. Khi Na tác dụng với khí chlorine (Cl2) sẽ thu được muối sodium chloride (NaCl), trong đó Na tồn tại ở dạng ion Na+. Ion Na+ có bao nhiêu proton trong hạt nhân?
A. 11.
B. 12.
C. 10.
D. 13.
Câu 7:
Từ kí hiệu nguyên tử \[{}_Z^AX\], ta không thể xác định được
A. kí hiệu hóa học của nguyên tố (X).
B. số khối.
C. kích thước của nguyên tử (X).
D. số hiệu nguyên tử.
Câu 8:
Nguyên tử aluminium (Al) có 13 proton và 14 neutron. Kí hiệu nguyên tử của nguyên tố này là
A. \[{}_{14}^{27}Al\].
B. \[{}_{27}^{13}Al\].
C. \[{}_{27}^{14}Al\].
D. \[{}_{13}^{27}Al\].
Câu 9:
Cho biết kí hiệu nguyên tử của nguyên tố fluorine là \[{}_9^{19}F\]. Số proton, neutron và electron trong nguyên tử fluorine lần lượt là
A. 9, 9, 10.
B. 9, 10, 9.
C. 10, 9, 9.
D. 9, 19, 9.
Câu 10:
Cho các nguyên tử sau: \[{}_8^{16}X\], \[{}_9^{19}Y\], \[{}_{11}^{23}Z\], \[{}_8^{17}M\], \[{}_8^{18}T\]. Những nguyên tử nào là đồng vị của nhau?
A. X, Y, Z.
B. Y, Z, M.
C. Y, M, T.
D. X, M, T.
Câu 11:
Nguyên tử khối là
A. khối lượng tuyệt đối của một nguyên tử.
B. khối lượng tương đối của một nguyên tử.
C. tổng số hạt proton, neutron và electron trong nguyên tử.
D. tổng số proton và electron trong nguyên tử.
Câu 12:
Trong tự nhiên, argon có các đồng vị là 40Ar chiếm khoảng 99,604% số nguyên tử; 38Ar chiếm khoảng 0,063% số nguyên tử và 36Ar. Nguyên tử khối trung bình của Ar là
A. 40,265.
B. 38,994.
C. 39,985.
D. 41, 226.
Câu 13:
Trong tự nhiên, bạc có hai đồng vị là 107Ag và 109Ag. Nguyên tử khối trung bình của bạc là 107,96. Phần trăm số nguyên tử của đồng vị là 107Ag là
A. 48%.
B. 52%.
C. 60%.
D. 40%.
Câu 14:
Chlorine có hai đồng vị bền trong tự nhiên, trong đó có một đồng vị là 35Cl chiếm 77,5% số nguyên tử. Biết nguyên tử khối trung bình của chlorine là 35,45. Đồng vị còn lại là
A. 37Cl.
B. 36Cl.
C. 38Cl.
D. 39Cl.
Câu 15:
Nguyên tử nguyên tố X phổ biến trong tự nhiên có tổng các hạt cơ bản là 46. Số khối của nguyên tử X là
A. 31.
B. 32.
C. 24.
D. 28.
Câu 1:
Mô hình nguyên tử theo Rutherford – Bohr không có nội dung nào sau đây?
A. Khối lượng nguyên tử tập trung chủ yếu ở hạt nhân.
B. Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
C. Electron mang điện tích âm nên bị hút vào hạt nhân.
D. Năng lượng của electron phụ thuộc vào khoảng cách từ electron đó tới hạt nhân nguyên tử. Electron ở càng xa hạt nhân thì có năng lượng càng cao.
Câu 2:
Theo mô hình nguyên tử Rutherford – Bohr, electron thuộc lớp nào sau đây có năng lượng thấp nhất?
A. Lớp N.
B. Lớp L.
C. Lớp M.
D. Lớp K.
Câu 3:
Phát biểu nào sau đây không đúng?
A. Các electron được phân bố vào lớp gần hạt nhân trước.
B. Số electron tối đa trong mỗi lớp là 2n (n là số thứ tự lớp electron, n ≤ 4).
C. Năng lượng của các electron ở lớp trong thấp hơn năng lượng electron ở lớp ngoài.
D. Sự liên kết giữa electron trên lớp K với hạt nhân là bền chặt nhất.
Câu 5:
Cho cấu trúc nguyên tử aluminium theo mô hình Rutherford – Bohr như sau:
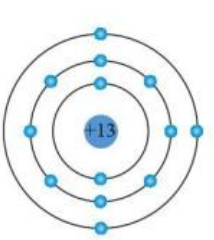
Lớp ngoài cùng của nguyên tử aluminium có bao nhiêu electron?
A. 2.
B. 3.
C. 5.
D. 8.
Câu 6:
Sự khác biệt cơ bản giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử là
A. Electron được phân bố vào các lớp (mô hình Rutherford – Bohr) và electron chuyển động tập trung tại một góc gần hạt nhân (mô hình hiện đại).
B. Electron chuyển động bị hút vào hạt nhân (mô hình Rutherford – Bohr) và electron chuyển động không thể bị hút vào hạt nhân (mô hình hiện đại).
C. Electron chuyển động rất nhanh (mô hình Rutherford – Bohr) và electron chuyển động rất chậm (mô hình hiện đại).
D. Electron chuyển động theo quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời (mô hình Rutherford – Bohr) và electron chuyển động không theo quỹ đạo cố định (mô hình hiện đại).
Câu 7:
Khu vực không gian xung quanh hạt nhân nguyên tử mà xác xuất tìm thấy electron ở khu vực đó là lớn nhất (khoảng 90%) gọi là
A. lớp vỏ electron.
B. orbital nguyên tử.
C. cấu hình nguyên tử.
D. trọng tâm nguyên tử.
Câu 8:
Phát biểu nào sau đây là đúng khi nói về hình dạng của orbital nguyên tử?
A. AO s hình số tám nổi; AO p hình cầu.
B. AO s hình vuông; AO p hình cầu.
C. AO s hình cầu; AO p hình số tám nổi.
D. AO s hình cầu; AO p hình vuông.
Câu 10:
Electron chuyển từ lớp gần hạt nhân ra lớp xa hạt nhân thì phải
A. giải phóng năng lượng.
B. vừa giải phóng năng lượng và vừa thu năng lượng.
C. thu năng lượng.
D. va chạm vào hạt nhân rồi bắn ra.
Câu 11:
Nguyên tử nguyên tố sodium có 11 electron. Nguyên tử này có
A. 1 lớp electron.
B. 2 lớp electron.
C. 3 lớp electron.
D. 4 lớp electron.
Câu 12:
Nguyên tử nguyên tố magnesium có 3 lớp electron, trong đó lớp ngoài cùng có 2 electron. Số proton trong nguyên tử magnesium là
A. 10.
B. 13.
C. 11.
D. 12.
Câu 13:
Nguyên tử nguyên tố X có 8 neutron và có số khối là 16. Lớp ngoài cùng của nguyên tử X có
A. 2 electron.
B. 3 electron.
C. 1 electron.
D. 6 electron.
Câu 14:
Cho mô hình nguyên tử của nguyên tố nitrogen (N) như sau:
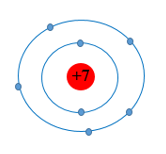
Số proton và số electron lớp ngoài cùng của nguyên tử N lần lượt là
A. 7 và 7.
B. 7 và 2.
C. 6 và 5.
D. 7 và 5.
Câu 15:
Nguyên tử nguyên tố Y có tổng số hạt cơ bản là 48, trong đó số hạt mang điện gấp đôi số hạt không mang điện. Nguyên tố Y là
A. sodium (Na).
B. calcium Ca).
C. boron (B).
D. magnesium (Mg).
Câu 1:
Electron càng xa hạt nhân thì có năng lượng
A. càng cao.
B. càng thấp.
C. không thay đổi.
D. gấp đôi năng lượng ban đầu.
Câu 2:
Các electron thuộc cùng một phân lớp có năng lượng
A. khác nhau.
B. bằng nhau.
C. tăng theo cấp số cộng.
D. tăng theo cấp số nhân.
Câu 3:
Số AO và số electron tối đa trong lớp electron thứ n (n ≤ 4) lần lượt là
A. n2; 2n.
B. n; 2n2.
C. n2; n2.
D. n2; 2n2.
Câu 4:
Lớp electron thứ 3 có bao nhiêu phân lớp và kí hiệu các phân lớp này là gì?
A. 1 phân lớp, kí hiệu là 1s.
B. 2 phân lớp, kí hiệu là 2s và 2p.
C. 3 phân lớp, kí hiệu là 3s, 3p và 3d.
D. 4 phân lớp, kí hiệu là 4s, 4p, 4d và 4f.
Câu 5:
Số lượng AO trong mỗi phân lớp s, p, d, f lần lượt là
A. 1, 3, 5, 6.
B. 1, 3, 5, 7.
C. 2, 4, 6, 8.
D. 2, 3, 4, 5.
Câu 6:
Số electron tối đa trên mỗi phân lớp ns, np, nd, nf lần lượt là
A. 1, 3, 5, 7.
B. 2, 4, 6, 8.
C. 2, 6, 10, 14.
D. 3, 7, 9, 15.
Câu 7:
Kí hiệu 1s2 cho biết
A. phân lớp 1s có 2 electron.
B. phân lớp 2s có 1 electron.
C. phân lớp 1s có 2 AO.
D. phân lớp 2s có 1 AO.
Câu 8:
Phân lớp được gọi là phân lớp bão hòa khi có
A. 2 electron.
B. 3 electron.
C. tối đa electron.
D. 5 electron.
Câu 10:
Lớp ngoài cùng của oxygen (Z = 8) có bao nhiêu electron, bao nhiêu AO?
A. 6 electron và 3 AO.
B. 4 electron và 3 AO.
C. 6 electron và 4 AO.
D. 4 electron và 4 AO.
Câu 11:
Nguyên tử Boron (B) có Z = 5. Cấu hình electron của B là
A. 1s22s22p2.
B. 1s22s22p1.
C. 1s22s23s1.
D. 1s22s12p13s1.
Câu 12:
Nguyên tử K có Z = 19. Cấu hình electron của K là
A. [Ar]4s1.
B. [Ar]3d1.
C. [Ar]4s2.
D. [Ar]3d2.
Câu 13:
Nguyên tử Iron (Fe) có Z = 26. Cấu hình electron của nguyên tử Fe là
A. [Ar]4s23d6.
B. [Ar]3d6.
C. [Ar]3d64s2.
D. [Ar]4s2.
Câu 14:
Nguyên tử sodium (Na) có Z = 11. Cấu hình electron của Na+ là
A. 1s22s22p6.
B. 1s22s22p63s1.
C. 1s22s22p63s2.
D. 1s22s22p5.
Câu 15:
Nguyên tử nitrogen (Z = 7) có
A. 2 electron độc thân.
B. 3 electron độc thân.
C. 4 electron độc thân.
D. 1 electron độc thân.

