Lý thuyết Hóa học 12 Bài 16: Điện phân - Kết nối tri thức
Haylamdo biên soạn tóm tắt lý thuyết Hóa 12 Bài 16: Điện phân sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh lớp 12 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 12.
Lý thuyết Hóa 12 Bài 16: Điện phân - Kết nối tri thức
I. HIỆN TƯỢNG ĐIỆN PHÂN
1. Khái niệm
- Điện phân là một quá trình oxi hoá - khử xảy ra tại các điện cực khi có dòng điện một chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
- Phản ứng oxi hoá - khử xảy ra trong quá trình điện phân là phản ứng không tự xảy ra mà phải nhờ tác động của điện năng để gây ra phản ứng đó.
- Các chất tham gia vào quá trình điện phân có thể ở trạng thái nóng chảy (điện phân nóng chảy) hoặc dung dịch (điện phân dung dịch). Trong quá trình điện phân, dưới tác dụng của điện trường, các ion âm sẽ di chuyển về điện cực dương, các ion dương sẽ di chuyển về điện cực âm.
- Khi điện phân dung dịch, nước cũng có thể tham gia điện phân với vai trò chất khử (2H2O → O2 + 4H+ + 4e) hoặc chất oxi hoá (2H2O + 2e → H2 + 2OH-).
- Theo quy ước chung, đối với cả pin điện và bình điện phân, tại cathode xảy ra quá trình khử và tại anode xảy ra quá trình oxi hoá. Do vậy, trong điện phân cathode là cực âm, anode là cực dương.
- Ví dụ: Sodium chloride (NaCl) nóng chảy điện li thành các ion Na+ và Cl− chuyển động tự do. Trong điện trường, các ion sẽ di chuyển về các cực trái dấu. Ở một hiệu điện thế đủ lớn, trên bề mặt các điện cực xảy ra các quá trình:
|
Cực âm (cathode) |
Quá trình khử ion Na+ |
Na+ + 1e → Na |
|
Cực dương (anode) |
Quá trình oxi hoá ion Cl− |
Phương trình hoá học của phản ứng điện phân NaCl nóng chảy:
2. Nguyên tắc (thứ tự) điện phân
- Khi bình điện phân chứa nhiều chất oxi hoá và chất khử, các quá trình xảy ra tại anode và cathode tuân theo thứ tự sau:
+ Tại anode, chất khử mạnh hơn sẽ bị oxi hóa trước.
+ Tại cathode, chất oxi hoá mạnh hơn sẽ bị khử trước.
Ví dụ: Điện phân dung dịch NaCl bão hoà với điện cực trơ, có màng ngăn. Trong dung dịch nước, NaCl điện li thành Na+ và Cl-.
NaCl(aq) → Na+(aq) + Cl-(aq)
|
Tại điện cực âm có ion Na+ và H2O. Vì H2O (bản chất là H+ của phân tử H2O) dễ nhận electron hơn Na+ nên ưu tiên xảy ra quá trình: 2H2O(l) + 2e → H2(g) + 2OH-(aq) |
Tại điện cực dương có Cl- và H2O. Trong điều kiện này, Cl- được ưu tiên điện phân trước theo quá trình: 2Cl-(aq) → Cl2(g) + 2e |
Phương trình hoá học của phản ứng điện phân:
2NaCl(aq) + 2H2O(l) → 2NaOH(aq) + Cl2(g) + H2(g)
Khi điện phân dung dịch NaCl với điện cực trơ và không có màng ngăn, trong quá trình điện phân, NaCl sinh ra ở cathode sẽ phản ứng với khí Cl2 sinh ra ở anode theo phương trình hoá học:
2NaOH(aq) + Cl2(aq) → NaOCl(aq) + NaCl(aq) + H2O(l)
Dung dịch sản phẩm thu được gọi là nước Javel.
- Ở điều kiện chuẩn, độ mạnh yếu của các chất oxi hóa và chất khử được so sánh dựa vào giá trị thế điện cực chuẩn hoặc vị trí cặp oxi hoá - khử trong dãy điện hoá.
Ví dụ:
+ Thứ tự điện phân tại anode:
(Các anion như coi như không bị điện phân).
Thứ tự điện phân tại cathode: Au3+ > Ag+ > Hg2+ > Cu2+ > H+ > H2O.
Chú ý: Thứ tự điện phân còn phụ thuộc vào bản chất của vật liệu làm điện cực và trạng thái bề mặt của điện cực, đặc biệt là các quá trình tạo ra sản phẩm ở thể khí.
II. ỨNG DỤNG CỦA PHƯƠNG PHÁP ĐIỆN PHÂN
1. Sản xuất kim loại
- Trong công nghiệp, một số kim loại trung bình và yếu được sản xuất bằng phương pháp điện phân dung dịch (đpdd).
- Các kim loại mạnh như Na, K, Mg, Ca, Al, ... được sản xuất bằng phương pháp điện phân nóng chảy (đpnc) hợp chất ion của chúng.
2. Tinh chế kim loại
- Từ nguồn kim loại thô (kim loại phế liệu hoặc sau quá trình nhiệt luyện, thuỷ luyện), các kim loại như Zn, Ni, Co, Cu, Ag, Au, ... được tinh chế bằng phương pháp điện phân.
- Quá trình tinh chế được thực hiện bằng cách điện phân dung dịch chất tan (muối hoặc phức chất) của kim loại đó với anode làm bằng kim loại thô tương ứng.
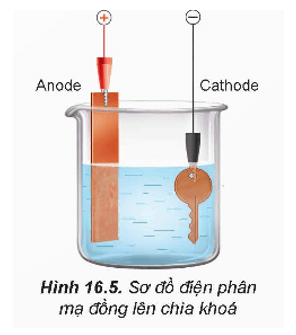
3. Mạ điện
- Phương pháp điện phân được sử dụng trong mạ điện, trong đó ion kim loại bị khử, tạo thành lớp kim loại rắn bao phủ trên bề mặt kim loại cần mạ nhằm trang trí bề mặt hoặc chống sự ăn mòn.
- Trong kĩ thuật mạ điện, các kim loại mạ thường là chromium, nickel, đồng, vàng, bạc, platinum, ...
- Bình mạ điện chứa dung dịch muối của kim loại mạ, vật cần mạ và thanh kim loại mạ.