Lý thuyết Hóa học 12 Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại - Kết nối tri thức
Haylamdo biên soạn tóm tắt lý thuyết Hóa 12 Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh lớp 12 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 12.
Lý thuyết Hóa 12 Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại - Kết nối tri thức
I - KIM LOẠI TRONG TỰ NHIÊN
- Trong tự nhiên, hầu hết các kim loại tồn tại ở dạng hợp chất (oxide, muối,...) trong quặng, chỉ một số kim loại kém hoạt động như vàng, bạc, platinum,... được tìm thấy dưới dạng đơn chất.
- Quặng là những loại đất, đá tồn tại trong tự nhiên có chứa khoáng vật của kim loại hoặc hợp chất kim loại với trữ lượng đủ lớn để có thể khai thác. Quặng thường chứa tạp chất. Phương pháp được sử dụng để tách một kim loại nhất định từ quặng của nó phụ thuộc vào tính chất của kim loại và của quặng.
- Một số loại quặng kim loại thông dụng:
|
Kim loại |
Quặng |
Thành phần chính |
|
Al |
Bauxite |
AI2O3.2H2O |
|
Zn |
Zinc blende |
ZnS |
|
Fe |
Hematite |
Fe2O3 |
|
Pyrite |
FeS2 |
|
|
Cu |
Chalcopyrite |
CuFeS2 |
II. CÁC PHƯONG PHÁP TÁCH KIM LOẠI
1. Nguyên tắc
Nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử:
Mn+ + ne ⟶ M
2. Tách kim loại hoạt động hoá học mạnh - Điện phân nóng chảy
Những kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al,... được điều chế bằng phương pháp điện phân nóng chảy các hợp chất của chúng (oxide, muối chloride).
a) Điện phân oxide nóng chảy
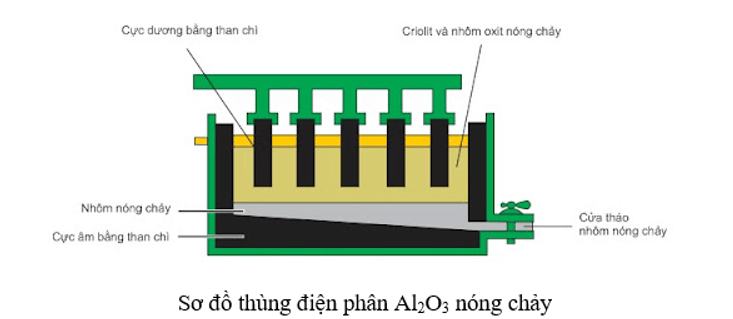
Ví dụ: Sản xuất Al bằng phương pháp điện phân
Các phản ứng xảy ra tại các điện cực khi điện phân Al2O3 nóng chảy trong quá trình sản xuất Al như sau:
Ở cực âm xảy ra sự khử ion Al3+:
Al3+ + 3e → Al
Ở cực dương xảy ra sự oxi hoá ion O2-:
Phương trình hoá học của phản ứng điện phân:
2Al2O3(l) → 4Al(l) + 3O2(g)
Trong thực tế Al2O3 nóng chảy ở nhiệt độ rất cao (2072oC). Bằng cách thêm cryolite (Na3AlF6), nhiệt độ nóng chảy của hỗn hợp còn khoảng 1000oC từ đó tiết kiệm được nhiều năng lượng cũng như giảm giá thành chế tạo bể điện phân.
b) Điện phân muối chloride nóng chảy
Để điều chế các kim loại như K, Na, Ca, Mg,... người ta điện phân muối chloride của chúng ở trạng thái nóng chảy.
Ví dụ: Tách magnesium bằng cách điện phân magnesium chloride nóng chảy với điện cực than chì (graphite) theo phương trình hoá học dưới đây:
2MgCl2(l) 2Mg(l) + Cl2(g)
Trong đó, tại anode và cathode xảy ra các quá trình sau:
Anode (+) : 2Cl− → Cl2 + 2e
Cathode (-): Mg2+ + 2e → Mg
3. Tách kim loại hoạt động trung bình, yếu
a) Phương pháp nhiệt luyện
- Nguyên tắc: Khử các oxide kim loại ở nhiệt độ cao bằng chất khử như C, CO,...
Những kim loại có độ hoạt động trung bình, yếu như Zn, Fe, Sn, Pb, Cu,... thường được điều chế bằng phương pháp nhiệt luyện.
Ví dụ: Tách kẽm từ quặng zinc blende.
Đốt quặng zinc blende:
2ZnS(s) + 3O2(g) 2ZnO(s) + 2SO2(g).
Khử zinc oxide ở nhiệt độ cao bằng than cốc:
ZnO(s) + C(s) Zn(g) + CO(g).
b) Phương pháp điện phân dung dịch
Kim loại hoạt động trung bình hoặc yếu có thể được điều chế bằng cách điện phân dung dịch muối của chúng.
Ví dụ: Điện phân dung dịch CuCl2 để điều chế Cu.
Phương trình hoá học của phản ứng điện phân:
CuCl2(aq) ⟶ Cu(s) + Cl2(g)
c) Phương pháp thuỷ luyện
Cơ sở của phương pháp này là dùng những dung dịch thích hợp như dung dịch H2SO4, NaOH, NaCN,... để hoà tan kim loại hoặc hợp chất của kim loại, tách phần không tan ra khỏi dung dịch. Sau đó khử những ion kim loại này trong dung dịch bằng kim loại có tính khử mạnh hơn như Fe, Zn,...
Ví dụ: Dùng Fe để khử ion Cu2+ trong dung dịch muối đồng.
Fe(s) + CuSO4(aq) ⟶ FeSO4(aq) + Cu(s)
III. TÁI CHẾ KIM LOẠI
- Tái chế kim loại là công việc cần thiết, vừa đảm bảo nguồn cung, vừa gia tăng giá trị kinh tế, bảo vệ môi trường và thực hiện mục tiêu phát triển bền vững.
- Quy trình tái chế kim loại thường gồm các giai đoạn: thu gom, phân loại; xử lí sơ bộ; phối trộn phế liệu; nấu chảy; tinh chế; đúc; chế tạo; gia công.
a) Tái chế nhôm
Nhôm là một trong những kim loại có thể được tái chế hiệu quả nhất, tiết kiệm năng lượng so với sản xuất từ quặng. Giống như hầu hết các kim loại, nhôm có thể được tái chế nhiều lần mà không mất đi các tính chất vốn có của nó. Nhôm tái chế được sử dụng trong các lĩnh vực như xây dựng, sản xuất ô tô, xe máy, xe đạp, thiết bị điện tử,... Hiện nay, khoảng 75% tổng lượng nhôm từng được sản xuất vẫn đang được sử dụng.
b) Tái chế đồng
Đồng cũng có thể được tái chế nhiều lần mà ít bị tiêu hao. Đồng tái chế được sử dụng trong nhiều lĩnh vực như làm vật liệu xây dựng, phương tiện giao thông, dụng cụ nấu ăn, nhạc cụ, dây dẫn điện,... Tái chế đồng giúp tiết kiệm một lượng lớn năng lượng so với sản xuất kim loại từ quặng. Ước tính khoảng 80% lượng đồng từng được khai thác từ Trái Đất vẫn đang được sử dụng cho đến ngày nay.
c) Tái chế sắt
Sắt là kim loại được tái chế nhiều nhất trên thế giới và có thể tái chế nhiều lần. Tái chế sắt giúp tiết kiệm năng lượng so với sản xuất sắt thép từ quặng sắt, giảm thiểu một số tác động tiêu cực tới môi trường của quá trình khai thác quặng. Phần lớn sắt tái chế được sử dụng để sản xuất thép, sắt thép tái chế được sử dụng trong các lĩnh vực xây dựng, sản xuất ô tô,...