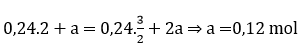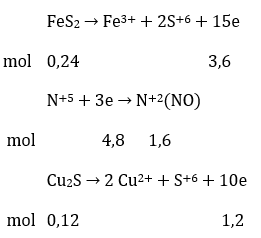Đề kiểm tra Hóa học 12 học kì 2 (có đáp án)
Đề kiểm tra Hóa học 12 học kì 2 (có đáp án)
Câu 1: Một este có công thức phân tử là C3H6O2 có phản ứng tráng bạc với dung dịch AgNO3 trong NH3. Công thức cáu tạo của este đó là:
A. HCOOC2H5 B. CH3COOCH3 C. HCOOC3H7 D. C2H5COOCH3
Câu 2: Etyl axetat được điều chế từ phản ứng giữa axit axetic và:
A. CH2=CH-OH B. CH2=CH2 C. C2H5OH D. C2H4(OH)2
Câu 3: Chất X có công thức phân tử là C8H8O2. Xà phong hoá X trong NaOH thu được dung dịch chứa 2 muối. số công thúc cấu tạo của X thoả mãn là:
A. 2 B. 4 C. 5 D. 3
Câu 4: Đun nóng 14,8 gam hỗn hợp X gồm (CH3COOCH3, HCOOC2H5, C2H5COOH) trong 100 ml dung dịch NaOH 1M và KOH 1M thì thu được 4,68 gam hỗn hợp 2 ancol (tỉ lệ mol 1:1) và m gam muối. Giá trị của m là:
A. 14,96 B. 18,28 C. 16,72 D. 19,72
Câu 5: Thành phần của dầu mau khô để pha sơn là triglixerit của các axit béo không no oleic và lioneic. Số triglixerit có thể thu được thừ hai axit béo đó với glixerol là:
A. 6 B. 3 C. 5 D. 4
Câu 6: Xà phòng hoá hoàn toàn 17,24 gam triglixerit cần vừa đủ 0,06 mol NaOH. Cô cạn dunh dịch sau phản ứng thu được khối lượng xà phòng là:
A. 17,8 gam B. 19,64 gam C. 14,84 gam D. 16,88 gam
Câu 7: Dãy gồm các dung dịch đều tác dụng với Cu(OH)2 là:
A. Glucozo, glixerol, saccarozo, etyl axetat
B. Glucozo, glixerol, saccarozo, ancol etylic
C. Glucozo, glixerol, saccarozo, axit axetic
D. Glucozo, glixerol, anđehit fomic, natri axetat
Câu 8: Cho các chất sau: amilozo, amilopectin. Saccarozo, xenlulozo, glucozo, fructozo. Số chất bị thuỷ phân khi đun nóng với dung dịch axit vô cơ là:
A. 6 B. 3 C. 5 D. 4
Câu 9: Thực hiện phản ứng thuỷ phân 16,2 gam xenlulozo trong môi trường axit, sau một thời gian phản ứng, đem trung hoà axit bằng kiềm, sau đó lấy hỗn hợp sau phản ứng cho tác dụng với AgNO3/NH3 thì thu được 16,2 gam Ag. Hiệu suất của phản ứng tuỷ phân là:
A. 50% B. 75% C. 66,67% D. 80%
Câu 10: Lên men 270 gam tinh bột thu được 92 gam ancol etylic. Hiệu suất của quá trình lên men tạo nên ancol etylic là:
A. 50% B. 70% C. 60% D. 80%
Câu 11: Cho các sơ đồ phản ứng sau:
Fe + O2 −to→ (A) (1) (C) + NaOH → (E) + (G) (4)
(A) + HCl → (B) + (C) + H2O (2) (D) + ? + ? → (E) (5)
(B) + NaOH → (D) + (G) (3) (E) −to→ (F) + ? (6)
Thứ tự các chất (A), (D), (F) lần lượt là
A. Fe2O3, Fe(OH)3, Fe2O3. B. Fe3O4, Fe(OH)3, Fe2O3.
C. Fe3O4, Fe(OH)2, Fe2O3. D. Fe2O3, Fe(OH)2, Fe2O3.
Câu 12: Sơ đồ phản ứng nào sau đây đúng (mỗi mũi tên biểu diễn một phản ứng) ?
A. FeS2 → Fe(NO3)2 →Fe(OH)2 →Fe(OH)3 → Fe2O3 → Fe.
B. FeS2 → FeO → FeSO4 → Fe(OH)2 →FeO → Fe.
C. FeS2 → Fe(NO3)2 → FeCl3→ Fe(OH)2 → Fe2O3→ Fe.
D. FeS2 → Fe(NO3)2 → Fe(NO3)3 → Fe(NO3)3 → Fe(OH)2 → Fe.
Câu 13: Hoà tạn hoàn toàn m gam Fe trong dung dịch HNO3 loãng dư, sau khi phàn ứng kết thúc thu được 0,448 lít khí NO duy nhất (đktc). Giá trị của m là
A. 11,2. B.0,56. C. 5,60. D. 1 12.
Câu 14: Cho a gam bột sắt tác dụng hết với dung dịch H2SO4 loãng dư, thu được 560 ml một chất khí (đktc). Nếu cho a gam bột sắt tác dụng hết với dung dịch CuSO4 dư thì thu được m gam một chất rắn. Giá trị m là
A. 1,4. B.2,8. C. 1,6. D. 3,2.
Câu 15: Nung một mẫu thép thường có khối lượng 10 gam trong O2 dư thu được 0,1568 lít khí CO2 (đktc). Thành phần phần trăm theo khối lượng của cacbon trong mẫu thép đó là
A. 0,82% B. 0,84%. C. 0,88%. D. 0,86%.
Câu 16: Cho 40,0 gam hỗn hợp X gồm Fe và Fe3O4 (tỉ lệ mol 3:1) vào dung dịch HNO3 loãng, nỏng thu dược khí NO và còn lại 2,8 gam Fe chưa tan. Thể tích khí NO thoát ra (đktc) là (biết NO là sản phẩm khứ duy nhất của HNO3)
A. 4,48 lít. B. 2,24 lit. C. 6,35 lít. D3,36 lít
Câu 17: Cho luồng khí CO dư đi qua ống sứ đựng m gam hỗn hợp FeO và Fe2O3 nung nóng. Sau một thời gian, khối lượng chất rắn còn lại trong ống sứ là 5,5 gam. Cho khí đi ra khỏi ống sứ hấp thụ vào nước vôi trong dư, thu được 5 gam kết tủa. Giá trị của m là:
A.6,30. B 6,50, C. 6.94 D.7,10.
Câu 18: Hoà tan hoàn toàn hỗn hợp gồm FeS2 0,24 mol và Cu2S vào dung dich HNO3 vừa đủ thu được dung địch X (chỉ chứa hai muối sunfat) và V lít đktc; khí NO duy nhất. Giá trị của V là
A, 34,048. B. 35,840. C. 31,360. D, 25,088.
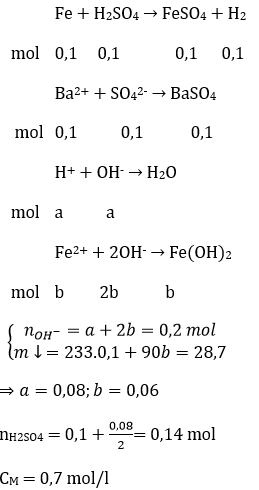
Câu 19: Hoà tan hoàn toàn m gam Fe trong 200 ml dung dịch H2SO4 loãng (dư), thu được dung dịch X và 2,24 lít khí H2 (đktc). Thêm 100 ml dung dịch Ba(OH)2 1M vào X, thu được 28,7 gam kết tủa. Nồng độ mol của dung dịch H2SO4 ban đầu là
A. 0,7M. B. 1,4M. C. 0,8M. D. 1,0M.
Câu 20: Cho m gam bột Fe vào dung dịch hỗn hợp chứa 0,16 mol Cu(NO3)2 và 0,4 mol HCl, lắc đều cho phản ứng xảy ra hoàn toàn, thu được hỗn hợp kim loại có khối lượng bằng 0,7m gam và V lít khí nâu đỏ duy nhất (đktc). Giá trị của m và V lần lượt là
A. 33,07 ; 4,48. B. 14,4 ; 4,48. C. 17,45 ; 3,36. D. 35,5 ; 5,6.
Câu 21: Dãy gồm các kim loại đều có thể tác dụng với nước tạo dung dịch kiềm là:
A. Na, K, Ca B. Na, Ca, Be
C. K, Ba, Al D. Ba, Ca, Mg
Câu 22: Hai kim loại đều không tan trong HNO3 đặc nguội là:
A. Al và Cu B. Fe và Ag
C. Cr và Fe D. Fe và Pb
Câu 23: Hoà tan 6,9 gam kim loại Na vào 200ml dung dịch HCl 1M thu được dung dịch X. Dung dịch X có thể hoà tan tối đa số gam Al là:
A. 2,7 gam B. 5,4 gam C. 8,1 gam D. 4,05 gam
Câu 24: Cho 11,2 lít hỗn hợp khí (đktc) gồm CO và H2 (tỉ lệ mol 1:1) qua m gam CuO nóng. Sau phản ứng hoàn toàn, khí và hơi thoát ra có tỉ khối hơi so với H2 là 10,7. Vậy giá trị của m tương ứng là:
A. 24,0 B. 20,0 C. 16,0 D. 12,8
Câu 25: Điện phân dung dịch X chứa hỗn hợp các muối sau: NaCl, CuCl2, FeCl3, ZnCl2. Kim loại cuối cùng thoát ra ở catot trước khi có khí thoát ra là:
A. Al, Fe, Cu B. Fe, Cu, Ag
C. Al, Cu, Ag D. Al, Fe, Al
Câu 26: Cho hỗn hợp Al và Fe vào dung dịch chứa AgNO3 và Cu(NO3)2 được dung dịch X và chất rắn Y gồm 3 lim loại. Vậy chất rắn Y gồm:
A. Al,Fe, Cu B. Fe, Cu, Ag
C. Al, Cu, Ag D. Al, Fe. Ag
Câu 27: Hoà tan 3,23 gam hỗn hợp gồm CuCl2 và Cu(NO3)2 vào nước được dung dịch X. Nhúng thanh kim loại Mg vào dung dịch X đến khi dung dịch mất màu xanh rồi lấy thanh Mg ra, cân lại thấy tăng thêm 0,8 gam. Khối lượng muối tạo ra trong dung dịch là:
A. 1,15 gam B. 1,43 gam C. 2,43 gam D. 4,13 gam
Câu 28: Điện phân điện cực trơ dung dịch muối clorua của một kim loại với cường độ dòng điện là 3,0A. Sau 1930 giây thấy khối lượng catot tăng 1,92 gam. Kim loại trong muối đã dùng là:
A. Cu B. Zn C. Ag D. Fe
Câu 29: Để điều chế Na2CO3 có thể dùng pương pháp nào sau đây?
A. Cho dung dịch K2CO3 tác dụng với dung dịch Na2SO4
B. Nhiệt phân NaHCO3
C. Cho khí CO2 dư đi qua dung dịch NaOH
D. Cho CaCO3 tác dụng với dung dịch NaCl
Câu 30: Cho sơ đồ phản ứng sau: NaCl→X→NaHCO3→Y→NaNO3
X và Y có thể là:
A. NaOH và NaClO B. Na2CO3 và NaClO
C. NaClO3 và Na2CO3 D. NaOH và Na2CO3
Câu 31: Ứng dụng nào sau đây không phải của Ca(OH)2?
A. Dùng làm vữa xây nhà
B. Khử chua đất trồng trọt
C. Bó bột khi bị gãy xương
D. Điều chế clorua vôi là chất tẩy trắng và khử trùng
Câu 32: Nung 13,5 gam hỗn hợp hai muối cacbonat của hai kim loại hoá trị 2, thu được 6,9 gam chất rắn và khí X. Lượng khí X sinh ra cho hấp thụ vào 75 ml dung dịch NaOH 1M. Khối lượng muối thu được sau phản ứng là:
A. 5,8 gam B. 6,5 gam C. 4,2 gam D. 6,3 gam
Câu 33: Để thu được Al2O3 từ hốn hợp Al2O3 và Fe2O3, người ta lần lượt dùng:
A. H2 ở nhiệt độ cao, dung dịch NaOH dư
B. Khí CO ở nhiệt độ cao, dung dịch HCl dư
C. Dung dịch NaOH dư, dung dịch HCl dư, nung nóng
D. Dung dịch NaOH dư, CO2 dư, nung nóng
Câu 34: Cho 26,8gam hỗn hợp X gồm: Al và Fe2O3, tiến hành ohanr ứng nhiệt nhôm cho tới khi hoàn toàn (giả sử chỉ xảy ra phản ứng khử Fe2O3 thành Fe). Hỗn hợp sản phẩm sau phản ứng cho tác dụng với lượng dư dung dịch HCl được 11,2 lít H2 (dktc). Khối lượng của Al trong X là:
A. 5,4 gam B. 7,02 gam C. 9,72 gam D. 10,8 gam
Câu 35: Dung dịch muối FeCl3 không tác dụng với kim loại nào dưới đây?
A. Fe B. Ag C. Zn D. Cu
Câu 36: Cho a mol hỗn hợp Fe, Cu tác dụng hết với a mol khí clo, sau phản ứng hoàn toàn thu được chất rắn X. Cho X vào nước thu được dung dịch Y. Thành phần chất tan có trong dung dịch Y là:
A. CuCl2, FeCl2 và FeCl3 B. FeCl2 và FeCl3
C. CuCl2 và FeCl3 D. CuCl2 và FeCl2
Câu 37: Cho 20 gam bột Fe vào dung dịch HNO3, khuấy đến khi phản ứng xong thu được V lít khí NO (đktc) và còn 3,2 gam kim loại. giá trị của V là:
A. 2,24 B. 4,48 C. 6,72 D. 5,6
Câu 38: Để m gam bột sắt ngoài không khí, sau một thời gian thu được 1,2m gam hỗn hợp chất rắn X. Hoà tan hoàn toàn hỗn hợp X trong dung dịch H2SO4 đặc, nóng thu được 1,972 lít SO2 (đktc). Giá trị của m là:
A. 5,6 B. 4,2 C. 7,0 D. 8,4
Câu 39: Cho các sơ đồ phản ứng:
Cr + Cl2 → X
X + NaOH(dư) → Y + NaCl + H2O
Y + Cl2 + NaOH → Z + NaCl + H2O
Z là:
A. NaCrO2 B. Cr(OH)2 C. Cr(OH)3 D. Na2CrO4
Câu 40: Nung hỗn hợp bột gồm 22,8 gam Cr2O3 và 10,8 gam Al ở nhiệt độ cao thu được hỗn hợp chất rắn X. Cho toàn bộ hỗn hợp X thu được phản ứng với dung dịch NaOH 1M (dư) thoát ra 5,376 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là:
A. 53,33% B. 80.00% C. 66,67% D. 90.00%