Lý thuyết Hóa học 11 Kết nối tri thức Bài 22: Ôn tập chương 5
Haylamdo biên soạn và sưu tầm với tóm tắt lý thuyết Hóa 11 Bài 22: Ôn tập chương 5 sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa 11 Kết nối tri thức Bài 22: Ôn tập chương 5
HỆ THỐNG HOÁ KIẾN THỨC
I. Tính chất hoá học của dẫn xuất halogen
Liên kết C−X phân cực về phía nguyên tử halogen nên phản ứng đặc trưng của dẫn xuất halogen là phản ứng thế nguyên tử halogen. Ngoài ra, dẫn xuất halogen còn tham gia phản ứng tách HX.
1. Phản ứng thế nguyên tử halogen
Các dẫn xuất halogen có thể tham gia phản ứng với dung dịch kiềm, nguyên tử halogen bị thay thế bởi nhóm OH−, tạo thành alcohol.
Phương trình hóa học chung:
R – X + NaOH R – OH + NaX
(X: Cl, Br, I; X liên kết với nguyên tử carbon no).
2. Phản ứng tách hydrogen halide
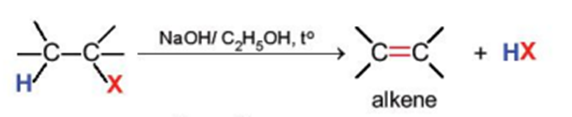
Các dẫn xuất monohalogen của alkane có thể bị tách hydrogen halide để tạo thành alkene theo sơ đồ sau:
Phản ứng này xảy ra khi đun nóng dẫn xuất halogen với base mạnh như NaOH, RONa trong dung môi alcohol.
Chú ý:
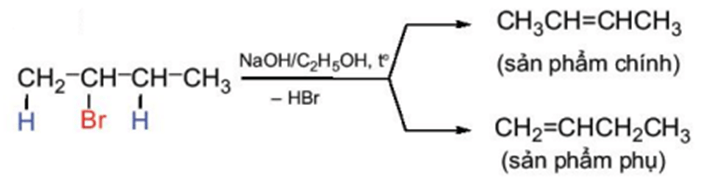
Phản ứng tách xảy ra theo quy tắc tách Zaitsev: Trong phản ứng tách hydrogen halide, nguyên tử halogen bị tách ưu tiên cùng với nguyên tử hydrogen ở carbon bên cạnh có bậc cao hơn.
Ví dụ:
II. Tính chất hoá học của ancol
1. Phản ứng thế nguyên tử H của nhóm – OH.
Liên kết O – H phân cực nên trong một số phản ứng, nguyên tử hydrogen trong nhóm hydroxy có thể bị thay thế.
Alcohol phản ứng với các kim loại mạnh như sodium, potassium giải phóng khí hydrogen:
2R – OH + 2Na → 2RONa + H2
2. Phản ứng tạo ether
Khi đun nóng alcohol với H2SO4 đặc ở nhiệt độ thích hợp thì thu được ether.
Ví dụ:
2C2H5OH C2H5OC2H5 + H2O
⇒ Công thức tính số ether tạo thành từ n alcohol khác nhau là .
3. Phản ứng tạo alkene
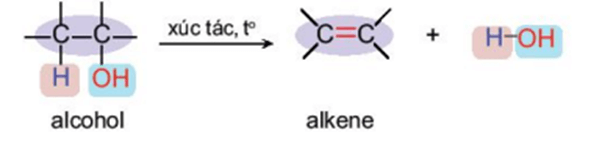
Khi cho hơi alcohol no, đơn chức, mạch hở đi qua bột Al2O3 nung nóng hoặc đun alcohol với H2SO4 đặc, H3PO4 đặc, alcohol bị tách nước tạo thành alkene:
Chú ý:
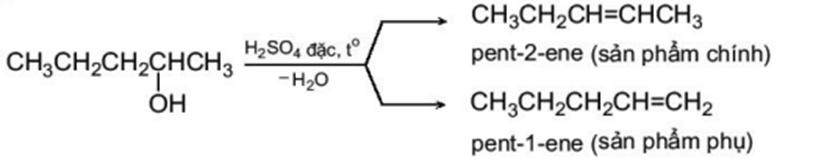
Phản ứng tách nước của alcohol tạo alkene ưu tiên theo quy tắc tách Zaitsev: Trong phản ứng tách nước của alcohol, nhóm – OH bị tách ưu tiên cùng với nguyên tử hydrogen ở carbon bên cạnh có bậc cao hơn.
Ví dụ:
4. Phản ứng oxi hoá
a) Oxi hoá không hoàn toàn
+ Các alcohol bậc I bị oxi hóa không hoàn toàn tạo thành aldehyde.
Tổng quát:
R – CH2 – OH + CuO R – CHO + Cu + H2O
+ Các alcohol bậc II bị oxi hóa không hoàn toàn tạo thành ketone.
Tổng quát:
R – CH(OH) – R’ + CuO R – CO – R’ + Cu + H2O
+ Trong điều kiện trên, alcohol bậc III không phản ứng.
b) Phản ứng cháy của alcohol
Các alcohol có thể bị đốt cháy trong không khí tạo thành carbon dioxide, hơi nước và toả nhiệt:
CnH2n + 2O + O2 nCO2 + (n + 1)H2O
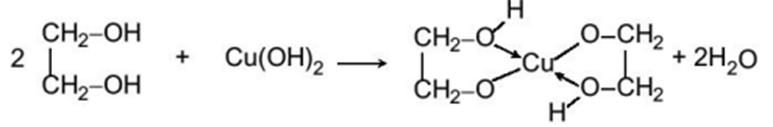
5. Phản ứng riêng của polyalcohol với Cu(OH)2
Các polyalcohol có các nhóm – OH liền kề như ethylene glycol, glycerol có thể tác dụng với copper(II) hydroxide tạo thành dung dịch màu xanh lam đậm.
Ví dụ:
Vì vậy, phản ứng này có thể dùng để nhận biết các polyalcohol có các nhóm – OH liền kề.
III. Tính chất hoá học của phenol
1. Phản ứng thế nguyên tử H của nhóm – OH (tính acid của phenol)
Trong dung dịch nước, phenol phân li theo cân bằng sau:
Phenol là một acid yếu, dung dịch phenol không làm đổi màu quỳ tím.
Phenol có thể phản ứng được với kim loại kiềm, dung dịch base, muối sodium carbonate …
2. Phản ứng thế ở vòng thơm
Phenol có thể tham gia phản ứng thế nguyên tử hydrogen của vòng benzene. Phản ứng thế ưu tiên vào vị trí 2, 4 và 6 (ortho và para).
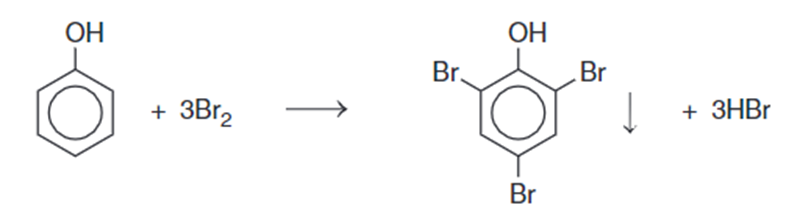
a) Phản ứng bromine hoá
Phenol phản ứng với nước bromine tạo sản phẩm thế 2,4,6 – tribromophenol ở dạng kết tủa màu trắng:
Do ảnh hưởng của nhóm – OH, phản ứng thế nguyên tử hydrogen ở vòng benzene của phenol xảy ra dễ dàng hơn so với benzene.
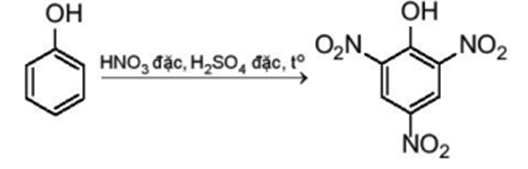
b) Phản ứng nitro hoá
Phenol phản ứng với dung dịch nitric acid đặc trong dung dịch sulfuric acid đặc tạo thành sản phẩm 2,4,6 – trinitrophenol (picric acid):