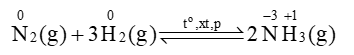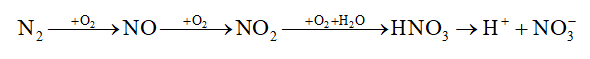Lý thuyết Hóa học 11 Kết nối tri thức Bài 4: Nitrogen
Haylamdo biên soạn và sưu tầm với tóm tắt lý thuyết Hóa 11 Bài 4: Nitrogen sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa 11 Kết nối tri thức Bài 4: Nitrogen
I. Trạng thái tự nhiên
Nguyên tố nitrogen tồn tại trong tự nhiên với 2 đồng vị bền là 14N (99,63%) và 15N (0,37%).
+ Trong khí quyển Trái Đất, nitrogen là nguyên tố phổ biến nhất, chiếm 75,5% khối lượng (hoặc 78,1% thể tích) và tập trung chủ yếu ở tầng đối lưu.
+ Trong vỏ Trái Đất, nguyên tố nitrogen tồn tại tập trung ở một số mỏ khoáng dưới dạng sodium nitrate (thường gọi là diêm tiêu Chile).
+ Nguyên tố nitrogen có trong tất cả cơ thể người, động vật và thực vật, là thành phần cấu tạo nên nucleic acid, protein, … Trong cơ thể người, nitrogen chiếm khoảng 3% khối lượng, đứng thứ tư sau oxygen, carbon và hydrogen.
II. Cấu tạo nguyên tử, phân tử
1. Cấu tạo nguyên tử
- Nguyên tố nitrogen ở ô số 7, nhóm VA, chu kì 2 trong bảng tuần hoàn. Nguyên tử nitrogen có độ âm điện lớn (3,04). Nitrogen là phi kim điển hình.
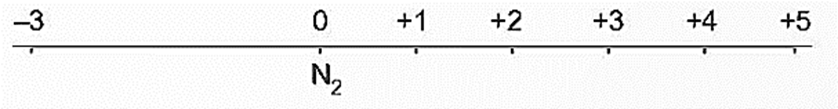
- Nitrogen tạo ra nhiều hợp chất với các số oxi hoá khác nhau từ ̶ 3 đến +5. Các số oxi hoá thường gặp của nitrogen được biểu diễn ở trục số oxi hoá dưới đây:
2. Cấu tạo phân tử
Phân tử nitrogen gồm 2 nguyên tử, liên kết với nhau bằng liên kết ba (1 liên kết σ và 2 liên kết π). Phân tử nitrogen có năng lượng liên kết lớn (945 kJ/mol) và không có cực.
III. Tính chất vật lí
Ở điều kiện thường, nitrogen là chất khí, không màu, không mùi, không vị, khó hoá lỏng (hoá lỏng ở -196 oC), tan rất ít trong nước (1 lít nước hoà tan được 0,012 lít khí nitrogen). Khí nitrogen không duy trì sự cháy và sự hô hấp.
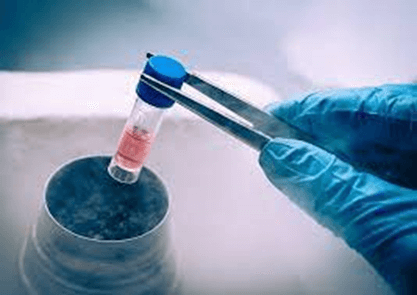
Lưu trữ tế bào gốc trong nitrogen lỏng
IV. Tính chất hoá học
Ở nhiệt độ thường, nitrogen khá trơ; ở nhiệt độ cao, nitrogen trở lên hoạt động hơn. Nitrogen thể hiện cả tính oxi hoá và tính khử.
1. Tác dụng với hydrogen
Trong phản ứng này, nitrogen thể hiện tính oxi hoá.
Đây là quá trình quan trọng nhất để sản xuất ammonia, thường gọi là quá trình Haber – Bosch, quá trình này được thực hiện ở quy mô công nghiệp từ năm 1913.
Phản ứng tổng hợp ammonia là quá trình trung gian quan trọng để sản xuất nitric acid, thuốc nổ, đạm nitrate, urea, ammophos,…
2. Tác dụng với oxygen
- Ở nhiệt độ cao trên 3000oC hoặc có tia lửa điện, nitrogen kết hợp với oxygen, tạo ra nitrogen monoxide (NO) với hiệu suất rất thấp.
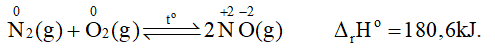
- Trong tự nhiên, phản ứng này xảy ra trong những cơn mưa giông kèm sấm sét, khởi đầu cho quá trình chuyển hoá từ nitrogen thành nitric acid. Nitric acid tan trong nước mưa và phân li ra ion nitrate là một dạng phân đạm mà cây trồng hấp thụ được để sinh trưởng, phát triển.
Quá trình tạo và cung cấp đạm nitrate cho đất từ nước mưa được biểu diễn theo sơ đồ:
- Trong thực tế, phản ứng hoá hợp giữa nitrogen với oxygen thường xảy ra đồng thời với quá trình đốt cháy nhiên liệu ở nhiệt độ cao bằng không khí. Các hoạt động giao thông vận tải và sản xuất công nghiệp là nguyên nhân chính gây phát thải các oxide của nitrogen vào khí quyển.
V. Ứng dụng
Một số ứng dụng của nitrogen được thể hiện trong sơ đồ sau: