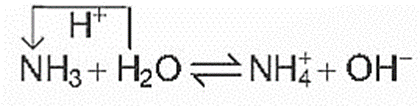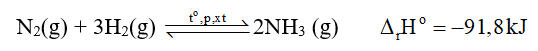Lý thuyết Hóa học 11 Kết nối tri thức Bài 5: Ammonia. Muối ammonium
Haylamdo biên soạn và sưu tầm với tóm tắt lý thuyết Hóa 11 Bài 5: Ammonia. Muối ammonium sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa 11 Kết nối tri thức Bài 5: Ammonia. Muối ammonium
I. Ammonia (NH3)
1. Cấu tạo phân tử
- Phân tử ammonia được tạo bởi một nguyên tử nitrogen liên kết với ba nguyên tử hydrogen và có dạng hình học là chóp tam giác.
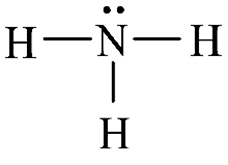 |
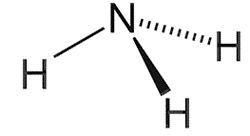 |
Công thức Lewis và dạng hình học của NH3 | |
- Đặc điểm cấu tạo của phân tử ammonia:
+ Nguyên tử nitrogen còn một cặp electron không liên kết, tạo ra vùng có mật độ điện tích âm trên nguyên tử nitrogen.
+ Liên kết N–H phân cực, cặp electron dùng chung lệch về nguyên tử nitrogen làm cho nguyên tử hydrogen mang một phần điện tích dương.
+ Liên kết N–H tương đối bền với năng lượng liên kết là 386 kJ/mol.
2. Tính chất vật lí
- Ammonia tồn tại ở cả trong môi trường đất, nước, không khí. Trong cơ thể người, ammonia được tạo ra trong quá trình chuyển hoá thức ăn chứa protein.
- Ở điều kiện thường, ammonia tồn tại ở thể khí, không màu, nhẹ hơn không khí, mùi khai và xốc. Ammonia tan nhiều trong nước. Ở điều kiện thường, 1 lít nước hoà tan được khoảng 700 lít khí ammonia. Ammonia dễ hoá lỏng (hoá lỏng ở –33,3 °C) và dễ hoá rắn (hoá rắn ở –77,7 °C).
3. Tính chất hoá học
a) Tính base
- Trong dung dịch, một phần số phân tử ammonia nhận proton của nước, tạo thành ion ammonium ().
- Dung dịch ammonia có môi trường base yếu, làm quỳ tím chuyển sang màu xanh, phenolphthalein chuyển sang màu hồng.
- Ở thể khí, ammonia cũng có khả năng nhận proton, thể hiện tính chất của một base Bronsted – Lowry.
Ví dụ: NH3(g) + HCl(g) → NH4Cl(s).
b. Tính khử
- Trong phân tử ammonia, nguyên tử nitrogen có số oxi hoá –3 (số oxi hoá thấp nhất của nitrogen) nên ammonia thể hiện tính khử.
- Khi đốt cháy trong oxygen, ammonia cháy với ngọn lửa màu vàng.
4NH3 + 3O2 2N2 + 6H2O
- Trong công nghiệp, phản ứng giữa ammonia và oxygen được thực hiện ở nhiệt độ 800 °C – 900 °C với xúc tác Pt.
4NH3 + 5O2 4NO + 6H2O
Phản ứng trên là giai đoạn trung gian quan trọng trong quá trình sản xuất nitric acid theo phương pháp Ostwald.
4. Ứng dụng
Một số ứng dụng của ammonia được thể hiện trong sơ đồ sau:
5. Sản xuất
Trong công nghiệp, quá trình sản xuất ammonia thường được thực hiện ở nhiệt độ 400 oC – 450 oC, áp suất 150 – 200 bar, xúc tác Fe.
II. Muối ammonium
1. Tính tan, sự điện li
Một số muối ammonium phổ biến: NH4Cl, NH4ClO4, NH4NO3, (NH4)2SO4, NH4H2PO4, (NH4)2HPO4, NH4HCO3, (NH4)2Cr2O7.
Hầu hết các muối ammonia đều tan trong nước và phân li hoàn toàn ra ion.
Ví dụ:
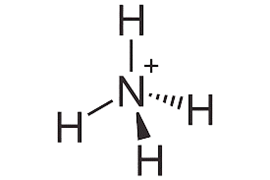
Chú ý: Dạng hình học của ion ammonium:
2. Tác dụng với kiềm – Nhận biết ion ammonium
Khi đun nóng hỗn hợp muối ammonium với dung dịch kiềm, sinh ra khí ammonia có mùi khai.
Ví dụ:
(NH4)2SO4 + 2NaOH Na2SO4 + 2NH3 + 2H2O
Phương trình ion rút gọn:
3. Tính chất
Các muối ammonium đều kém bền nhiệt và dễ bị phân huỷ khi đun nóng.
Ví dụ:
NH4Cl NH3 + HCl
NH4HCO3 NH3 + CO2 + H2O
NH4NO3 N2O + 2H2O
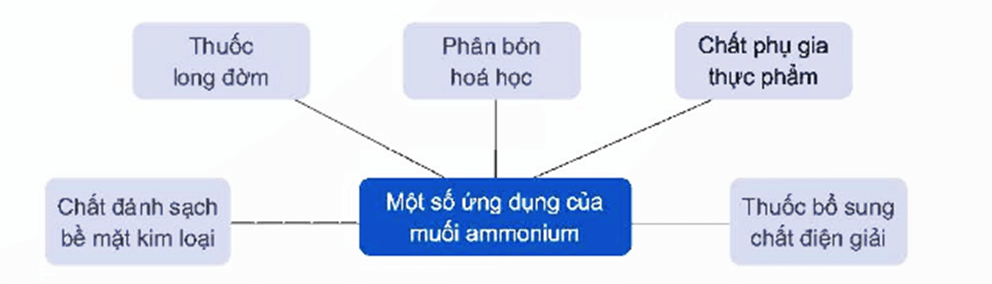
4. Ứng dụng
Một số ứng dụng của muối ammonium được thể hiện ở sơ đồ sau: