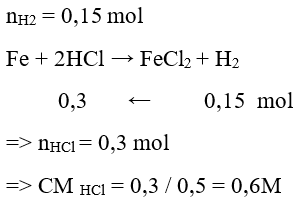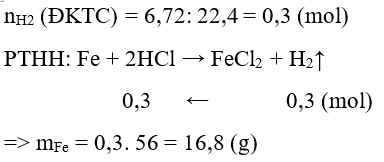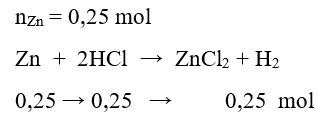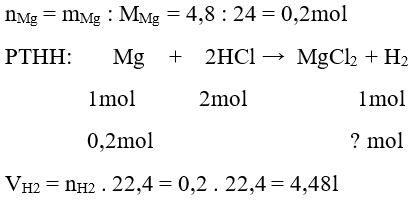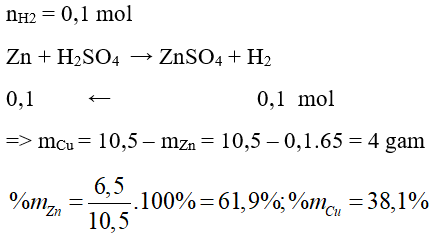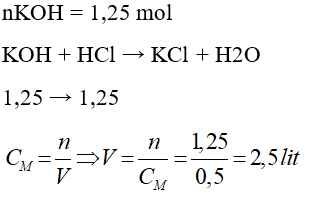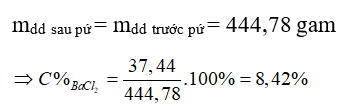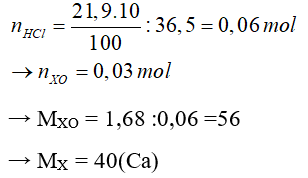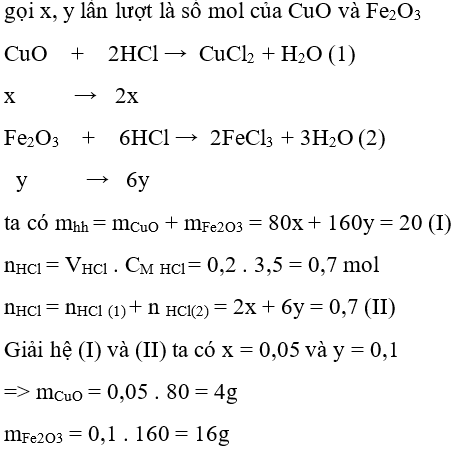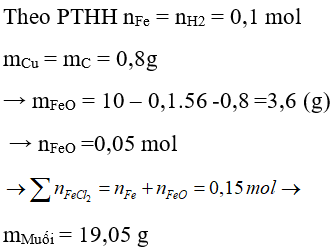Trắc nghiệm Hóa học 9 Bài 4 (có đáp án): Một số axit quan trọng (phần 2)
Trắc nghiệm Hóa học 9 Bài 4 (có đáp án): Một số axit quan trọng (phần 2)
Haylamdo biên soạn và sưu tầm câu hỏi trắc nghiệm Hóa học 9 Bài 4 (có đáp án): Một số axit quan trọng (phần 2) hay, chọn lọc sẽ giúp học sinh hệ thống lại kiến thức bài học và ôn luyện để đạt điểm cao trong bài thi môn Hóa học 9.

Câu 1: Tính chất hóa học nào không phải của axit?
A. Tác dụng với kim loại.
B. Tác dụng với muối.
C. Tác dụng với oxit axit.
D. Tác dụng với oxit bazơ.
Câu 2: Chất nào sau đây tác dụng với Fe ở nhiệt độ thường tạo ra khí hiđro là
A. O2.
B. HCl.
C. CO2.
D. H2O.
Câu 3: Hãy cho biết muối nào có thể điều chế bằng phản ứng của kim loại với dung dịch Axit H2SO4 loãng ?
A. ZnSO4
B. Na2SO3
C. CuSO4
D. MgSO3
Câu 4: Hiện tượng quan sát được khi cho mẩu magie vào ống nghiệm chứa axit HCl dư là:
A. Mẩu Mg tan dần, không có bọt khí thoát ra
B. Mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được không màu
C. Mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được có màu xanh lam
D. Không xảy ra hiện tượng gì
Câu 5: Các kim loại nào sau đây tác dụng được với dung dịch H2SO4 loãng?
A. Mg, Zn, Ag, Cu.
B. Mg, Zn, Fe, Cu.
C. Zn, Fe, Al, Mg.
D. Al, Cu, Fe, Ag.
Câu 6: Axit H2SO4 loãng không tác dụng với kim loại nào sau đây:
A. Al
B. Fe
C. Mg
D. Ag
Câu 7: Kim loại nào sau đây không tác dụng được với dung dịch axit H2SO4 loãng?
A. Fe
B. Al
C. Cu
D. Na
Câu 8: Dãy gồm các oxit tác dụng được với nước tạo thành dung dịch axit là:
A. CO, CO2, SO2
B. P2O5, NO, SO2
C. P2O5, SO2, CO2
D. NO, SO2, CO
Câu 9: Chất nào sau đây tác dụng với axit HCl tạo kết tủa trắng?
A. Ba(OH)2.
B. Ca(NO3)2.
C. AgNO3.
D. MgSO4.
Câu 10: Nhóm chất tác dụng với dung dịch H2SO4 loãng sinh ra chất kết tủa màu trắng:
A. ZnO, BaCl2
B. CuO, BaCl2
C. BaCl2, Ba(NO3)2
D. Ba(OH)2, ZnO
Câu 11: Dãy các chất có thể tác dụng với dung dịch HCl là:
A. Na, FeO, CuO
B. FeO, CuO, CO2
C. Fe, FeO, CO2
D. Na, FeO, CO2
Câu 12: Dung dịch A tác dụng với CuO tạo ra dung dịch có màu xanh lam. A là
A. NaOH.
B. Na2CO3.
C. H2SO4.
D. Ca(OH)2.
Câu 13: Cặp chất tác dụng với nhau tạo thành sản phẩm có chất khí:
A. Bari oxit và axit sunfuric loãng
B. Bari hiđroxit và axit sunfuric loãng
C. Bari cacbonat và axit sunfuric loãng
D. Bari clorua và axit sunfuric loãng
Câu 14: Nhóm oxit vừa tác dụng với nước, vừa tác dụng với dung dịch HCl là
A. Na2O, SO3, CO2.
B. K2O, P2O5, CaO.
C. BaO, Al2O3, Na2O.
D. CaO, BaO, K2O.
Câu 15: Axit HCl tác dụng được với oxit nào trong các oxit sau: Na2O; BaO; CuO; MgO; SO2; P2O5
A. Na2O; BaO; CuO; P2O5
B. BaO; CuO; MgO; SO2
C. Na2O; BaO; CuO; MgO
D. Na2O; BaO; MgO ;P2O5
Câu 16: Dãy các chất tác dụng được với dung dịch H2SO4 loãng tạo thành sản phẩm có chất khí là
A. Na2SO3, CaCO3, Zn.
B. Al, MgO, KOH.
C. BaO, Fe, CaCO3.
D. Zn, Fe2O3, Na2SO3.
Câu 17: Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là:
A. Mg
B. CaCO3
C. Cu
D. Na2SO3.
Câu 18: Cho một khối lượng mạt sắt dư vào 500 ml dd HCl, sau phản ứng thu được 3,36 lít khí (đktc). Nồng độ mol của dung dịch HCl đã dùng là
A. 0,5M.
B. 0,6M.
C. 0,15M.
D. 0,3M.
Câu 19: Cho a gam sắt vào dung dịch HCl dư. Sau phản ứng thu được 6,72 lít khí hidro ở đktc.Giá trị của a là
A. 5,6 gam.
B. 11,2 gam.
C. 16,8 gam.
D. 22,4 gam.
Câu 20: Hòa tan hoàn toàn 5,6 gam Fe cần dùng V(ml) dung dịch HCl 2M. Giá trị của V cần tìm là:
A. 0,1.
B. 100.
C. 50.
D. 300.
Câu 21: Cho 16,25 gam kẽm vào 300 gam dung dịch HCl lấy dư, phản ứng hoàn toàn thu được dung dịch A và khí H2. Khối lượng dung dịch A là
A. 316,25 gam.
B. 300,00 gam.
C. 312,35 gam.
D. 315,75 gam.
Câu 22: Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit clohidric. Thể tích khí Hiđro thu được ở đktc là:
A. 44,8 lít
B. 4,48 lít
C. 2,24 lít
D. 22,4 lít
Câu 23: Cho 10,5 gam hỗn hợp hai kim loại Zn và Cu vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là
A. 63% và 37%.
B. 61,9% và 38,1%.
C. 61,5% và 38,5%.
D. 65% và 35%.
Câu 24: Hỗn hợp X gồm Fe và Al (với tỉ lệ mol 1 : 1). Hòa tan hoàn toàn m gam X bằng dung dịch HCl dư, sau phản ứng thu được 5,6 lít H2 (đktc). Giá trị của m là:
A. 10,2 gam.
B. 8,3 gam.
C. 2,7 gam.
D. 16,6 gam.
Câu 25: Cho 1,25 lít dung dịch KOH 1M tác dụng vừa đủ với x lít dung dịch HCl 0,5M. Giá trị của x là
A. 1,25
B. 2,0
C. 2,5
D. 1,5
Câu 26: Để trung hòa hoàn toàn 100ml dung dịch NaOH 1M cần vừa đủ V ml dung dịch H2SO4 2M. Giá trị của V là:
A. 25ml.
B. 50ml.
C. 100ml.
D. 200ml.
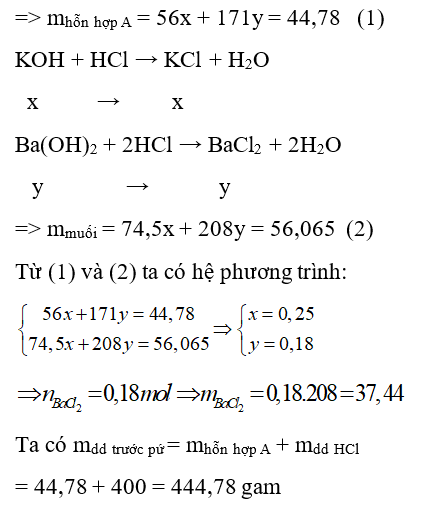
Câu 27: Cho 44,78 gam hỗn hợp A gồm KOH và Ba(OH)2 vào 400 gam dung dịch HCl vừa đủ, phản ứng hoàn toàn thu được dung dịch X. Cô cạn dung dịch X thu được 56,065 gam hỗn hợp muối. Nồng độ phần trăm của BaCl2 trong dung dịch X là
A. 8,42%.
B. 5,34%.
C. 9,36%.
D. 14,01%.
Câu 28: Hòa tan hoàn toàn một hiđroxit của kim loại R bằng dung dịch HCl 14,6% (vừa đủ), sau phản ứng thu được dung dịch chứa muối clorua có nồng độ 17,03%. Công thức hiđroxit của kim loại R là
A. Mg(OH)2.
B. Cu(OH)2.
C. Zn(OH)2.
D. Fe(OH)3.
Câu 29: Hòa tan 2,4 gam oxit của một kim loại hóa trị II vào 21,9 gam dung dịch HCl 10% thì vừa đủ . Oxit đó là:
A. CuO
B. CaO
C. MgO
D. FeO
Câu 30: Hòa tan 1,68 gam oxit của 1 kim loại hóa trị II vào 21,9 gam dung dịch HCl 10% thì phản ứng xảy ra vừa đủ. Công thức của oxit là:
A. CuO
B. CaO
C. MgO
D. FeO
Câu 31: Hòa tan hoàn toàn 23,2 gam hỗn hợp A gồm (FeO, CuO) cần dùng vừa đủ 200 ml dung dịch H2SO4 1,5M thu được dung dịch X. Phần trăm khối lượng của mỗi chất trong hỗn hợp A là
A. 32,23% và 67,77%.
B. 31,03% và 68,97%.
C. 56,25% và 43,75%.
D. 45,55 và 54,45%.
Câu 32: Hòa tan vừa hết 20 gam hỗn hợp CuO và Fe2O3 trong 200 ml dung dịch HCl 3,5M . Khối lượng mỗi oxit trong hỗn hợp là:
A. 4 g và 16 g
B. 10 g và 10 g
C. 8 g và 12 g
D. 14 g và 6 g.
Câu 33: Hòa tan 10 gam hỗn hợp chất rắn gồm Fe, FeO và Cu vào dung dịch HCl loãng dư. Kết thúc phản ứng thấy có 2,24 lít khí H2 (đktc) thoát ra và thu được dung dịch B và 0,8 gam chất rắn C. Cô cạn dung dịch B thu được m gam muối. Gía trị của m là:
A. 19,00 gam
B. 19,05 gam
C. 20 gam
D. 20,05 gam
Câu 34: Lấy 200 ml dung dịch BaCl2 0,6M tác dụng với 400 ml dung dịch H2SO4 0,5M thu được m gam kết tủa. Giá trị của m là
A. 46,60
B. 34,95
C. 23,30
D. 27,96
Câu 35: Khi cho axit tác dụng với bazơ thu được:
A. Muối và khí hiđro.
B. Muối và nước.
C. Dung dịch bazơ.
D. Muối.
Câu 36: Phản ứng giữa dung dịch HCl và NaOH là phản ứng
A. Hóa hợp
B. Trung hòa
C. Thế
D. Phân hủy
Câu 37: Phản ứng giữa natri hiđroxit và axit sunfuric loãng được gọi là phản ứng
A. hiđrat hóa.
B. oxi hóa – khử.
C. trung hòa.
D. thế.
Câu 38: Thêm vài giọt kali hiđroxit vào dung dịch đồng (II) clorua. Sản phẩm thu được là:
A. Cu(OH)2 và KCl.
B. Cu(OH)2 và NaCl.
C. CuOH và KCl.
D. CuOH và NaCl.
Câu 39: Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và H2SO4 cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là
A. 0,8M và 0,6M.
B. 1M và 0,5M.
C. 0,6M và 0,7M.
D. 0,2M và 0,9M.