Đề thi Giữa kì 1 Hóa học lớp 11 có đáp án (Trắc nghiệm - Tự luận - 2 đề)
Đề thi Giữa kì 1 Hóa học lớp 11 có đáp án (Trắc nghiệm - Tự luận - 2 đề)
Với Đề thi Giữa kì 1 Hóa học lớp 11 có đáp án (Trắc nghiệm - Tự luận - 2 đề) được tổng hợp chọn lọc từ đề thi môn Hoá học 11 của các trường trên cả nước sẽ giúp học sinh có kế hoạch ôn luyện từ đó đạt điểm cao trong các bài thi Hoá học lớp 11.

Phòng Giáo dục và Đào tạo .....
Đề thi giữa Học kì 1
Năm học 2024
Môn: Hóa học lớp 11
Thời gian làm bài: 45 phút
(Đề số 1)
Câu 1: Để nhận biết ion photphat ( PO43-), người ta sử dụng thuốc thử
A. Dung dịch AgNO3.
B. Quỳ tím.
C. Dung dịch NaOH.
D. Dung dịch BaCl2.
Câu 2: Chỉ ra nội dung sai:
A. Trong nhóm nitơ, khả năng oxi hoá của các nguyên tố tăng dần từ nitơ đến photpho.
B. Trong các hợp chất, nitơ có thể có các số oxi hoá –3, +1, +2, +3, +4, +5.
C. Trong các hợp chất, các nguyên tố nhóm nitơ có số oxi hoá cao nhất là +5.
D. Các nguyên tố nhóm nitơ thể hiện tính oxi hoá và tính khử.
Câu 3: Cho Cu tác dụng với dung dịch HNO3 loãng tạo ra khí A không màu, hóa nâu ngoài không khí. Cho Fe tác dụng với dung dịch HNO3 tạo ra khí B màu nâu đỏ. A và B lần lượt là
A. NO và NO2.
B. NO2 và NO.
C. NO và N2O.
D. N2 và NO.
Câu 4: Cho 200ml dung dịch NH4NO3 0,1M tác dụng với 250 ml dung dịch KOH 0,1 M. Sau phản ứng thu được thể tích khí là
A. 0,56 lit.
B. 0,224 lit.
C. 0,448 lit.
D. 0,672 lit.
Câu 5: Thuốc thử để nhận biết khí NH3 là
A. Dung dịch NaOH.
B. Quỳ tím ẩm.
C. Dung dịch KCl.
D. Quỳ tím khô.
Câu 6: Cho các kim loại sau : Mg, Al, Cu, Ag, Fe, Cr, Zn, Ca. Số kim loại tác dụng được với dung dịch axit HNO3 đặc, nguội là
A. 3.
B. 4.
C. 5.
D. 6.
Câu 7: Hệ số cân bằng của HNO3 trong phản ứng:
Cu + HNO3 → Cu(NO3)2 + NO + H2O là
A. 3.
B. 2.
C. 4.
D. 8.
Câu 8: Câu trả lời nào dưới đây không đúng khi nói về axit photphoric?
A. Axit photphoric là axit ba nấc.
B. Axit photphoric là axit có độ mạnh trung bình
C. Axit photphoric có tính oxi hóa rất mạnh.
D. Axit photphoric làm quỳ tím chuyển màu đỏ.
Câu 9: Chỉ ra nội dung đúng?
A. Thành phần chính của supephotphat đơn và supephotphat kép là muối canxi hiđrophotphat.
B. Supephotphat đơn chứa Ca(H2PO4)2 và CaSO4; supephotphat kép chứa Ca(H2PO4)2.
C. Supephotphat đơn và supephotphat kép đều sản xuất qua hai giai đoạn.
D. Supephotphat đơn sản xuất qua hai giai đoạn.
Câu 10: Nhiệt phân hoàn toàn 17,0 gam AgNO3 thu được a gam kim loại. Giá trị của a là
A. 2,7 gam.
B. 10,8 gam.
C. 5,4 gam.
D. 13,5 gam.
Câu 11: Chỉ ra nội dung đúng:
A. Photpho đỏ độc, kém bền trong không khí ở nhiệt độ thường.
B. Khi làm lạnh, hơi của photpho trắng chuyển thành photpho đỏ.
C. Photpho đỏ có cấu trúc polime.
D. Photpho đỏ không tan trong nước, nhưng tan tốt trong các dung môi hữu cơ như benzen, ete...
Câu 12: Hai khoáng vật chính của photpho là
A. Photphorit và đolomit.
B. Apatit và đolomit.
C. Photphorit và cacnalit.
D. Apatit và photphorit.
Câu 13: Cho 33,6 gam hỗn hợp Mg, Cu tác dụng vừa đủ với dung dịch HNO3 loãng thu được 13,44 lit NO ( duy nhất ở đktc). Khối lượng Mg, Cu trong hỗn hợp lần lượt là
A. 12,4 và 21,2.
B. 19,2 và 14,4.
C. 21,2 và 12,4.
D. 14,4 và 19,2.
Câu 14: Cho 200 ml dung dịch NaOH 0,1 M tác dụng với 100 ml dung dịch H3PO4 0,1 M. Sau phản ứng thu được muối là
A. NaH2PO4.
B. Na3PO4.
C. Na2HPO4.
D. NaH2PO4 và Na2HPO4.
Câu 15: Chỉ ra nội dung sai:
A. Muối amoni không tác dụng được với dung dịch kiềm
B. Tất cả muối amoni đều dễ tan trong nước.
C. Ion amoni có công thức là NH4+
D. Muối amoni khi tan điện li hoàn toàn.
Câu 16: Khối lượng N có trong 100 kg phân đạm NH4NO3 là
A. 70 kg.
B. 35 kg.
C. 17,5 kg.
D. Đáp án khác.
Câu 17: Cho các muối nitrat: NaNO3, Cu(NO3)2, Mg(NO3)2, Fe(NO3)3, AgNO3, KNO3, Pb(NO3)2, Al(NO3)3. Có bao nhiêu muối nitrat khi bị nhiệt phân sinh ra oxit kim loại, NO2 và O2?
A. 2.
B. 3.
C. 4.
D. 5.
Câu 18: Trong công nghiệp, phần lớn lượng nitơ sản xuất ra được dùng để
A. tổng hợp phân đạm.
B. tổng hợp amoniac.
C. sản xuất axit nitric.
D. làm môi trường trơ trong luyện kim, điện tử...
Câu 19: Cho 31,2 gam hỗn hợp Fe, Cu tác dụng với dung dịch HNO3 đặc, nguội, dư thu được 17,92 lit khí màu nâu đỏ. Khối lượng Fe trong hỗn hợp là
A. 4,4 gam.
B. 1,2 gam.
C. 28,8 gam.
D. 5,6 gam.
Câu 20: Trong các loại phân đạm sau: NH4Cl, (NH4)2SO4, NaNO3, (NH2)2CO. Phân đạm có hàm lượng Nitơ cao nhất là
A. NaNO3.
B. NH4Cl.
C. (NH4)2SO4.
D. (NH2)2CO.
Câu 21. Hoà tan hoàn toàn 9,45 gam kim loại X có hóa trị cao nhất là III bằng HNO3 loãng thu được 5,04 lít (đktc) hỗn hợp khí N2O và NO (không có sản phẩm khử khác), trong đó số mol NO gấp 2 lần số mol N2O. Kim loại X là
A. Zn.
B. Cr.
C. Al.
D. Fe.
Câu 22. Hòa tan hoàn toàn 6,5 gam Zn trong dung dịch HNO3 loãng, dư thu được dung dịch X và 0,224 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là
A. 18,90 gam.
B. 17,80 gam.
C. 19,9 gam.
D. 28,35 gam.
Câu 23. Cho 2,7 gam Al tác dụng hết với dung dịch HNO3 (dư), sinh ra 2,24 lít khí X (sản phẩm khử duy nhất, ở đktc). Khí X là
A. N2O.
B. NO2.
C. N2.
D. NO.
Câu 24. Cho 22,72 gam hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư thu được V lít khí NO duy nhất (ở đktc) và dung dịch X. Cô cạn dung dịch X thu được 77,44 gam muối khan. Giá trị của V là
A. 2,688 lít.
B. 2,24 lít.
C. 4,48 lít.
D. 5,6 lít.
Câu 25. Cho phản ứng hóa học sau:
FeO + HNO3 → Fe(NO3)3 + NO + H2O
Tổng hệ số cân bằng (là các số nguyên và tối giản) của phản ứng hóa học đó là
A. 15.
B. 25.
C. 24.
D. 22.
Đáp án & Hướng dẫn giải
Câu 1. A
Để nhận biết ion photphat dùng AgNO3.
3Ag+ + PO43- → Ag3PO4↓ vàng.
Câu 2. A
Trong nhóm nitơ, khả năng oxi hoá của các nguyên tố giảm dần từ nitơ đến photpho.
Câu 3. A
A là khí không màu hóa nâu ngoài không khí → A là NO.
2NO (không màu) + O2 → 2NO2 (nâu đỏ)
B là khí có màu nâu đỏ → B là NO2.
Câu 4. C
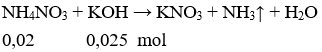
Vậy NH4NO3 hết, nkhí = nNH4NO3 = 0,02 mol
→ Vkhí = 0,02.22,4 = 0,448 lít.
Câu 5. B
Khí NH3 làm xanh quỳ tím ẩm.
Câu 6. C
Các kim loại tác dụng được với HNO3 đặc, nguội là: Mg, Cu, Ag, Zn, Ca.
Câu 7. D
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Câu 8. C
Axit photphoric không có tính oxi hóa.
Câu 9. B
A sai vì thành phần chính của supephotphat đơn là Ca(H2PO4)2 và CaSO4.
C, D sai vì supephotphat đơn được sản xuất qua 1 giai đoạn.
Câu 10. B
Bảo toàn Ag có: nAg = nMuối = 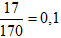
→ a = 0,1.108 = 10,8 gam.
Câu 11. C
A sai vì photpho đỏ bền trong không khí ở nhiệt độ thường.
B sai vì khi làm lạnh hơi P đỏ chuyển thành P trắng.
D sai vì photpho đỏ không tan trong các dung môi thông thường.
Câu 12. D
Hai khoáng vật chính của photpho là Apatit và photphorit.
Câu 13. D
Gọi số mol của Mg và Cu lần lượt là x và y mol.
mhh = 33,6 gam → 24x + 64y = 33,6 (1)
Bảo toàn electron có: 2x + 2y = 3.nNO = 1,8 (2)
Từ (1) và (2) có x = 0,6 và y = 0,3
Khối lượng Mg, Cu trong hỗn hợp lần lượt là 14,4 gam và 19,2 gam.
Câu 14. C
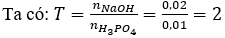
Vậy sau phản ứng thu được: Na2HPO4.
Câu 15. A
Muối amoni tác dụng với dung dịch kiềm giải phóng NH3
Ví dụ:
NH4Cl + NaOH → NH3 + NaCl + H2O.
Câu 16. B
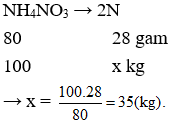
Câu 17. D
Các muối nitrat của các kim loại từ Mg đến Cu trong dãy hoạt động hóa học khi nhiệt phân sinh ra oxit kim loại, NO2 và O2.
→ Các muối thỏa mãn đề bài: Cu(NO3)2, Mg(NO3)2, Fe(NO3)3, Pb(NO3)2, Al(NO3)3.
Câu 18. B
Trong công nghiệp, phần lớn lượng nitơ được sản xuất ta được dùng để tổng hợp amoniac từ đó điều chế ra axit nitric, phân đạm....
Câu 19. D
Cho Fe, Cu tác dụng với HNO3đặc, nguội chỉ có Cu phản ứng.
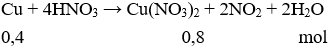
mFe = 31,2 – 0,4.64 = 5,6 gam.
Câu 20. D
Ure: (NH2)2CO có hàm lượng N cao nhất.
Câu 21. C
nhh khí = 5,04 : 22,4 = 0,225 mol
Gọi số mol N2O là a → nNO = 2a → a = 0,075 mol
Gọi số mol X là x mol. Theo bài ra ta có các quá trình:
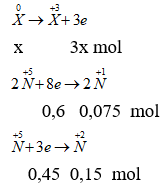
Áp dụng định luật bảo toàn số mol electron ta có: ne nhường = ne nhận
→ 3x = 0,6 + 0,45
→ x = 0,35 → MX = 9,45 : 0,35 = 27 → X là Nhôm.
Câu 22. C
nZn = 0,1 mol; nN2 = 0,01 mol.
Giả sử sản phẩm khử sinh ra chỉ có N2. Ta có nZn.2 = 0,2 ≠ nN2.10 = 0,1.
Vậy còn có sản phẩm khử là NH4NO3 x mol
Áp dụng định luật bảo toàn electron có: nZn.2 = nN2.10 + nNH4NO3.8
→ nNH4NO3 = 0,0125 mol.
Muối trong X gồm Zn(NO3)2 và NH4NO3.
Bảo toàn nguyên tố Zn có nZn(NO3)2 = nZn = 0,1
→ mmuối = 0,1.(65 + 62.2) + 0,0125.(18 +62) = 19,9 gam.
Câu 23. D
nAl = 0,1 mol; nx = 0,1 mol
Áp dụng định luật bảo toàn electron có:
3.nAl = nx. n ( với n là số e nhận)
→ 0,1.3 = 0,1.n → n = 3. Vậy khí X là NO.
Câu 24. A
Quy đổi hỗn hợp sắt và oxit sắt thành hỗn hợp gồm Fe (x mol) và O (y mol).
→ 56x + 16y = 22,72.
mmuối = mFe(NO3)3 = 0,32 mol.
Bảo toàn Fe có nFe = x = nmuối = 0,32 mol → y = 0,3 mol.
Áp dụng định luật bảo toàn electron có:
nFe.3 = nO.2 + nNO.3 → nNO= 0,12
→ V = 0,12.22,4 = 2,688 lít.
Câu 25. D
3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O
Tổng hệ số cân bằng = 3 + 10 + 3 + 1 + 5 = 22.

Phòng Giáo dục và Đào tạo .....
Đề thi giữa Học kì 1
Năm học 2024
Môn: Hóa học lớp 11
Thời gian làm bài: 45 phút
(Đề số 2)
Cho nguyên tử khối (đvC) của các nguyên tử: H = 1,C = 12, N = 14, O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K= 39.
Câu 1. Ở 3000°C (hoặc có tia lửa điện) N2 hoá hợp với O2 theo phương trình phản ứng nào sau đây
A. N2 + O2 ⇌ 2NO.
B. N2 + 2O2 ⇌ 2NO2.
C. 4N2 + O2 ⇌ 2N2O.
D. 4N2 + 3O2 ⇌ 2N2O.
Câu 2. Có thể dùng bình đựng HNO3 đặc, nguội bằng kim loại nào ?
A. Đồng, bạc.
B. Đồng, chì.
C. Sắt, nhôm.
D. Đồng, kẽm.
Câu 3. Magie photphua có công thức là
A. Mg2P2O7.
B. Mg3P2.
C. Mg2P3.
D. Mg3(PO4)3.
Câu 4. Cho các dung dịch: (NH4)2SO4; NH4Cl; Al(NO3)3; Fe(NO3)3; Cu(NO3)2 .Để phân biệt các dung dịch trên chỉ dùng 1 hóa chất nào sau?
A. Dung dịch NH3.
B. Dung dịch Ba(OH)2.
C. Dung dịch KOH.
D. Dung dịch NaCl.
Câu 5. Từ 34 tấn NH3 sản xuất được 160 tấn dung dịch HNO3 63%. Hiệu suất
A. 80%
B. 50%
C. 60%
D. 85%.
Câu 6.Chọn cấu hình electron lớp ngoài cùng của nguyên tố nhóm VA?
A. ns2np5.
B. ns2np3.
C. ns2np2.
D. ns2np4.
Câu 7. Xác định chất (A) và (B) trong chuỗi sau :
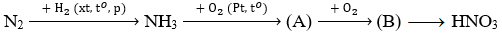
A. (A) là NO, (B) là N2O5.
B. (A) là N2, (B) là N2O5.
C. (A) là NO, (B) là NO2.
D. (A) là N2, (B) là NO2.
Câu 8. Trong phản ứng nào sau đây, nitơ thể hiện tính khử ?
A. N2 + 3H2 ⇌ 2NH3
B. N2 + 6Li → 2Li3N
C. N2 + O2 ⇌ 2NO
D. N2 + 3Mg → Mg3N2
Câu 9. Trong thí nghiệm đồng tác dụng với dung dịch HNO3 đặc để tránh khí độc NO2 bay ra người ta thường nút ống nghiệm bằng bông có tẩm dung dịch nào sau đây?
A. dd NaCl .
B. dd NaOH.
C. dd HCl.
D. dd NaNO3.
Câu 10. Cho sơ đồ: 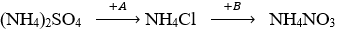
Trong sơ đồ A ,B lần lượt là các chất :
A. HCl , HNO3
B. CaCl2 , HNO3
C. BaCl2 , AgNO3
D. HCl , NaNO3.
Câu 11. Khi nhiệt phân AgNO3 thu được những sản phẩm nào?
A. Ag, NO2, O2.
B. Ag, NO,O2.
C. Ag2O, NO2, O2.
D. Ag2O, NO, O2.
Câu 12. Hiện tượng xảy ra khi cho giấy quỳ khô vào bình đựng khí amoniac là
A. Giấy quỳ chuyển sang màu đỏ.
B. Giấy quỳ chuyển sang màu xanh.
C. Giấy quỳ mất màu.
D. Giấy quỳ không chuyển màu.
Câu 13. Sản phẩm của phản ứng nhiệt phân nào dưới đây là không đúng?
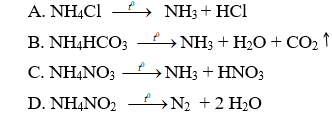
Câu 14. Nồng độ ion NO3- trong nước uống tối đa cho phép là 9 ppm. Nếu thừa ion NO3- sẽ gây một loại bệnh thiếu máu hoặc tạo thành nitrosamin, một hợp chất gây ung thư đường tiêu hóa. Để nhận biết ion NO3-, người ta dùng:
A. CuSO4 và NaOH.
B. Cu và NaOH.
C. Cu và H2SO4.
D. CuSO4 và H2SO4.
Câu 15. Cần lấy bao nhiêu lít khí N2 và H2 để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí được đo trong cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%.
A. 33,6 lít N2 và 100,8 lít H2.
B. 8,4 lít N2 và 25,2 lít H2.
C. 268,8 lít N2 và 806,4 lít H2.
D. 134,4 lít N2 và 403,2 lít H2.
Câu 16. Hòa tan 32 g hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư), thoát ra 6,72 lít khí NO (đktc). Khối lượng CuO trong hỗn hợp ban đầu là
A. 1,2g.
B. 1,88g.
C. 2,52g.
D. 3,2g.
Câu 17. Cho 44g NaOH vào dung dịch chứa 39,2g H3PO4. Sau khi phản ứng xảy ra hoàn toàn , đem cô dung dịch thu được đến cạn khô. Hỏi những muối nào được tạo nên và khối lượng muối khan thu được là bao nhiêu ?
A. Na3PO4 và 50,0g .
B. NaH2PO4 và 49,2g ; Na2HPO4 và 14,2g
C. Na2HPO4 và 15,0g.
D. Na2HPO4 và 14,2g ; Na3PO4 và 49,2g.
Câu 18. Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của?
A. P.
B. P2O5.
C. PO43- .
D. H3PO4.
Câu 19. Chọn phát biểu đúng?
A. Photpho trắng tan trong nước không độc.
B. Photpho trắng được bảo quản bằng cách ngâm trong nước.
C. Photpho trắng hoạt động hoá học kém hơn photpho đỏ.
D. Photpho đỏ phát quang màu lục nhạt trong bóng tối.
Câu 20. Thêm 0,15 mol KOH vào dung dịch chứa 0,1 mol H3PO4. Sau phản ứng, trong dung dịch có muối nào ?
A. KH2PO4 và K2HPO4.
B. K2HPO4 và K3PO4.
C. KH2PO4.
D. KH2PO4; K2HPO4 và K3PO4.
Câu 21. Cho m(g) Al tan hoàn toàn trong dung dịch HNO3 thấy tạo ra 11,2 lít (đktc) hỗn hợp 3 khí NO, N2O, N2 với tỷ lệ mol tương ứng là 1: 2 : 2. Giá trị của m là
A. 16.47g.
B. 23g.
C. 35.1g.
D. 12.73g.
Câu 22. Hòa tan hết m(g) Al trong dung dịch HNO3, thu được hỗn hợp khí (đktc) gồm NO và NO2 có thể tích là 8,96 lít và có tỷ khối đối với hiđro là 16,75. Giá trị của m là
A. 9,252.
B. 2,7g.
C. 8,1g.
D. 9,225g.
Câu 23. Hoà tan hoàn toàn 19,2 gam một kim loại M trong dung dịch HNO3 ta thu được 4,48 lít NO (đktc). Kim loại M là
A. Zn (M = 65).
B. Fe (M = 56).
C. Mg (M = 24).
D. Cu (M = 64).
Câu 24. Hòa tan hoàn toàn 15,9g hỗn hợp 3 kim loại Al, Mg, Cu bằng dd HNO3 thu được 6,72 lit khí NO (là sản phẩm khử duy nhất ở đktc) và dd X. Đem cô cạn dd X thì thu được khối lượng muối khan là
A. 77,1g.
B. 71,7g.
C. 17,7g.
D. 53,1g.
Câu 25. Cho 1,92 gam Cu vào 100ml dung dịch chứa đồng thời KNO3 0,16M và H2SO4 0,4M thấy sinh ra một chất khí có tỉ khối so với H2 là 15 và dung dịch A. Thể tích khí sinh ra (ở đktc) là
A. 3,584 lít.
B. 0,3584lít.
C. 35,84 lít.
D. 358,4 lít.
Đáp án & Hướng dẫn giải
Câu 1. A
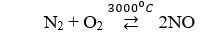
Câu 2. C
Sắt, nhôm bị thụ động hóa trong HNO3 đặc, nguội nên có thể dùng bình bằng những kim loại này để chứa HNO3 đặc, nguội.
Câu 3. B
Magie photphua: Mg3P2.
Câu 4. B
Dùng Ba(OH)2:
+ Có khí mùi khai thoát ra và xuất hiện kết tủa trắng → (NH4)2SO4.
(NH4)2SO4 + Ba(OH)2 → BaSO4 ↓ trắng + 2NH3 ↑ + 2H2O
+ Có khí mùi khai thoát ra → NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 ↑ + 2H2O
+ Có kết tủa keo trắng, khi cho đến dư Ba(OH)2 kết tủa tan → Al(NO3)3
Al3+ + 3OH- → Al(OH)3 ↓ keo trắng
Al(OH)3 ↓ + OH- → AlO2- + 2H2O
+ Có kết tủa nâu đỏ xuất hiện → Fe(NO3)3.
Fe3+ + 3OH- → Fe(OH)3 ↓ nâu đỏ
+ Có kết tủa xanh → Cu(NO3)2
Cu(NO3)2 + Ba(OH)2 → Cu(OH)2↓ xanh + Ba(NO3)2.
Câu 5. A
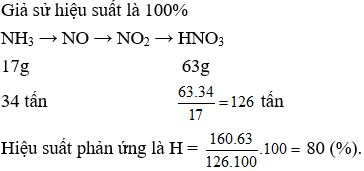
Câu 6. B
Nhóm VA có 5 electron lớp ngoài cùng. Cấu hình electron lớp ngoài cùng có dạng: ns2np3.
Câu 7. C
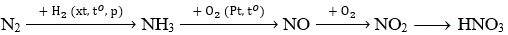
Câu 8. C
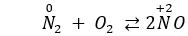
Số oxi hóa của N tăng từ 0 lên +2. Vậy N2 thể hiện tính khử.
Câu 9. B
2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O.
Câu 10. C
(NH4)2SO4 + BaCl2 → BaSO4 ↓ + 2NH4Cl
NH4Cl + AgNO3 → AgCl ↓ + NH4NO3.
Câu 11. A
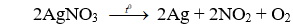
Câu 12. D
Khí NH3 không làm đổi màu giấy quỳ khô.
Câu 13. C
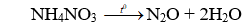
Câu 14. C
Để nhận ra NO3- dùng Cu và H2SO4. Hiện tượng: Cu tan dần, dung dịch sau phản ứng có màu xanh, thoát ra khí không màu hóa nâu trong không khí.
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
Câu 15. D
Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
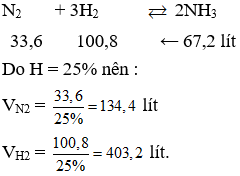
Câu 16. D
Bảo toàn electron có:
2.nCu = 3.nNO → nCu = 0,45 mol
mCuO = 32 – 0,45.64 = 3,2 gam.
Câu 17. D
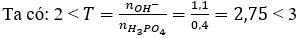
Vậy sau phản ứng thu được hai muối Na2HPO4 (x mol) và Na3PO4 (y mol)
Bảo toàn Na có: 2x + 3y = 1,1 (1)
Bảo toàn C có: x + y = 0,4 (2)
Từ (1) và (2) có x = 0,1 và y = 0,3 mol
Vậy khối lượng Na2HPO4 và Na3PO4 lần lượt là 14,2 gam và 49,2 gam.
Câu 18. B
Độ dinh dưỡng của phân lân được tính bằng hàm lượng % của P2O5.
Câu 19. B
A sai vì photpho trắng độc.
C sai vì photpho trắng hoạt động mạnh hơn photpho đỏ.
D sai vì Photpho trắng phát quang màu lục nhạt trong bóng tối.
Câu 20. A
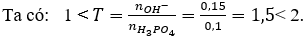
Vậy sau phản ứng thu được hai muối KH2PO4 và K2HPO4.
Câu 21. C
Gọi số mol của NO là a mol → số mol của N2O là 2a mol; số mol N2 là 2a mol.
nkhí = 0,5 mol → a + 2a + 2a = 0,5 mol → a = 0,1 mol.
Bảo toàn electron có:
3.nAl = 3.nNO + 8.nN2O + 10.nN2 → nAl = 1,3 (mol)
Vậy m = 1,3.27 = 35,1 gam.
Câu 22. D
Gọi số mol của NO và NO2 lần lượt là x và y (mol)
Theo bài ra ta có: x + y = 0,4 (mol) (1)
mkhí = 0,4.16,75.2 = 13,4 gam → 30x + 46y = 13,4 (gam) (2)
Từ (1) và (2) có: x = 0,3125 mol và y = 0,0875 mol.
Bảo toàn electron có:
3.nAl = 3.nNO + nNO2 → nAl = 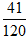
mAl = 27. nAl = 9,225 gam.
Câu 23. D
Bảo toàn electron có: 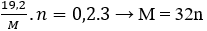
Vậy n = 2; M = 64 thỏa mãn. Kim loại cần tìm là Cu.
Câu 24. B
Ta có:
nNO3- (muối) = ne nhường = ne nhận = 3.nNO = 0,9 mol
mmuối = mKL + mNO3 = 15,9 + 0,9.62 = 71,7 gam.
Câu 25. B
Mkhí = 15.2 = 30. Vậy khí là NO.