Lý thuyết KHTN 8 Cánh diều Bài 8: Acid
Haylamdo biên soạn và sưu tầm tóm tắt lý thuyết Khoa học tự nhiên 8 Bài 8: Acid sách Cánh diều hay nhất, ngắn gọn sẽ giúp học sinh lớp 8 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn KHTN 8.
Lý thuyết KHTN 8 Cánh diều Bài 8: Acid
I. Khái niệm acid
Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H+.
Acid tạo ra ion H+ theo sơ đồ sau:
Acid → ion H+ + ion âm gốc acid
Ví dụ:
HCl |
→ |
H+ |
+ |
|
Hydrochloric acid |
Ion hydrogen |
Ion chloride |
||
H2SO4 |
→ |
2H+ |
+ |
|
Sulfuric acid |
Ion hydrogen |
Ion sulfate |
II. Tính chất hoá học của acid
1. Làm đổi màu chất chỉ thị
Dung dịch acid làm quỳ tím chuyển sang màu đỏ.
Quỳ tím được dùng làm chất chỉ thị màu để nhận ra dung dịch acid.
2. Tác dụng với kim loại
Dung dịch acid tác dụng được với nhiều kim loại tạo ra muối và khí hydrogen.
Acid + Kim loại → Muối + Hydrogen
Ví dụ:
Zn + 2HCl → ZnCl2 + H2
Mg + H2SO4 loãng → MgSO4 + H2
Lưu ý: Riêng HNO3, H2SO4 đặc tác dụng với kim loại sẽ được học sau.
III. Ứng dụng của một số acid
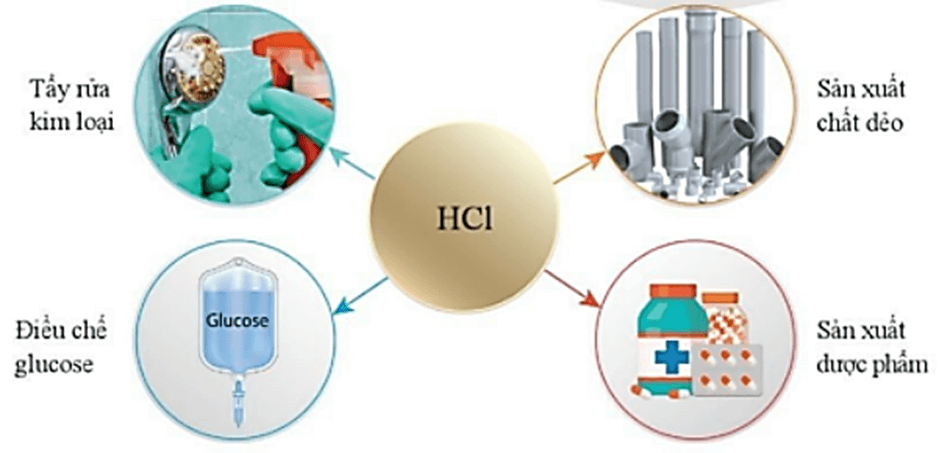
1. Hydrochloric acid (HCl)
Hydrochloric acid có trong dạ dày của người và động vật giúp tiêu hoá thức ăn. Hydrochloric acid được sử dụng nhiều trong công nghiệp.
Một số ứng dụng quan trong của hydrochloric acid được thể hiện trong sơ đồ sau:
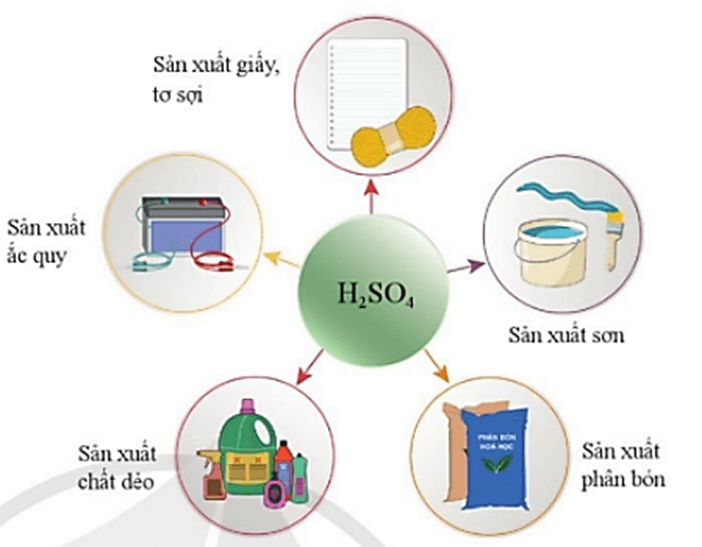
2. Sulfuric acid
Sulfuric acid là một hoá chất quan trọng được sử dụng nhiều trong công nghiệp.
Một số ứng dụng quan trọng của sulfuric acid được trình bày trong sơ đồ:
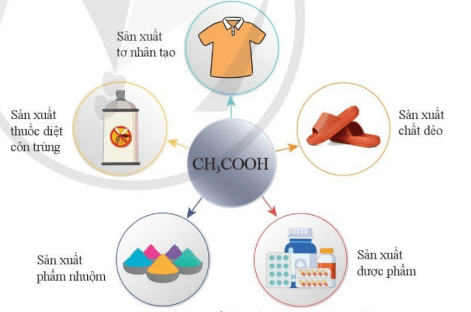
3. Acetic acid (CH3COOH)
Acetic acid là một acid hữu cơ có trong giấm ăn với nồng độ khoảng 4%. Một số ứng dụng của acetic acid được thể hiện trong sơ đồ sau: