Top 50 bài tập ôn tập Hóa học 12 Chương 5 (có đáp án)
Haylamdo biên soạn và sưu tầm 50 bài tập ôn tập Hóa học 12 Chương 5 hóa học 12 mới nhất được biên soạn bám sát chương trình hóa học 12 giúp các bạn học tốt môn Hóa học hơn.
Bài tập ôn tập Hóa học 12 Chương 5 (có đáp án)
Câu 1:
Đốt cháy 6,48 gam bột Al trong oxi, sau một thời gian thu được hỗn hợp rắn X. Hòa tan toàn bộ X trong dung dịch HCl 7,3% vừa đủ thu được a mol khí H2 và dung dịch Y có nồng độ là 8,683%. Các phản ứng xảy ra hoàn toàn và nước bay hơi không đáng kể. Giá trị của a là:
A. 0,24.
B. 0,15.
C. 0,12.
D. 0,18.
Xem lời giải »
Câu 2:
Cho 2,97 gam Al tác dụng vừa đủ với 2,688 lít (đktc) hỗn hợp khí gồm Cl2 và O2 chỉ thu được m gam hỗn hợp oxit và muối clorua. Giá trị của m gần nhất với giá trị nào sau đây?
A. 8,5
B. 10,2
C. 9,7
D. 5,8
Xem lời giải »
Câu 3:
Cho 12,45 gam hỗn hợp Mg, Zn, Fe tác dụng hết với dung dịch HCl thấy thoát ra 6,72 lít H2 (đktc). Tính khối lượng muối tạo thành?
A. 33 gam
B. 33,75 gam
C. 34 gam
D. 33,50 gam
Xem lời giải »
Câu 4:
Cho 16 gam hỗn hợp bột Fe và Mg tác dụng với dung dịch HCl dư thấy có 1 gam khí H2 bay ra. Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam?
A. 33,75 gam.
B. 1,5 gam.
C. 87 gam.
D. 51,5 gam
Xem lời giải »
Câu 5:
Hoà tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là:
A. 38,93 gam.
B. 103,85 gam.
C. 25,95 gam.
D. 77,86 gam.
Xem lời giải »
Câu 6:
Cho 7,28 gam kim loại M tác dụng hoàn toàn với dung dịch HCl, sau phản ứng thu được 2,912 lít H2 ở đktc. M là kim loại nào dưới đây?
A. Zn
B. Mg
C. Fe
D. Al
Xem lời giải »
Câu 7:
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%, thu được 2,24 lít khí H2 (ở đktc). Khối lượng dung dịch thu được sau phản ứng là :
A. 101,68 gam.
B. 88,20 gam.
C. 101,48 gam.
D. 97,80 gam.
Xem lời giải »
Câu 8:
Cho 2,52g một kim loại tác dụng với dd H2SO4 loãng tạo ra 6,84g muối sunfat. Kim loại đó là:
A. Mg
B. Fe
C. Cr
D. Mn
Xem lời giải »
Câu 9:
Cho hỗn hợp Cu và Fe hòa tan vào dung dịch H2SO4 đặc nóng tới khi phản ứng hoàn toàn, thu được dung dịch X và một phần Cu không tan. Cho dung dịch NH3 dư vào dung dịch X thu được kết tủa Y. Thành phần của kết tủa Y gồm
A. Fe(OH)2.
B. Fe(OH)2, Cu(OH)2
C. Fe(OH)3, Cu(OH)2
D. Fe(OH)3.
Xem lời giải »
Câu 10:
Hòa tan hết m gam kim loại M cần dùng 136 gam dung dịch HNO3 31,5%. Sau khi kết thúc phản ứng thu được dung dịch X và 0,12 mol khí NO duy nhất. Cô cạn dung dịch X thu được (2,5m + 8,49) gam muối khan. Kim loại M là
A. Mg.
B. Cu.
C. Ca.
D. Zn.
Xem lời giải »
Câu 11:
Hòa tan hoàn toàn 3,2 gam Cu bằng dung dịch HNO3, thu được x mol NO2 (là sản phẩm khử duy nhất của N+5). Giá trị của x là
A. 0,25
B. 0,20
C. 0,10
D. 0,15
Xem lời giải »
Câu 12:
Cho m gam hỗn hợp Fe và Cu tác dụng với dung dịch H2SO4 loãng dư thu được 4,48 lít H2 (đktc). Nếu cho hỗn hợp trên phản ứng với dung dịch H2SO4 đặc nguội dư thu được 8,96 khí SO2 (sản phẩm khử duy nhất, ở đktc). Giá trị của m gần nhất là
A. 17,72.
B. 36,91.
C. 17,81.
D. 36,82.
Xem lời giải »
Câu 13:
Hòa tan hoàn toàn 25,3 gam hỗn hợp X gồm Mg, Al và Zn bằng dung dịch HNO3. Sau khi phản ứng kết thúc thu được dung dịch Y và 4,48 lít (đktc) khí Z (gồm 2 hợp chất khí không màu) có khối lượng 7,4 gam. Cô cạn dung dịch Y thu được 122,3 gam hỗn hợp muối. Số mol HNO3 đã tham gia phản ứng gần nhất với giá trị nào sau đây?
A. 1,95 mol.
B. 1,81 mol.
C. 1,91 mol.
D. 1,80 mol.
Xem lời giải »
Câu 14:
Cho hỗn hợp Al, Fe vào dung dịch HNO3 loãng, dư thu được 6,72 lít NO (là sản phẩm khử duy nhất của N+5 ở đktc). Số mol axit đã phản ứng là
A. 0,3 mol.
B. 0,6 mol.
C. 1,2 mol.
D. 2,4 mol.
Xem lời giải »
Câu 15:
Cho hỗn hợp X gồm Mg và Fe vào dung dịch axit H2SO4 đặc, nóng đến khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y và một phần Fe không tan. Chất tan có trong dung dịch Y là
A. MgSO4 và FeSO4.
B. MgSO4.
C. MgSO4 và Fe2(SO4)3.
D. MgSO4, Fe2(SO4)3 và FeSO4
Xem lời giải »
Câu 16:
Hòa tan m gam hỗn hợp T gồm FexOy, Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m+60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m - 6,04) gam rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với giá trị nào sau đây?
A. 21,0
B. 23,0
C. 22,0
D. 24,0
Xem lời giải »
Câu 17:
Cho các chất sau FeCO3, Fe3O4, FeS, FeS2. Nếu hòa tan hoàn toàn cùng số mol mỗi chất trên vào dung dịch H2SO4 đặc, nóng (dư) thì số mol H2SO4 đã phản ứng lớn nhất ở phản ứng với
A. FeS2
B. Fe3O4
C. FeCO3
D. FeS
Xem lời giải »
Câu 18:
Cho ít bột Fe vào dung dịch AgNO3 dư, sau khi kết thúc thí nghiệm thu được dung dịch X gồm:
A. Fe(NO3)2, H2O
B. Fe(NO3)3, AgNO3 dư
C. Fe(NO3)2, AgNO3 dư
D. Fe(NO3)2, Fe(NO3)3, AgNO3 dư
Xem lời giải »
Câu 19:
Ngâm một lá sắt trong dung dịch đồng sunfat, sau phản ứng khối lượng lá sắt tăng thêm 1,2 g. khối lượng đồng tạo ra bám trên sắt là bao nhiêu?
A. 6,9g.
B. 7,2g.
C. 2,7g
D. 9,6g.
Xem lời giải »
Câu 20:
Cho 8,4 g Fe vào dung dịch có chứa 0,4mol AgNO3. Kết thúc phản ứng, khối lượng bạc là bao nhiêu?
A. 42,3g.
B. 21,6g.
C. 43,2g.
D. 26,1g.
Xem lời giải »
Câu 21:
Cho 5,6 gam bột Fe tác dụng với 500 ml dung dịch AgNO3 0,5 M . Tính khối lượng muối và khối lượng kim loại thu được?
A. 21,1g; 27g.
B. 27g; 21,1g
C. 21g; 27g.
D. 27g; 21g.
Xem lời giải »
Câu 22:
Cho a mol bột kẽm vào dung dịch có hòa tan b mol Fe(NO3)3. Tìm điều kiện liên hệ giữa a và b để sau khi kết thúc phản ứng không có kim loại.
A. a ≥ 2b
B. b > 3a
C. b ≥ 2a
D. b = 2a/3
Xem lời giải »
Câu 23:
Nhúng một lá kim loại M (chỉ có hoá trị hai trong hợp chất) có khối lượng 50 gam vào 200 ml dung dịch AgNO3 1M cho đến khi phản ứng xảy ra hoàn toàn. Lọc dung dịch, đem cô cạn thu được 18,8 gam muối khan. Kim loại M là
A. Mg
B. Cu
C. Zn
D. Fe
Xem lời giải »
Câu 24:
Nhúng 1 thanh kim loại Zn(dư) vào 1 dd chứa hỗn hợp 3,2g CuSO4 và 6,24g CdSO4. Sau khi Cu và Cd bị đẩy hoàn toàn khỏi dd thì khối lượng Zn tăng hoặc giảm bao nhiêu:
A. Tăng 1,39 g
B. giảm 1,39g
C. tăng 4g
D. kết quả khác
Xem lời giải »
Câu 25:
Nhúng 19,5g thanh kim loại Zn vào dd chứa 0,2mol Cu(NO3)2 và 0,2 mol Pb(NO3)2.Chất rắn thu được sau khi phản ứng xảy ra hoàn toàn có khối lượng là:
A. 10,2g
B. 12,5g
C. 33,5 g
D. 46.5g
Xem lời giải »
Câu 1:
Cho 6,48 gam bột kim loại nhôm vào 100 ml dung dịch hỗn hợp Fe2(SO4)3 1M và ZnSO4 0,8M. Sau khi kết thúc phản ứng, thu được hỗn hợp các kim loại có khối lượng m gam. Trị số của m là:
A. 14,5 gam
B. 16,4 gam
C. 15,1 gam
D. 12,8 gam
Xem lời giải »
Câu 2:
Cho 1 đinh Fe vào 1 lit dd chứa Cu(NO3)2 0,2M và AgNO3 0,12M. Sau khi pư kết thúc thu đc dd A với màu xanh đã nhạt 1 phần và 1 chất rắn B có khối lượng lớn hơn khối lượng của đinh Fe ban đầu là 10,4g. Tính khối lượng của đinh Fe ban đầu.
A. 11,2g
B. 5,6g
C. 16,8g
D. 8,96g
Xem lời giải »
Câu 3:
Cho hỗn hợp bột gồm 2,7 gam Al và 5,6 gam Fe vào 550 ml dung dịch AgNO3 1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là (biết thứ tự trong dãy thế điện hoá: Fe3+/Fe2+ đứng trước Ag+/Ag)
A. 59,4.
B. 64,8.
C. 32,4.
D. 54,0.
Xem lời giải »
Câu 4:
Cho m gam hỗn hợp bột Zn và Fe vào lượng dư dung dịch CuSO4. Sau khi kết thúc các phản ứng, lọc bỏ phần dung dịch thu được m gam bột rắn. Thành phần phần trăm theo khối lượng của Zn trong hỗn hợp bột ban đầu là:
A. 12,67%.
B. 90,27%.
C. 82,20%.
D. 85,30%.
Xem lời giải »
Câu 5:
Cho 5,6g gồm Mg và Cu tác dụng với 400ml dd AgNO3 1M. Phản ứng hoàn toàn thu được 32,4 g chất rắn A và dd nước lọc B. Khối lượng mỗi kim loại trong hỗn hợp đầu (lần lượt Mg và Cu) là:
A. 2,6 và 3
B. 4,15 và 1,45
C. 3,52 và 2,08
D. Đáp án khác
Xem lời giải »
Câu 6:
Cho hỗn hợp (Y) gồm 2,8 gam Fe và 0,81 gam Al vào 200ml dung dịch (C) chứa AgNO3 và Cu(NO3)2. Kết thúc phản ứng thu được dung dịch (D) và 8,12 gam chất rắn (E) gồm ba kim loại. Cho (E) tác dụng với dung dịch HCl dư, ta thu được 0,672 lít H2 (đktc). Tính nồng độ mol/l AgNO3, Cu(NO3)2 trước khi phản ứng.

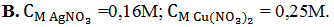
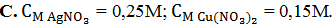

Xem lời giải »
Câu 7:
Một hỗn hợp X gồm 6,5 gam Zn và 4,8 gam Mg được cho vào 200ml dung dịch chứa CuSO4 0,5 M và AgNO3 0,3M. Tính khối lượng chất rắn A thu được?
A. 26,1g
B. 23,6g
C. 21,06g
D. 34,2g.
Xem lời giải »
Câu 8:
Khi nhúng thanh Mg có khối lượng m gam vào dung dịch hỗn hợp X chứa a mol Cu(NO3)2 và b mol HCl. Sau khi phản ứng xảy ra hoàn toàn lấy thanh Mg ra (NO là sản phẩm khử duy nhất của N+5) . Ta có đồ thị dưới đây biểu diễn sự phụ thuộc của khối lượng Mg vào thời gian phản ứng:
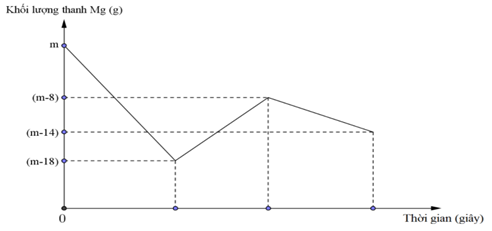
Tỉ lệ a:b là:
A. 1:12
B. 1:8
C. 1:6
D. 1:10
Xem lời giải »
Câu 9:
Cho 2 thanh kim loại M có hóa trị II và có khối lượng bằng nhau.Nhúng thanh 1 vào dd Cu(NO3)2 và thanh 2 vào dd Pb(NO3)2. Sau 1 thời gian khối lượng thanh 1 giảm 0,2% và thanh 2 tăng 28,4 % so với thanh kim loại đầu. Số mol của Cu(NO3)2 và Pb(NO3)2 trong 2 dd giảm như nhau. Kim loại M là:
A. Zn
B. Fe
C. Mg
D. Cd
Xem lời giải »
Câu 10:
Cho 7,8 gam hỗn hợp Mg, Al tác dụng hết với dung dịch HCl dư sau phản ứng thấy khối lượng dung dịch tăng thêm 7 gam. Tính số mol HCl đã tham gia phản ứng.
A. 0,8 mol
B. 0,4mol
C. 0,3 mol
D. 0,25 mol
Xem lời giải »
Câu 11:
Hoà tan p gam hỗn hợp X gồm CuSO4 và FeSO4 vào nước thu được dung dịch Y. Cho m gam bột Zn dư tác dụng với dung dịch Y sau phản ứng thu được m-0,216 gam chất rắn. Nếu cho dung dịch Y tác dụng với BaCl2 dư thu được 27,96 gam kết tủa. p có giá trị là
A. 20,704 gam.
B. 20,624 gam.
C. 25,984 gam.
D. 19,104 gam.
Xem lời giải »
Câu 12:
Cho m gam Mg vào 1 lít dung dịch Cu(NO3)2 0,1M và Fe(NO3)2 0,1M. Sau phản ứng thu được 9,2 gam chất rắn và dung dịch B. Giá trị của m là
A. 3,36 gam.
B. 2,88 gam.
C. 3,6 gam.
D. 4,8 gam.
Xem lời giải »
Câu 13:
Cho m gam hỗn hợp gồm Fe và Al ở dạng bột vào 200ml dd CuSO4 0,525M. Khuấy kỹ hỗn hợp để các phản ứng hóa học xảy ra hoàn toàn. Sau phản ứng thu được 7,84g chất rắn A gồm 2 kim loại và dung dịch B. Để hòa tan hoàn toàn chất rắn A cần dùng ít nhất bao nhiêu ml dd HNO3 2M, biết rằng phản ứng sinh ra sản phẩm khử duy nhất là NO?
A. 211,12 ml
B. 221,13 ml
C. 166,67 ml
D. 233,33 ml
Xem lời giải »
Câu 14:
Cho m gam hỗn hợp bột kim loại X gồm Cu và Fe vào trong dung dịch AgNO3 dư thu được m + 54,96 gam chất rắn và dung dịch Y. Nếu cho m gam X tác dụng dung dịch HNO3 loãng dư thu được 4,928 lít NO (đktc). m có giá trị là:
A. 19,52 gam.
B. 16,32 gam.
C. 19,12 gam.
D. 22,32
Xem lời giải »
Câu 15:
Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 ?
A. Fe, Ni, Sn
B. Zn, Cu, Mg
C. Hg, Na, Ca
D. Al, Fe, CuO
Xem lời giải »
Câu 16:
Cho dãy các kim loại: Na, Ba, Al, K, Mg. Số kim loại trong dãy phản ứng với lượng dư dung dịch FeCl3 thu được kết tủa là
A. 3
B. 4
C. 2
D. 5
Xem lời giải »
Câu 17:
Điện phân dung dịch AgNO3 trong thời gian 15 phút, cường độ dòng điện 5 Ampe. Khối lượng Ag thu được ở catot là:
A. 6,037 gam
B. 5,036 gam.
C. 7,001 gam
D. 5,531 gam
Xem lời giải »
Câu 18:
Điện phân dung dịch CuCl2, điện cực trơ bằng dòng điện 5A trong 45 phút 20 giây. Khối lượng kim loại sinh ra trên catot và thể tích khí sinh ra ở anot (ở đktc) lần lượt bằng:
A. 4,512 g và 3,1584 lít
B. 4,512 g và 1,5792 lít
C. 2,256 g và 3,1584 lít
D. 2,256 g và 1,5792 lít
Xem lời giải »
Câu 19:
Điện phân dung dịch NaCl cho đến khi hết muối với dòng điện 1,61A thấy hết 60 phút. Tính khối lượng khí thoát ra, biết rằng điện cực trơ, màng ngăn xốp.
A. 2,13 gam.
B. 0,06 gam.
C. 2,19 gam.
D. 2,22 gam.
Xem lời giải »
Câu 20:
Điện phân dung dịch CuSO4 bằng điện cực trơ với dòng điện có cường độ I = 0,5A trong thời gian 1930 giây thì khối lượng đồng và thể tích khí O2 sinh ra là:
A. 0, 15g và 0,112 lít
B. 0, 32g và 0, 056 lít
C. 0, 32g và 0, 168 lít
D. 1, 28g và 0, 224 lít
Xem lời giải »
Câu 21:
Điện phân hoàn toàn 200 ml một dung dịch chứa 2 muối là Cu(NO3)2 và AgNO3 với I = 0,804A, thời gian điện phân là 2 giờ, người ta nhận thấy khối lượng cực âm tăng thêm 3,44 g. Nồng độ mol của mỗi muối trong dung dịch ban đầu lần lượt là:
A. 0,1M và 0,2M
B. 0,1M và 0,1M
C. 0,1M và 0,15M
D. 0,15M và 0,2M
Xem lời giải »
Câu 22:
Điện phân dung dịch hỗn hợp chứa Ag2SO4 và CuSO4 một thời gian thấy khối lượng catot tăng lên 4,96g và khí thoát ra ở anot có thể tích là 0,336 lít (đktc). Khối lượng kim loại bám ở catot lần lượt là:
A. 4,32g và 0,64g
B. 3,32g và 0,64g
C. 3,32g và 0,84
D. 4,32 và 1,64
Xem lời giải »
Câu 23:
Điện phân một dung dịch muối MCln với điện cực trơ. Khi ở catot thu được 16g kim loại M thì ở anot thu được 5,6 lít khí (đktc). Kim loại M là:
A. Mg
B. Fe
C. Cu
D. Ca
Xem lời giải »
Câu 24:
Có 400ml dung dịch chứa HCl và KCl đem điện phân trong bình điện phân có vách ngăn với cường độ dòng điện 9,65A trong 20 phút thì dung dịch chứa một chất tan có pH=13 (coi thể tích dung dịch không đổi). Nồng độ mol/lit của HCl và KCl trong dung dịch ban đầu lần lượt bằng:
A. 0,2M và 0,2M
B. 0,1M và 0,2M
C. 0,2M và 0,1M
D. 0,1M và 0,1M
Xem lời giải »
Câu 25:
Điện phân 100ml dung dịch A chứa Cu2+, Na+; H+; SO42- có pH = 1, điện cực trơ. Sau một thời gian điện phân, rút điện cực ra khỏi dung dịch, thấy khối lượng dung dịch giảm 0,64 gam và dung dịch có màu xanh nhạt, thể tích dung dịch không đổi. Tính nồng độ H+ có trong dung dịch sau khi điện phân.
A. 0,2 M
B. 0,1 M.
C. 0,16 M.
D. 0,26 M.
Xem lời giải »
div class="qitem">
Câu 1:
Điện phân dung dịch chứa a mol CuSO4 và b mol NaCl (với điện cực trơ, có màng ngăn xốp). Để dung dịch sau điện phân làm phenolphtalein chuyển sang màu hồng thì điều kiện của a và b là (biết ion SO42- không bị điện phân trong dung dịch)
A. b > 2a
B. b = 2a
C. b < 2a
D. 2b = a
Xem lời giải »
Câu 2:
Mắc nối tiếp hai bình điện phân: bình (1) chứa dung dịch MCl2 và bình (2) chứa dung dịch AgNO3. Sau 3 phút 13 giây thì ở catot bình (1) thu được 1,6 gam kim loại còn ở catot bình (2) thu được 5,4 gam kim loại. Cả hai bình đều không thấy khí ở catot thoát ra. Kim loại M là:
A. Zn
B. Cu
C. Ni
D. Pb
Xem lời giải »
Câu 3:
Hòa tan 50 gam tinh thể CuSO4.5H2O vào 200 ml dung dịch HCl 0,6 M thu được dung dịch X. Đem điện phân dung dịch X (các điện cực trơ) với cường độ dòng điện 1,34A trong 4 giờ. Khối lượng kim loại thoát ra ở catot và thể tích khí thoát ra ở anot (ở đktc) lần lượt là (Biết hiệu suất điện phân là 100 %):
A. 6,4 gam và 1,792 lít
B. 10,8 gam và 1,344 lít
C. 6,4 gam và 2,016 lít
D. 9,6 gam và 1,792 lít
Xem lời giải »
Câu 4:
Điện phân dung dịch Cu(NO3)2 với cường độ dòng điện 9,65A đến khi bắt đầu có khí thoát ra ở catot thì dừng lại. thời gian điện phân là 40 phút. Khối lượng Cu sinh ra ở catot là:
A. 7,68g
B. 8,67g
C. 6,4g
D. 3,2g
Xem lời giải »
Câu 5:
Điện phân dung dịch gồm 7,45 gam KCl và 28,2 gam Cu(NO3)2 (điện cực trơ, màng ngăn xốp) đến khi khối lượng dung dịch giảm đi 10,75 gam thì ngừng điện phân (giả thiết lượng nước bay hơi không đáng kể). Tất cả các chất tan trong dung dịch sau điện phân là
A. KNO3, HNO3 và Cu(NO3)2
B. KNO3, KCl và KOH.
C. KNO3 và Cu(NO3) 2.
D. KNO3 và KOH.
Xem lời giải »
Câu 6:
Điện phân dung dịch hỗn hợp chứa 18,8g Cu(NO3)2 và 29,8g KCl điện cực trơ có màng ngăn.sau một thời gian thấy khối lượng dung dịch giảm 17,15g so với ban đầu, thể tích dung dịch là 400ml. Nồng độ mol lớn nhất của các chất sau điện phân là giá trị nào dưới đây?
A. 1,00 M.
B. 2,00 M
C. 0,25 M
D. 0,50 M
Xem lời giải »
Câu 7:
Điện phân dung dịch A chứa 0,4 mol M(NO3)2 và 1 mol NaNO3 với điện cực trơ trong thời gian 48 phút 15 giây thì thu được 11,52 gam kim loại M bên catot và 2,016 lít khí tại anot. Cho các phát biểu sau:
1. M là Cu.
2. Cường độ dòng điện đã dùng bằng 10 (A).
3. Thời gian điện phân dung dịch mất hết M2+ với cường độ dòng điện 12 (A) là là 48 phút 15 giây.
Trong các phát biểu trên, số phát biểu đúng là?
A. 0
B. 1
C. 2
D. 3
Xem lời giải »
Câu 8:
Hòa tan hoàn toàn 13,00 gam Zn trong dung dịch HNO3 loãng dư thu được dung dịch X và 0,448 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là:
A. 18,90 gam
B. 37,80 gam
C. 39,80 gam
D. 28,35 gam
Xem lời giải »
Câu 9:
Hòa tan 50 gam tinh thể CuSO4.5H2O vào 200 ml dung dịch HCl 0,6 M thu được dung dịch X. Đem điện phân dung dịch X (các điện cực trơ) với cường độ dòng điện 1,34A trong 4 giờ. Khối lượng kim loại thoát ra ở catot và thể tích khí thoát ra ở anot (ở đktc) lần lượt là (Biết hiệu suất điện phân là 100 %):
A. 6,4 gam và 1,792 lít
B. 10,8 gam và 1,344 lít
C. 6,4 gam và 2,016 lít
D. 9,6 gam và 1,792 lít
Xem lời giải »
Câu 10:
Ngâm 1 lá Zn vào dung dịch HCl thấy bọt khí thoát ra ít và chậm. Nếu nhỏ thêm vào vài giọt dung dịch X thì thấy bọt khí thoát ra rất mạnh và nhanh. Chất tan trong dung dịch X là
A. NaOH
B. H2SO4
C. FeSO4
D. MgSO4
Xem lời giải »
Câu 11:
Trong quá trình điện phân dung dịch CuSO4 có điện cực bằng Cu, nhận thấy :
A. Nồng độ Cu2+ trong dung dịch không đổi.
B. nồng độ Cu2+ giảm dần
C. Chỉ nồng độ SO42- thay đổi
D. nồng độ Cu2+ tăng dần
Xem lời giải »
Câu 12:
Khử 16 gam hỗn hợp các oxit kim loại : FeO, Fe2O3, Fe3O4, CuO và PbO bằng khí CO ở nhiệt độ cao, khối lượng chất rắn thu được là 11,2 gam. Tính thể tích khí CO đã tham gia phản ứng (đktc)?
A. 5,6 lit
B. 6,72 lit
C. 13,44 lit
D. 2,24 lit
Xem lời giải »
Câu 13:
Hoà tan hoàn toàn 20,0 gam một oxit kim loại bằng dung dịch H2SO4 loãng thu được 50,0 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là:
A. 2,80 lít.
B. 5,60 lít.
C. 6,72 lít.
D. 8,40 lít.
Xem lời giải »
Câu 14:
Khử 3,48 g một oxit của kim loại M cần dùng 1,344 lít H2(đktc). Toàn bộ lượng kim loại M sinh ra cho tác dụng với dung dịch HCl dư thu được 1,008 lít H2 (đktc). Công thức oxit là :
A. Fe3O4.
B. Fe2O3.
C. FeO.
D. ZnO.
Xem lời giải »
Câu 15:
Hỗn hợp A dạng bột gồm Fe2O3 và Al2O3. Cho khí H2 dư tác dụng hoàn toàn với 14,2 gam hỗn hợp A nung nóng, thu được hỗn hợp chất rắn B. Hòa tan hết hỗn hợp B bằng dung dịch HCl thì thấy thoát ra 2,24(l) khí hiđro ở điều kiện tiêu chuẩn. Phần trăm khối lượng mỗi chất trong hỗn hợp A là:
A. 60% Fe2O3 ; 40% Al2O3
B. 52,48% Fe2O3 ; 47,52% Al2O3.
C. 40% Fe2O3 ; 60% Al2O3
D. 56,34% Fe2O3 ; 43,66% Al2O3
Xem lời giải »
Câu 16:
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m
A. 0,224 lít và 14,48 gam
B. 0,672 lít và 18,46 gam
C. 0,112 lít và 12,28 gam
D. 0,448 lít và 16,48 gam
Xem lời giải »
Câu 17:
Dẫn khí CO dư qua ống đựng bột một oxit sắt (FexOy) ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được 0,84 gam sắt và dẫn khí sinh ra vào nước vôi trong dư thì thu được 2 gam kết tủa. Xác định công thức phân tử của FexOy.
A. FeO
B. Fe2O3
C. Fe3O4
D. Cả 3 đáp án đều sai
Xem lời giải »
Câu 18:
Hòa tan 46g hỗn hợp gồm Ba và 2 kim loại kiềm A, B thuộc 2 chu kì liên tiếp vào nước thu được dd D và 11,2 lít khí (đktc). Nếu thêm 0,18 mol Na2SO4 vào dd D thì sau phản ứng vẫn còn dư ion Ba2+. Nếu thêm 0,21 mol Na2SO4 vào dd D thì sau phản ứng còn dư Na2SO4. Vậy 2 kim loại kiềm là?
A. Li và Na
B. Na và K
C. K và Rb
D. Rb và Cs
Xem lời giải »
Câu 19:
Cho 200 ml dung dịch AlCl3 1,5M tác dụng với V lít dung dịch NaOH 0,5M, thu được 15,6 gam kết tủa. Giá trị lớn nhất của V là
A. 1,2.
B. 1,8.
C. 2,0.
D. 2,4.
Xem lời giải »
Câu 20:
Cho V lít dung dịch NaOH 2M vào dung dịch chứa 0,1 mol Al2(SO4)3 và 0,1 mol H2SO4 đến khi phản ứng hoàn toàn thu được 7,8 gam kết tủa. Giá trị lớn nhất của V để thu được lượng kết tủa trên là
A. 0,45.
B. 0,35.
C. 0,25.
D. 0,15.
Xem lời giải »
Câu 21:
Cho a mol AlCl3 vào 1 lít dung dịch NaOH có nồng độ b M được 0,05 mol kết tủa, thêm tiếp 1 lít dung dịch NaOH trên thì được 0,06 mol kết tủa. Giá trị của a và b lần lượt là
A. 0,15 và 0,06.
B. 0,09 và 0,18.
C. 0,09 và 0,15.
D. 0,06 và 0,15.
Xem lời giải »
Câu 22:
X là dung dịch chứa 0,1 mol AlCl3, Y là dung dịch chứa 0,32 mol NaOH. Thực hiện 2 thí nghiệm sau:
-Thí nghiệm 1: Cho từ từ Y vào X, sau khi cho hết Y vào X được a gam kết tủa.
-Thí nghiệm 2: Cho từ từ X vào Y, sau khi cho hết X vào Y được b gam kết tủa.
Nhận định nào sau đây là đúng?
A. a = b = 3,12.
B. a = b = 6,24.
C. a = 3,12, b = 6,24.
D. a = 6,24, b = 3,12.
Xem lời giải »
Câu 23:
X là dung dịch AlCl3, Y là dung dịch NaOH 2M. Cho 150 ml dung dịch Y vào cốc chứa 100 ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 7,8 gam kết tủa. Thêm tiếp vào cốc 100 ml dung dịch Y, khuấy đều đến khi kết tủa phản ứng thấy trong cốc có 10,92 gam kết tủa. Nồng độ mol của dung dịch X là
A. 3,2M.
B. 2,0M.
C. 1,6M.
D. 1,0M.
Xem lời giải »
Câu 24:
Chia m gam hỗn hợp Na2O và Al2O3 thành 2 phần bằng nhau:
-Phần 1: Hoà tan trong nước dư thu được 1,02 gam chất rắn không tan.
-Phần 2: Hoà tan vừa hết trong 140 ml dung dịch HCl 1M. Giá trị của m là
A. 2,26.
B. 2,66.
C. 5,32.
D. 7,0.
Xem lời giải »
Câu 25:
Hoà tan hết hỗn hợp gồm một kim loại kiềm và một kim loại kiềm thổ trong nước được dung dịch A và có 1,12 lít H2 bay ra (ở đktc). Cho dung dịch chứa 0,03 mol AlCl3 vào dung dịch A. Khối lượng kết tủa thu được là
A. 0,78 gam.
B. 0,81 gam
C. 1,56 gam.
D. 2,34 gam.
Xem lời giải »
Câu 1:
Hòa tan hết 15,0 gam hỗn hợp X gồm và Fe(NO3)2 trong dung dịch chứa và 0,16 mol thu được dung dịch Y và hỗn hợp khí Z gồm và NO (tỉ lệ mol tương ứng 1 : 4). Dung dịch Y hòa tan tối đa 8,64 gam bột Cu, thấy thoát ra 0,03 mol khí NO. Nếu cho dung dịch dư vào Y, thu được 154,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn và khí NO là sản phẩm khử duy nhất của cả quá trình. Phần trăm khối lượng của Fe đơn chất trong hỗn hợp X là:
A. 48,80%
B. 33,60%
C. 37,33%
D. 29,87%
Xem lời giải »
Câu 2:
X là hỗn hợp gồm Mg và MgO (trong đó Mg chiếm 60% khối lượng). Y là dung dịch gồm H2SO4 và NaNO3. Cho 6 gam X tan hoàn toàn vào Y, thu được dung dịch Z (chỉ chứa ba muối trung hòa) và hỗn hợp hai khí (gồm khí NO và 0,04 mol H2). Cho dung dịch BaCl2 dư vào Z, thu được m gam kết tủa. Biết Z có khả năng tác dụng vừa đủ với dung dịch chứa 0,44 mol NaOH. Giá trị của m là
A. 55,92.
B. 25,2.
C. 46,5.
D. 53,6.
Xem lời giải »
Câu 3:
Bảng dưới đây ghi lại hiện tượng khi làm thí nghiệm với các chất sau ở dạng dung dịch nước: X, Y, Z và T:
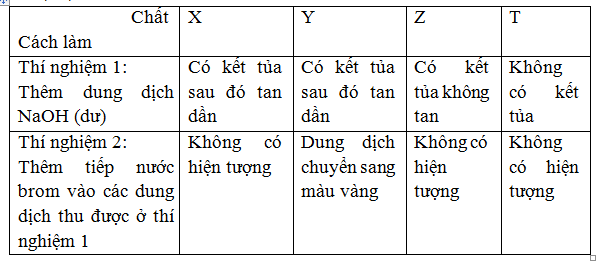
Các chất X, Y, Z và T lần lượt là
A. MgCl2, CrCl3, AlCl3, KCl
B. CrCl3, AlCl3, MgCl2, KCl
C. CrCl3, MgCl2, KCl, AlCl3
D. AlCl3, CrCl3, MgCl2, KCl.
Xem lời giải »
Câu 4:
Hình vẽ sau do một học sinh vẽ để mô tả lại thí nghiệm ăn mòn điện hóa học khi cắm hai lá Cu và Zn (được nối với nhau bằng một dây dẫn) vào dung dịch H2SO4 loãng. Trong hình vẽ bên chi tiết nào chưa đúng?
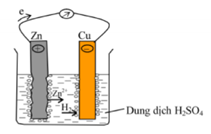
A. Bề mặt hai thanh Cu và Zn.
B. Chiều dịch chuyển của electron trong dây dẫn.
C. Ký hiệu các điện cực.
D. Hiện tượng xảy ra trên điện cực Zn.
Xem lời giải »
Câu 5:
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư.
(b) Sục khí Cl2 vào dung dịch FeCl2.
(c) Dẫn khí H2 dư qua bột CuO nung nóng.
(d) Cho Na vào dunh dịch CuSO4 dư.
(e) Nhiệt phân AgNO3.
(g) Đốt FeS2 trong không khí.
(h) Điện phân dung dịch CuSO4 với điện cực trơ.
Sau khi kết thúc các pahrn ứng, số thí nghiệm thu được kim loại là
A. 5.
B. 3.
C. 4.
D. 2.
Xem lời giải »
Câu 6:
Thực hiện các thí nghiệm sau:
(1) Cho kim loại Fe nguyên chất vào dung dịch CuSO4.
(2) Cho lá kim loại Al nguyên chất vào dung dịch HNO3 đặc, nguội.
(3) Đốt dây kim loại Mg nguyên chất trong khí Cl2.
(4) Cho lá hợp kim Fe – Cu vào dung dịch H2SO4 loãng.
Số thí nghiệm xảy ra phản ứng ăn mòn kim loại là
A. 1
B. 4
C. 2
D. 3.
Xem lời giải »
Câu 7:
Cho các cặp chất với tỉ lệ số mol tương ứng như sau :
(a) Fe3O4 và Cu (1:1)
(b) Na và Zn (1:1)
(c) Zn và Cu (1:1)
(d) Fe2(SO4)3 và Cu (1:1)
(e) FeCl2 và Cu (2:1)
(g) FeCl3 và Cu (1:1)
Số cặp chất tan hoàn toàn trong một lượng dư dung dịch HCl loãng nóng là
A. 2
B. 5
C. 3
D. 4
Xem lời giải »
Câu 8:
Cho 24,3 gam bột Al vào 225 ml dung dịch hỗn hợp NaNO3 1M và NaOH 3M khuấy đều cho đến khi khí ngừng thoát ra thì dừng lại và thu được V lít khí (ở đktc).Giá trị của V là:
A. 11,76 lít
B. 9,072 lít
C. 13,44 lít
D. 15,12 lít
Xem lời giải »
Câu 9:
Hòa tan 12,8 gam bột Cu trong 200 ml dung dịch hỗn hợp KNO3 0,5M và H2SO4 1M. Thể tích khí NO (sản phẩm khử duy nhất) thoát ra ở đktc là
A. 2,24 lít.
B. 2,99 lít.
C. 4,48 lít.
D. 11,2 lít.
Xem lời giải »
Câu 10:
Hòa tan m gam bột Al vào lượng dư dung dịch hỗn hợp của NaOH và NaNO3 thấy xuất hiện 6,72 lít (đkc) hỗn hợp khí NH3 và H2 với số mol bằng nhau. Khối lượng m bằng:
A. 6,72 gam.
B. 7,59 gam.
C. 8,10 gam.
D. 13,50 gam.
Xem lời giải »
Câu 11:
Cho hỗn hợp gồm 1,12 gam Fe và 1,92 gam Cu vào 400 ml dung dịch chứa hỗn hợp gồm H2SO4 0,5M và NaNO3 0,2M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho V ml dung dịch NaOH 1M vào dung dịch X thì lượng kết tủa thu được là lớn nhất. Giá trị tối thiểu của V là:
A. 360 ml
B. 240 ml
C. 400 ml
D. 120 ml
Xem lời giải »
Câu 12:
Đem điện phân 200ml dung dịch NaCl 2M (d = 1,1g/ml) với điện cực bằng than có màng ngăn xốp và dung dịch luôn luôn được khuấy đều. Khí ở catot thoát ra 22,4 lít khí đo ở điều kiện tiêu chuẩn thì ngừng điện phân. Cho biết nồng độ phần trăm của dung dịch NaOH sau điện phân:
A. 8,38 %
B. 54,42%
C. 16,64%
D. 8,32%
Xem lời giải »
Câu 13:
Tiến hành điện phân (với điện cực Pt) 200 gam dung dịch NaOH 10% đến khi dung dịch NaOH trong bình có nồng độ 25 % thì ngừng điện phân. Thể tích khí (ở đktc) thoát ra ở anot và catot lần lượt là:
A. 149,3 lít và 74,7 lít
B. 156,8 lít và 78,4 lít
C. 78,4 lít và 156,8 lít
D. 74,7 lít và 149,3 lít
Xem lời giải »
Câu 14:
Sau một thời gian điện phân 200 ml dung dịch CuSO4 (d = 1,25 g/ml) với điện cực graphit (than chì) thấy khối lượng dung dịch giảm 8 gam. Để làm kết tủa hết ion Cu2+ còn lại trong dung dịch sau điện phân cần dùng 100 ml dung dịch H2S 0,5 M. Nồng độ phần trăm của dung dịch CuSO4 ban đầu là:
A. 12,8 %
B. 9,6 %
C. 10,6 %
D. 11,8 %
Xem lời giải »
Câu 15:
Điện phân hòa toàn 2,22 gam muối clorua kim loại ở trạng thái nóng chảy thu được 448 ml khí (ở đktc) ở anot. Kim loại trong muối là:
A. Na
B. Ca
C.K
D. Mg
Xem lời giải »
Câu 16:
Cho các phát biểu sau :
(a) Kim loại kiềm là những nguyên tố nhóm s
(b) Các kim loại kiềm có cấu trúc mạng tinh thể lập phương tâm khối.
(c) Các kim loại kiềm mềm do liên kết kim loại trong tinh thể yếu
(d) Ứng dụng kim loại xexi dùng làm tế bào quang điện
(e) Phương pháp thường dùng để điều chế kim loại kiềm là điện phân nóng chảy muối halogenua của kim loại kiềm.
Số phát biểu đúng là :
A. 5
B. 2
C. 4
D. 3
Xem lời giải »
Câu 17:
So sánh độ dẫn điện của hai dây dẫn bằng đồng tinh khiết, có khối lượng bằng nhau. Dây thứ nhất chỉ có một sợi. Dây thứ hai gồm một bó hàng trăm sợi nhỏ. Độ dẫn điện của hai dây dẫn là
A. không so sánh được.
B. dây thứ hai dẫn điện tốt hơn.
C. dây thứ nhất dẫn điện tốt hơn.
D. bằng nhau.
Xem lời giải »
Câu 18:
Kim loại nào sau đây phản ứng được với cả hai dung dịch là dung dịch FeSO4 và dung dịch H2SO4 đặc, nguội?
A. Na.
B. Al.
C. Fe.
D. Cu.
Xem lời giải »
Câu 19:
Cho các phát biểu sau:
(1) Các oxit của kim loại kiềm phản ứng với CO tạo thành kim loại.
(2) Các kim loại Ag, Fe, Cu và Mg đều được điều chế được bằng phương pháp điện phân dung dịch.
(3) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(4) Cho Cu vào dung dịch FeCl3 dư, thu được dung dịch chứa 3 muối.
Số phát biểu đúng là
A. 4.
B. 1.
C. 3.
D. 2.
Xem lời giải »
Câu 20:
Dẫn khí CO (dư) đi qua hỗn hợp gồm Al2O3, FeO, CuO ở nhiệt độ cao đến phản ứng hoàn toàn thu được chất rắn X. Để hòa tan hết X có thể dùng dung dịch (loãng, dư) nào sau đây?
A. NaOH.
B. Fe2(SO4)3.
C. H2SO4.
D. HNO3.
Xem lời giải »
Câu 21:
Khi không có không khí, hai kim loại nào sau đây đều tác dụng với HCl trong dung dịch theo cùng tỉ lệ số mol?
A. Na và Mg.
B. Fe và Al.
C. Na và Zn
D. Fe và Mg.
Xem lời giải »
Câu 22:
Điện phân dung dịch NaCl có màng ngăn. Nhận xét nào sau đây là đúng?
A. Ở catot xảy ra sự khử ion kim loại Natri.
B. Ở anot xảy ra sự oxi hóa H2O.
C. Ở anot sinh ra khí H2.
D. Ở catot xảy ra sự khử nước.
Xem lời giải »
Câu 23:
Cho các phát biểu sau
(1) Các kim loại Fe, Ni, Zn đều có thể điều chế bằng phương pháp điện phân dung dịch muối của nó.
(2) Trong dung dịch Na, Fe đều khử được AgNO3 thành Ag.
(3) Cho Fe vào dung dịch FeCl3 dư sau phản ứng thu được dung dịch chứa hai muối.
(4) Hỗn hợp Na và Al có thể tan hoàn toàn trong nước.
(5) Tính oxi hóa của Ag+ > Fe3+ > Cu2+ > Fe2+.
Tổng số phát biểu đúng là
A. 2.
B. 3.
C. 4.
D. 5.
Xem lời giải »
Câu 24:
Cho thứ tự trong dãy điện hóa của một cặp oxi hóa- khử như sau Al3+/Al; Zn2+/Zn; Fe2+/Fe; Pb2+/Pb; Ag+/Ag. Phát biểu nào sau đây là đúng ?
A. Nguyên tử Pb có thể khử Zn2+ trong dung dịch.
B. Nguyên tử Ag có thể khử Zn2+ trong dung dịch.
C. Nguyên tử Fe có thể khử Zn2+ trong dung dịch.
D. Nguyên tử Al có thể khử Zn2+ trong dung dịch.
Xem lời giải »
Câu 25:
Có 5 kim loại là Mg, Ba, Zn, Fe, Ag. Chỉ dùng thêm dung dịch H2SO4 loãng thì có thể nhận biết được các kim loại
A. Mg, Ba, Zn, Fe
B. Mg, Ba, Zn, Fe, Ag
C. Mg, Ba, Zn
D. Mg, Ba, Cu
Xem lời giải »
Câu 1:
Công thức chung của oxit kim loại thuộc nhóm IIA là
A. R2O3
B. RO2
C. R2O
D. RO
Xem lời giải »
Câu 2:
Nguyên tử Fe có cấu hình e là
A. [Ar ] 3d6 4s2
B. [Ar ] 4s13d7
C. [Ar ]3d7 4s1
D. [Ar ] 4s23d6
Xem lời giải »
Câu 3:
Cấu hình e của Cr là
A. [Ar ] 3d4 4s2
B. [Ar ] 4s23d4
C. [Ar ] 3d5 4s1
D. [Ar ] 4s13d5
Xem lời giải »
Câu 4:
Kim loại Ni phản ứng được với tất cả các muối trong dung dịch ở dãy nào sau đây ?
A. NaCl, AlCl3, ZnCl2
B. MgSO4, CuSO4, AgNO3
C. Pb(NO3)2 , AgNO3, NaCl
D. AgNO3, CuSO4, Pb(NO3)2
Xem lời giải »
Câu 5:
Cho ba kim loại là Al, Fe, Cu và bốn dung dịch muối riêng biệt là ZnSO4, AgNO3, CuCl2, MgSO4. Kim loại nào tác dụng được với cả bốn dung dịch muối đã cho ?
A. Al
B. Fe
C. Cu
D. Không kim loại
Xem lời giải »
Câu 6:
Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3 và MgO (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm :
A. Cu, Al, Mg
B. Cu, Al, MgO
C. Cu, Al2O3, Mg
D. Cu, Al2O3, MgO
Xem lời giải »
Câu 7:
Nguyên tử kim loại khi tham gia phản ứng hoá học có tính chất nào sau đây ?
A. Nhường electron và tạo thành ion âm
B. Nhường electron và tạo thành ion dương
C. Nhận electron để trở thành ion âm
D. Nhận electron để trở thành ion dương
Xem lời giải »
Câu 8:
Cặp chất không xảy ra phản ứng là
A. Fe + Cu(NO3)2
B. Cu + AgNO3
C. Zn + Fe(NO3)2
D. Ag + Cu(NO3)2
Xem lời giải »
Câu 9:
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường bazơ là:
A. Na, Ba, K
B. Be, Na, Ca
C. Na, Fe, K
D. Na, Cr, K
Xem lời giải »
Câu 10:
Để loại bỏ kim loại Cu ra khỏi hỗn hợp bột gồm Ag và Cu, người ta ngâm hỗn hợp kim loại trên vào lượng dư dung dịch
A. AgNO3
B. HNO3
C. Cu(NO3)2
D. Fe(NO3)2
Xem lời giải »
Câu 11:
Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên chủ yếu bởi
A. cấu tạo mạng tinh thể của kim loại
B. khối lượng riêng của kim loại
C. các electron độc thân trong tinh thể kim loại
D. các electron tự do trong tinh thể kim loại
Xem lời giải »
Câu 12:
So với nguyên tử phi kim cùng chu kì, nguyên tử kim loại
A. thường có bán kính nguyên tử nhỏ hơn
B. thường có năng lượng ion hoá nhỏ hơn
C. thường dễ nhận electron trong các phản ứng hoá học
D. thường có số electron ở các phân lớp ngoài cùng nhiều hơn
Xem lời giải »
Câu 13:
Kim loại nào sau đây có tính dẫn điện tốt nhất trong tất cả các kim loại ?
A. Vàng
B. Bạc
C. Đồng
D. Nhôm
Xem lời giải »
Câu 14:
Kim loại nào sau đây dẻo nhất trong tất cả các kim loại ?
A. Vàng
B. Bạc
C. Đồng
D. Nhôm
Xem lời giải »
Câu 15:
Kim loại nào sau đây có độ cứng lớn nhất trong tất cả các kim loại ?
A. Vonfam
B. Crom
C. Sắt
D. Đồng
Xem lời giải »
Câu 16:
Kim loại nào sau đây là kim loại mềm nhất trong tất cả các kim loại ?
A. Liti
B. Xesi
C. Natri
D. Kali
Xem lời giải »
Câu 17:
Kim loại có nhiệt độ nóng chảy cao nhất trong tất cả các kim loại ?
A. Vonfam
B. Đồng
C. Sắt
D. Kẽm
Xem lời giải »
Câu 18:
Kim loại nào sau đây nhẹ nhất (có khối lượng riêng nhỏ nhất) trong tất cả các kim loại
A. Liti
B. Rubidi
C. Natri
D. Kali
Xem lời giải »
Câu 19:
Bao nhiêu gam clo tác dụng vừa đủ kim loại nhôm tạo ra 26,7 gam AlCl3?
A. 21,3 gam
B. 12,3 gam
C. 13,2 gam
D. 23,1 gam
Xem lời giải »
Câu 20:
Một thanh kim loại M hóa trị 2 được nhúng vào trong 1 lít dung dịch CuSO4 0,5M. Sau khi lấy thanh M ra và cân lại ,thấy khối lượng thanh tăng 1,6 gam, nồng độ CuSO4 còn 0,3M. Hãy xác định kim loại M?
A. Fe
B. Mg
C. Zn
D. Pb
Xem lời giải »
Câu 1:
Ngâm một lá kẽm trong 100ml dung dịch AgNO3 0,1 mol. Kết thúc phản ứng, khối lượng lá kẽm tăng a gam. Giá trị a là?
A. 0,655g
B. 0,75g
C. 0,65g
D. 0,755g
Xem lời giải »
Câu 2:
Cho 8,4 g Fe vào dung dịch có chứa 0,4mol AgNO3. Kết thúc phản ứng, khối lượng bạc là bao nhiêu?
A. 42,3g
B. 23,4g
C. 43,2g
D. 21,6g
Xem lời giải »
Câu 3:
Cho biết các cặp oxi hoá- khử sau :
Fe2+/ Fe Cu2+/ Cu Fe3+/Fe2+
Tính oxi hoá tăng dần theo thứ tự
A. Cu2+, Fe2+, Fe3+
B. Cu2+, Fe3+,Fe2+
C. Fe3+,Cu2+, Fe2+
D. Fe2+ ,Cu2+, Fe3+
Xem lời giải »
Câu 4:
Muốn khử dd chứa Fe3+ thành dd có chứa Fe2+ cần dùng kim loại sau:
A. Cu
B. Na
C. Zn
D. Ag
Xem lời giải »
Câu 5:
Cho các kim loại: Fe , Al , Mg , Cu , Zn , Ag. Số kim loại tác dụng được với dd H2SO4 loãng là:
A. 5
B. 3
C. 6
D. 4
Xem lời giải »
Câu 6:
Ngâm Cu dư vào dd AgNO3 thu được dd X, sau đó ngâm Fe dư vào dung dịch X thu được dung dịch Y. dung dịch Y gồm:
A. Fe(NO3)2
B. Fe(NO3)2 , Cu(NO3)2 , AgNO3
C. Fe(NO3)2 , Cu(NO3)2
D. Fe(NO3)3
Xem lời giải »
Câu 7:
Ngâm đinh sắt sạch trong 200 ml dd CuSO4. Sau phản ứng kết thúc lấy đinh sắt ra rửa nhẹ và làm khô thấy khối lượng đinh sắt tăng 8 gam. Nồng độ CuSO4 ban đầu là:
A. 0,52 M
B. 0,5 M
C. 5 M
D. 0,25 M
Xem lời giải »
Câu 8:
Cho 4 dung dịch muối: CuSO4, K2SO4, NaCl, KNO3. Dung dịch nào sau khi điện phân cho ra một dung dịch axit (điện cực trơ).
A. CuSO4
B. K2SO4
C. NaCl
D. KNO3
Xem lời giải »
Câu 9:
Cho các kim loại sau: K, Ba, Cu và Ag. Số kim loại điều chế được bằng phương pháp điện phân dung dịch (điện cực trơ) là:
A. 3
B. 1
C. 2
D. 4
Xem lời giải »
Câu 10:
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A. Fe
B. Cu
C. Mg
D. Ag
Xem lời giải »
Câu 11:
Trong quá trình điện phân, các muối X- (X: Cl-, Br-) di chuyển về:
A. Cực dương và bị oxi hóa
B. Cực âm và bị oxi hóa
C. Cực dương và bị khử
D. Cực âm và bị khử
Xem lời giải »
Câu 12:
Cho dung dịch chứa các ion: Na+, K+, Cu+, Cl-, SO42-, NO3-. Các ion nào không bị điện phân khi ở trạng thái dung dịch:
A. Na+, K+, Cl-, SO42-
B. K+, Cu+, Cl-, NO3-
C. Na+, Cu+, Cl-, SO42-
D. Na+, K+, SO42-, NO3-
Xem lời giải »
Câu 13:
Điện phân một lượng dư dung dịch MgCl2 (điện cực trơ, có màng ngăn xốp bao điện cực) với cường độ dòng điện 2,68A trong 2 giờ. Sau khi dừng điện phân khối lượng dung dịch giảm m gam, giả thiết nước không bay hơi, các chất tách ra đều khan. Giá trị của m là:
A. 8,7
B. 18,9
C. 7,3
D. 13,1.
Xem lời giải »
Câu 14:
Điện phân nóng chảy hoàn toàn 1,9g muối clorua của kim loại M được 0,48g kim loại M ở catot. Kim loại M là:
A. Zn
B. Ca
C. Mg
D. Ba
Xem lời giải »
Câu 15:
Điện phân một dd muối MCln với điện cực trơ. Khi ở catot thu được 16g kim loại M thì ở anot thu được 5,6 lít khí (đktc). Kim loại M là:
A. Mg
B. Fe
C. Cu
D. Ca
Xem lời giải »
Câu 16:
Nếu muốn điện phân hoàn toàn (mất màu xanh) 400 ml dung dịch CuSO4 0,5M với cường độ dòng điện I = 1,34A (hiệu suất điện phân là 100%) thì cần bao nhiêu thời gian.
A. 6 giờ
B. 7 giờ
C. 8 giờ
D. 9 giờ
Xem lời giải »
Câu 17:
Điện phân dung dịch muối CuSO4 dư trong thời gian 1930 giây, thu được 1,92 gam Cu ở catot. Cường độ dòng điện trong quá trình điện phân là giá trị nào dưới đây:
A. 3A
B. 4,5A
C. 1,5A
D. 6A
Xem lời giải »
Câu 18:
Điện phân hòa toàn 2,22 gam muối clorua kim loại ở trạng thái nóng chảy thu được 448 ml khí (ở đktc) ở anot. Kim loại trong muối là:
A. Na
B. Ca
C. K
D. Mg
Xem lời giải »
Câu 19:
Điện phân 250g dd CuSO4 8% đến khi nồng độ CuSO4 trong dd thu được giảm đi và bằng một nửa so với trước phản ứng thì dừng lại. Khối lượng kim bám ở catot gần với giá trị nào?
A. 4,08g
B. 2,04g
C. 4,58g
D. 4,5g
Xem lời giải »
Câu 20:
Điện phân dung dịch CuCl2, điện cực trơ bằng dòng điện 5A trong 45 phút 20 giây. Tính khối lượng kim loại sinh ra ở Catot .
A. 4,512g
B. 4,5g
C. 4,6g
D. 4,679g
Xem lời giải »
Câu 1:
Biết rằng ion Pb2+ trong dung dịch oxi hóa được Sn. Khi nhúng hai thanh kim loại Pb và Sn được nối với nhau bằng dây dẫn điện vào một dung dịch chất điện li thì
A. Cả Pb và Sn đều bị ăn mòn điện hóa
B. Cả Pb và Sn đều không bị ăn mòn điện hóa
C. Chỉ có Pb bị ăn mòn điện hóa
D. Chỉ có Sn bị ăn mòn điện hóa
Xem lời giải »
Câu 2:
Có 4 dung dịch riêng biệt: CuSO4, ZnCl2, FeCl3, AgNO3. Nhúng vào mỗi dung dịch một thanh Ni. Số trường hợp xuất hiện ăn mòn điện hoá là
A. 2
B. 3
C. 4
D. 1
Xem lời giải »
Câu 3:
Trường hợp nào dưới đây, kim loại không bị ăn mòn điện hóa?
A. Đốt Al trong khí Cl2
B. Để gang ở ngoài không khí ẩm
C. Vỏ tàu làm bằng thép neo đậu ngoài bờ biển
D. Fe và Cu tiếp xúc trực tiếp cho vào dung dịch HCl
Xem lời giải »
Câu 4:
Tiến hành các thí nghiệm sau:
(a) Cho lá Fe vào dung dịch gồm CuSO4 và H2SO4 loãng;
(b) Đốt dây Fe trong bình đựng khí O2;
(c) Cho lá Cu vào dung dịch gồm Fe(NO3)3 và HNO3;
(d) Cho lá Zn vào dung dịch HCl;
Số thí nghiệm có xảy ra ăn mòn điện hóa là
A. 3
B. 2
C. 1
D. 4
Xem lời giải »
Câu 5:
Phát biểu nào dưới đây không đúng?
A. Nguyên tắc chung để điều chế kim loại là khử ion kim loại thành nguyên tử kim loại.
B. Bản chất của ăn mòn kim loại là quá trình oxi hóa - khử
C. Tính chất hóa học đặc trưng của kim loại là tính khử
D. Ăn mòn hóa học phát sinh dòng điện
Xem lời giải »
Câu 6:
Tiến hành các thí nghiệm sau:
a. Cho lá Zn vào dung dịch gồm CuSO4 và H2SO4 loãng;
b. Đốt dây Cu trong bình đựng khí O2;
c. Cho lá Cu vào dung dịch Fe(NO3)2;
d. Cho lá Fe vào dung dịch HCl;
Số thí nghiệm có xảy ra ăn mòn điện hóa là
A. 3
B. 2
C. 1
D. 4
Xem lời giải »
Câu 7:
Trường hợp nào sau đây kim loại bị ăn mòn điện hoá học?
A. Cho kim loại Zn nguyên chất vào dung dịch HCl
B. Cho kim loại Cu nguyên chất vào trong dung dịch HNO3 loãng
C. Thép cacbon để trong không khí ẩm
D. Đốt dây sắt nguyên chất trong khí O2
Xem lời giải »
Câu 8:
Khi vật bằng gang, thép bị ăn mòn điện hóa trong không khí ẩm, nhận định nào sau đây là nhận định đúng:
A. Tinh thể cacbon là cực âm xảy ra quá trình oxi hóa
B. Tinh thể cacbon là cực dương, xảy ra quá trình oxi hóa
C. Tinh thể sắt cực dương xảy ra quá trình khử
D. Tinh thể sắt là cực âm xảy ra quá trình oxi hóa
Xem lời giải »
Câu 9:
Tiến hành các thí nghiệm sau:
- Ngâm một lá đồng trong dung dịch AgNO3.
- Ngâm một lá kẽm trong dung dịch HCl loãng.
- Ngâm một lá nhôm trong dung dịch NaOH.
- Ngâm ngập một đinh sắt được quấn một đoạn dây đồng trong dung dịch NaCl.
- Để một vật bằng gang ngoài không khí ẩm.
- Ngâm một miếng đồng vào dung dịch Fe2(SO4)3.
Số thí nghiệm xảy ra ăn mòn điện hóa là
A. 4
B. 2
C. 3
D. 1
Xem lời giải »
Câu 10:
Thực hiện các thí nghiệm sau:
(1) Thả một viên Fe vào dung dịch HCl.
(2) Thả một viên Fe vào dung dịch Cu(NO3)2.
(3) Thả một viên Fe vào dung dịch FeCl3.
(4) Nối một dây Ni với một dây Fe rồi để trong không khí ẩm.
(5) Đốt một dây Fe trong bình kín chứa đầy khí .
(6) Thả một viên Fe vào dung dịch chứa đồng thời CuSO4 và H2SO4 loãng.
Trong các thí nghiệm trên thì thí nghiệm mà Fe không bị ăn mòn điện hóa học là
A. (2), (3), (4), (6)
B. (1), (3), (4), (5)
C. (2), (4), (6)
D. (1), (3), (5)
Xem lời giải »
Câu 11:
Trường hợp nào sau đây, kim loại bị ăn mòn điện hóa học?
A. Đốt dây sắt trong khí oxi khô
B. Kim loại sắt trong dung dịch HNO3 loãng
C. Kim loại kẽm trong dung dịch HCl
D. Thép cacbon để trong không khí ẩm
Xem lời giải »
Câu 12:
Ngâm một lá Zn tinh khiết trong dung dịch HCl, sau đó thêm vài giọt dung dịch CuSO4 vào. Trong quá trình thí nghiệm trên
A. chỉ xảy ra hiện tượng ăn mòn điện hóa học
B. lúc đầu xảy ra hiện tượng ăn mòn điện hóa học sau đó xảy ra thêm hiện tượng ăn mòn hóa học
C. lúc đầu xảy ra hiện tượng ăn mòn hóa học sau đó xảy ra thêm hiện tượng ăn mòn điện hóa học
D. Chỉ xảy ra hiện tượng ăn mòn hóa học
Xem lời giải »
Câu 13:
Tiến hành các thí nghiệm sau:
- TN 1: Cho hơi nước đi qua ống đựng bột sắt nung nóng.
- TN 2: Cho đinh sắt nguyên chất vào dung dịch H2SO4 loãng có nhỏ thêm vài giọt dung dịch CuSO4.
- TN 3: Cho từng giọt dung dịch Fe(NO3)2 vào dung dịch AgNO3.
- TN 4: Để thanh thép (hợp kim của sắt với cacbon) trong không khí ẩm.
- TN 5: Nhúng lá kẽm nguyên chất vào dung dịch CuSO4.
Số trường hợp xảy ra ăn mòn điện hoá học là:
A. 3
B. 4
C. 1
D. 2
Xem lời giải »
Câu 14:
Nếu vật làm bằng hợp kim Fe-Zn bị ăn mòn điện hoá thì trong quá trình ăn mòn
A. sắt đóng vai trò anot và bị oxi hoá
B. kẽm đóng vai trò anot và bị oxi hoá
C. sắt đóng vai trò catot và ion H+ bị oxi hóa
D. kẽm đóng vai trò catot và bị oxi hóa
Xem lời giải »
Câu 15:
Trường hợp nào sau đây xảy ra ăn mòn điện hoá?
A. Sợi dây bạc nhúng trong dung dịch HNO3
B. Đốt lá sắt trong khí Cl2
C. Thanh nhôm nhúng trong dung dịch H2SO4 loãng
D. Thanh kẽm nhúng trong dung dịch CuSO4
Xem lời giải »
Câu 16:
Tiến hành các thí nghiệm sau đây:
(a) Ngâm một lá kẽm vào dung dịch CuSO4.
(b) Ngâm một lá đồng vào dung dịch FeCl3.
(c) Cho thép cacbon tiếp xúc với nước mưa.
(d) Cho thép vào dung dịch axit clohiđric.
(e) Để sắt tây tiếp xúc với nước tự nhiên.
Trong các thí nghiệm trên có bao nhiêu trường hợp xảy ra ăn mòn điện hóa?
A. 2
B. 5
C. 3
D. 4
Xem lời giải »
Câu 17:
Phương pháp thích hợp điều chế kim loại Mg từ MgCl2 là
A. điện phân dung dịch MgCl2
B. điện phân MgCl2nóng chảy
C. nhiệt phân MgCl2
D. dùng K khử Mg2+trong dung dịch MgCl2
Xem lời giải »
Câu 18:
Hai kim loại có thể điều chế bằng phương pháp nhiệt luyện là
A. Ca và Fe
B. Mg và Zn
C. Na và Cu
D. Fe và Cu
Xem lời giải »
Câu 19:
“Ăn mòn kim loại” là sự phá huỷ kim loại do:
A. Tác dụng hoá học của môi trường xung quanh
B. Kim loại tác dụng với dung dịch chất điện ly tạo nên dòng diện
C. Kim loại phản ứng hoá học với chất khí hoặc hơi nước ở nhiệt độ cao
D. Tác động cơ học
Xem lời giải »
Câu 20:
Để chống ăn mòn cho đường ống dẫn dầu bằng thép chôn dưới đất, người ta dùng phương pháp điện hoá. Trong thực tế, người ta dùng kim loại nào sau đây làm điện cực hi sinh?
A. Zn
B. Sn
C. Cu
D. Na
Xem lời giải »
Câu 1:
Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Pb; Fe và Zn; Fe và Sn; Fe và Ni. Khi nhúng các cặp kim loại trên vào dung dịch axit, số cặp kim loại trong đó Fe bị phá huỷ trước là
A. 1
B. 3
C. 2
D. 4
Xem lời giải »
Câu 2:
Kim loại M bị ăn mòn điện hoá học khi tiếp xúc với sắt trong không khí ẩm. M có thể là
A. Bạc
B. Đồng
C. Chì
D. Kẽm
Xem lời giải »
Câu 3:
Trường hợp xảy ra ăn mòn điện hóa là
A. Nhúng thanh Fe vào dung dịch chứa hỗn hợp H2SO4 loãng và lượng nhỏ CuSO4
B. Nhúng thanh Fe vào dung dịch hỗn hợp Fe2(SO4)3 và H2SO4 loãng
C. Nhúng thanh Fe vào dung dịch Fe2(SO4)3
D. Nhúng thanh Fe vào dung dịch H2SO4 loãng
Xem lời giải »
Câu 4:
Kim loại nào sau đây có tính khử mạnh nhất?
A. Fe
B. K
C. Mg
D. Al
Xem lời giải »
Câu 5:
Cho các nửa phản ứng:
Số nửa phản ứng xảy ra ở catot trong quá trình điện phân là:
A. 4
B. 5
C. 6
D. 3
Xem lời giải »
Câu 6:
Ở nhiệt độ cao, khí CO khử được các oxit nào sau đây:
A. Fe2O3 và CuO
B. Al2O3 và CuO
C. MgO và Fe2O3
D. CaO và MgO
Xem lời giải »
Câu 7:
Điện phân dung dịch chứa HCl, NaCl, FeCl3 (điện cực trơ, có màng ngăn). Đồ thị nào sau đây biểu diễn đúng sự biến thiên pH của dung dịch theo thời gian (bỏ qua sự thuỷ phân của muối)?
A. 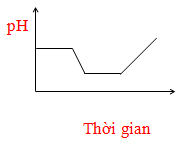
B. 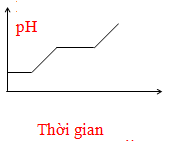
C. 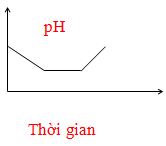
D. 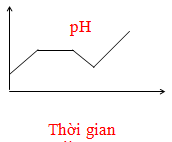
Xem lời giải »
Câu 8:
Cho 2,24 lit đktc khí CO đi từ từ qua một ống sứ nung nóng chứa m gam hỗn hợp MgO, Fe2O3, CuO. Sau phản ứng thu được (m - 0,8) gam chất rắn và hỗn hợp khí X. Tính tỷ khối hơi của X so với H2.
A. 14
B. 18
C. 12
D. 24
Xem lời giải »
Câu 9:
Điện phân (điện cực trơ) dung dịch X chứa 0,2 mol CuSO4; 0,12 mol Fe2(SO4)3 và 0,44 mol NaCl bằng dòng điện có cường độ 2 ampe. Thể tích khí (đktc) thoát ra ở anoot sau 26055 giây điện phân là:
A. 5,936 lít
B. 9,856 lít
C. 5,488 lit
D. 4,928 lit
Xem lời giải »
Câu 10:
Cho Fe phản ứng với dd HNO3 đặc, nóng thu được một chất khí màu nâu đỏ. Chất khí đó là:
A. N2
B. NH3
C. NO2
D. N2O
Xem lời giải »
Câu 11:
Có thể dùng axit nào sau đây để hòa tan hoàn toàn hỗn hợp gồm: Al, Fe, Cu, Ag?
A. HCl
B. HNO3 loãng
C. H2SO4 loãng
D. H2SO4 đặc nguội
Xem lời giải »
Câu 12:
Cho sơ đồ sau:
Số phương trình phản ứng oxi hóa - khử trong dãy là:
A. 3
B. 4
C. 5
D. 6
Xem lời giải »
Câu 13:
Phương trình phản ứng nào sau đây viết sai?
A.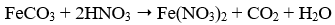
B. 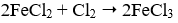
C. 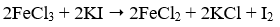
D. 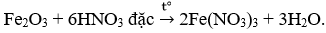
Xem lời giải »
Câu 14:
Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng dư chất nào sau đây?
A. Mg
B. Cu
C. Ba
D. Na
Xem lời giải »
Câu 15:
Nguyên tử 23Z có cấu hình e là: 1s22s22p63s1. Z có
A. 11 nơtron, 12 proton
B. 11 proton, 12 nơtron
C. 13 proton, 10 nơtron
D. 11 proton, 12 electron
Xem lời giải »
Câu 16:
Cho sơ đồ chuyển hóa sau:
Công thức của X, Y, Z lần lượt là:
A. Cl2, AgNO3, MgCO3
B. Cl2, HNO3, CO2
C. HCl, HNO3, NaNO3
D. HCl, AgNO3, (NH4)2CO3
Xem lời giải »
Câu 17:
Cho sơ đồ sau:
FeS2 → X → Y → Z → Fe
Các chất X, Y, Z lần lượt là:
A. FeS, Fe2O3, FeO
B. Fe3O4, Fe2O3, FeO
C. Fe2O3, Fe3O4, FeO
D. FeO, Fe3O4, Fe2O3
Xem lời giải »
Câu 18:
Có thể dùng dung dịch muối nào sau đây để hòa tan hoàn toàn hỗn hợp gồm: Al, Fe, Pb, Cu?
A. Cu(NO3)2
B. Pb(NO3)2
C. AgNO3
D. Al(NO3)3
Xem lời giải »
Câu 19:
Chất nào sau đây có thể oxi hóa Zn thành Zn2+?
A. Fe
B. Ag+
C. Al3+
D. Ca2+
Xem lời giải »
Câu 20:
Nung nóng từng cặp chất sau trong bình kín:
(1) H2(k) + CuO(r) ;
(2) C (r) + KClO3;
(3) Fe (r) + O2 (r)
(4) Mg(r) + SO2(k);
(5) Cl2 (k) + O2(k);
(6) K2O ( r ) + CO2(k)
Số trường hợp có phản ứng hóa học xảy ra là:
A. 4
B. 2
C. 3
D. 5
Xem lời giải »





