Lý thuyết Hóa học 8 Chương 5 hay, chi tiết
Lý thuyết Hóa học 8 Chương 5 hay, chi tiết
Haylamdo biên soạn và sưu tầm tóm tắt Lý thuyết Hóa học 8 Chương 5 hay, chi tiết nhất sẽ tóm tắt kiến thức trọng tâm bài học từ đó giúp học sinh ôn tập để nắm vững kiến thức môn Hóa 8.

Lý thuyết Hóa học 8 Bài 31: Tính chất - Ứng dụng của hiđro
- Kí hiệu: H. Nguyên tử khối: 1
- Công thức hóa học của đơn chất: H2. Phân tử khối: 2
1. Tính chất vật lý:
Là chất khí không màu, không mùi, không vị, nhẹ nhất trong các khí, tan rất ít trong nước
2. Tính chất hóa học
a. Tác dụng với oxi
Nếu đốt cháy hidro trong oxi: hidro cháy mạnh, trên thành lọ xuất hiện những giọt nước nhỏ
PTHH: 2H2 + O2 −to→ 2H2O
Hỗn hợp sẽ gây nổ nếu trộng hidro và oxi theo tỉ lệ thể tích 2:1
b. Tác dụng với đồng oxit CuO
Khi đốt nóng tới khoảng 400°C : bột CuO màu đen chuyển thành lớp kim loại đồng màu đỏ gạch và có những giọt nước tạo thành trên thành cốc
PTHH: H2 + CuO −to→ Cu +H2O
⇒ Hidro đã chiến oxi trong CuO. Vậy hidro có tính khử
⇒ở nhiệt độ thích hợp, hidro có thể kết hợp với nguyên tố oxi trong một số oxit kim loại. do vậy hidro có tính khử. Các phản ứng này đều tỏa nhiệt
3. Ứng dụng
Do tính chất nhẹ, tính khử và khih cháy tỏa nhiềt nhiệt mà hidro ứng dụng trong đời sống
- làm nguyên liệu cho động cơ tên lửa, nhiên liệu cho động cơ ô tô thay cho xăng
- làm nguyên liệu điều chế axit
- dùng để điều chế kim loại từ oxit của chúng
- bơm vào khinh khí cầu, bóng thám
Lý thuyết Hóa học 8 Bài 32: Phản ứng oxi hóa - khử
1. Sự khử. Sự ôxi hóa
Sự khử là sự tách oxi khỏi một chất
Sự oxi hóa là sự tác dụng của oxi với một chất
VD: 3H2 + Fe2O3 −to→ 2Fe + 3H2O
- quá trinh kết hợp của nguyên tử O trong Fe2O3 với H2 gọi là quá trình oxi hóa. Ta nói đã xảy ra sự oxi hóa H2 tạo thành H2O
- quá trình tách oxi khỏi Fe2O3 gọi là quá trình khử. Ta nói đã xảy ra sự khử Fe2O3 tạo ra Fe
2. chất khử. Chất oxi hóa
chất chiếm oxi của chát khác gọi là chất khử
chất nhường oxi cho chât khác là chất oxi hóa
VD: 3H2 + Fe2O3 −to→ 2Fe + 3H2O
- H2 là chất khử
- Fe2O3 là chất oxi hóa
3. Phản ứng oxi hóa – khử
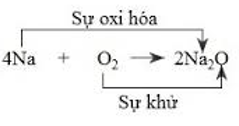
Sự khử và sự oxi hóa là hai quá trình tuy ngược nhau nhưng xảy ra đồng thời trong cùng một phản ứng hóa học. Phản ứng hóa học này được gọinlà phản ứng oxi hóa – khử
Phản ứng oxi hóa – khử là phản ứng hóa trong đó xảy ra đồng thời sự oxi oxi hóa và sự khử
4. Tầm quan trọng của phản ứng oxi hóa – khử
- Cơ sở của nhiều công nghệ sản xuất trong luyện kimvà công nghiệp hóa học
- Diễn ra trong quá trình kim loại bị phá hủy trong tự nhiên
Lý thuyết Hóa học 8 Bài 33: Điều chế khí hiđro - Phản ứng thế
1. Điều chế hidro
a. Trong phòng thí nghiệm
Cho kim loại (Al, Fe, ….) tác dụng với dung dịch axit (HCl, H2SO4).
Khí H2 được thư bằng cách đẩy không khí hay đẩy nước. nhận ra khí H2 bằng que đóm đang cháy ( cháy trong không khí với ngộn lửa xanh nhạt) hoặc dùng tàn đóm ( không làm tàn đóm bùng cháy)
VD: Fe + 2HCl → FeCl2 + H2
b. Trong công nghiệp
Hidro được điều chế bằng cách điện phân nước hoặc dùng than khử oxi của H2O trong lò khí than hoặc điều chế H2 từ khí tự nhiên, khí dầu mỏ
PT: 2H2O −điện phân→ 2H2 + O2
2. Phản ứng thế
Phản ứng thế là phản ứng hóa học của đơn chất và hợp chất trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất
VD: Fe + 2HCl → FeCl2 + H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2

