Tính chất của Brom (Br) - Tính chất hoá học, tính chất vật lí, điều chế, ứng dụng
Tính chất của Brom (Br) - Tính chất hoá học, tính chất vật lí, điều chế, ứng dụng
Với Tính chất của Brom (Br) được tổng hợp đầy đủ tất cả các tính chất hoá học, tính chất vật lí, cách nhận biết, điều chế và ứng dụng giúp bạn nắm vững kiến thức và học tốt môn Hóa hơn.

I. Định nghĩa
- Brom là một phi kim hay còn được gọi là một halogen
- Kí hiệu: Br
- Cấu hình electron:1s22s22p63s23p64s24p5 hay [Ar]4s24p5
- Số hiệu nguyên tử: Z = 35
- Khối lượng nguyên tử: 80
- Vị trí trong bảng tuần hoàn:
+ Ô, nhóm: ô số 35, nhóm VIIA
+ Chu kì: 4
- Đồng vị: Brom có 2 đồng vị bền là 7935Br và 8135Br
- Độ âm điện: 2,96
II. Tính chất vật lí & nhận biết
- Ở điều kiện bình thường, brom là chất lỏng, dễ bay hơi, có màu nâu đỏ.
- Brom ít tan trong nước, tan nhiều trong dung môi hữu cơ như benzen hay cacbon tetraclorua.
- Brom và hơi brom độc, rơi vào da có thể gây bỏng nặng.

III. Tính chất hóa học
Nhận xét: Brom là chất có tính oxi hóa mạnh nhưng kém clo.
1. Tác dụng với kim loại
Brom oxi hóa được hầu hết kim loại, trừ Au, Pt
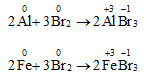
2. Tác dụng với hiđro
Brom tác dụng với hiđro khi đun nóng (không gây nổ), phản ứng tỏa nhiệt nhưng ít hơn so với phản ứng của clo.
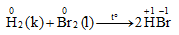
3. Tác dụng với nước và với dung dịch kiềm
* Brom phản ứng với nước tương tự như clo nhưng kém hơn
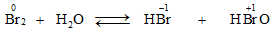
* Khi tác dụng với kiềm:
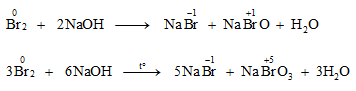
4. Tác dụng với muối của các halogen khác
* Halogen mạnh đẩy halogen yếu hơn ra khỏi dung dịch muối
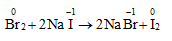
5. Tác dụng với clo trong nước
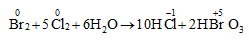
IV. Trạng thái tự nhiên
Brom không tồn tại ở dạng đơn chất, chỉ tồn tại ở dạng hợp chất; chủ yếu dưới dạng muối NaBr, KBr,.. trong nước biển, nước hồ.
V. Điều chế
* Việc điều chế brom dựa vào sự oxi hóa ion Br- , chất oxi hóa là clo
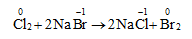
VI. Ứng dụng
- Chế tạo dược phẩm, phẩm nhuộm
- Chế tạo AgBr là chất nhạy cảm với ánh sáng để tráng lên phim ảnh
VII. Các hợp chất quan trọng của clo
- Khí hiđro bromua, axit bromhiđric (HBr)
- Hợp chất chứa oxi của Brom

