Tính chất của Silic (Si) - Tính chất hoá học, tính chất vật lí, điều chế, ứng dụng
Tính chất của Silic (Si) - Tính chất hoá học, tính chất vật lí, điều chế, ứng dụng
Với Tính chất của Silic (Si) được tổng hợp đầy đủ tất cả các tính chất hoá học, tính chất vật lí, cách nhận biết, điều chế và ứng dụng giúp bạn nắm vững kiến thức và học tốt môn Hóa hơn.

I. Định nghĩa
- Silic là một phi kim
- Kí hiệu: Si
- Cấu hình electron: 1s22s22p63s23p2 hay [Ne]3s23p2
- Số hiệu nguyên tử: Z = 14
- Khối lượng nguyên tử: 28
- Vị trí trong bảng tuần hoàn:
+ Ô, nhóm: ô số 14, nhóm IVA
+ Chu kì: 3
- Đồng vị: Silic có 3 đồng vị bền là 2814Si , 2914Si và 3014Si
- Độ âm điện: 1,90
II. Tính chất vật lí & nhận biết
- Silic có 2 dạng thù hình là silic tinh thể và silic vô định hình
+ Silic tinh thể: màu xám, có ánh kim, bền, nhiệt độ nóng chảy = 1420oC, có tính bán dẫn
+ Silic vô định hình: bột màu nâu
III. Tính chất hóa học
Nhận xét:
- Độ hoạt động hóa học: Si tinh thể < Si vô định hình
- Si là nguyên tố vừa có tính khử vừa có tính oxi hóa
1. Tính khử
a. Khử phi kim mạnh hơn: X2 (halogen), O2, S, N, C,...
+ Khử F2 ở nhiệt độ thường: 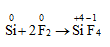
+ Khử các phi kim khác ở nhiệt độ cao: 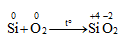
b. Khử nước trong môi trường kiềm
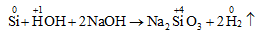
2. Tính oxi hóa
* Si oxi hóa được một số kim loại như Ca, Mg, Fe,…
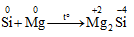
* Chú ý:
+ Khác với C, Si không oxi hóa được H2
+ Tương tự C: Si khử một số chất có tính oxi hóa mạnh (HNO3, H2SO4(đ,n),... )

IV. Trạng thái tự nhiên
- Trong tự nhiên, nguyên tố Si
+ chiếm khoảng 29,5% về khối lượng vỏ trái đất
+ có ở dạng hợp chất: cát (có SiO2 ), cao lanh (Al2O3.SiO2.H2O ),…
V. Điều chế
1. Trong phòng thí nghiệm
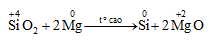
2. Trong công nghiệp
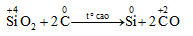
VI. Ứng dụng
- Dùng Si tinh thể, siêu tinh thể để chế tạo: các linh kiện điện tử, pin mặt trời,…
- Chế tạo thép silic: chịu axit, đàn hồi tốt.
VII. Các hợp chất quan trọng của silic
- Silic đioxit (SiO2 )
- Axit silixic, muối silicat

