Cách hoàn thành phương trình hóa học cực hay, chi tiết | Tìm chất còn thiếu trong phương trình hóa học
Cách hoàn thành phương trình hóa học cực hay, chi tiết | Tìm chất còn thiếu trong phương trình hóa học
Haylamdo biên soạn và sưu tầm Cách hoàn thành phương trình hóa học cực hay, chi tiết | Tìm chất còn thiếu trong phương trình hóa học môn Hoá học lớp 8 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập từ đó đạt điểm cao trong bài thi môn Hoá 8.

A. Lý thuyết & Phương pháp giải
Ở dạng bài tập này, để bài thường cho một phản ứng có n chất (kể cả chất phản ứng và sản phẩm), trong đó đã biết (n – 1) chất. Yêu cầu xác định chất còn lại và hệ số còn thiếu.
Để xác định chất còn lại trong phản ứng cần nhớ: Trong phản ứng hóa học số nguyên tử mỗi nguyên tố giữ nguyên trước và sau phản ứng.
Ví dụ: Hãy chọn hệ số và công thức hóa học thích hợp đặt vào chỗ dấu hỏi trong phương trình hóa học sau:
?Cu + ? → 2CuO
Hướng dẫn:
- Vế phải có Cu và O nên chất còn thiếu ở vế trái phải là O2.
- Vế phải có 2 nguyên tử Cu nên để số nguyên tử Cu ở vế trái bằng số nguyên tử Cu ở vế phải thì hệ số của Cu ở vế trái là 2.
Vậy phương trình hóa học là: 2Cu + O2 → 2CuO.
B. Ví dụ minh họa
Ví dụ 1: Chọn hệ số và công thức hóa học thích hợp đặt vào những chỗ có dấu ? trong phương trình hóa học sau:
a) Fe + ?HCl → FeCl2 + H2
b) CaO + ?HCl → CaCl2 + ?
Hướng dẫn giải:
a) Thấy vế phải có 2 nguyên tử Cl và 2 nguyên tử H, để số nguyên tử Cl và H ở hai vế bằng nhau cần thêm 2 vào trước phân tử HCl.
Vậy phương trình hóa học là:
Fe + 2HCl → FeCl2 + H2
b) Vế trái có Ca, H, Cl, O vậy chất còn lại ở vế phải nhất định phải chứa cả H và O. Vậy chất còn thiếu ở vế phải là H2O.
Vế phải có 2 nguyên tử Cl, vậy để số Cl ở hai vế bằng nhau cần thêm 2 vào trước HCl.
Vậy phương trình hóa học là:
CaO + 2HCl → CaCl2 + H2O
Ví dụ 2: Cho sơ đồ của phản ứng như sau:
Al + CuSO4 → Alx(SO4)y + Cu
Xác định các chỉ số x, y và cân bằng phương trình hóa học.
Hướng dẫn giải:
- Xác định các chỉ số x và y
Ta có Al có hóa trị III; nhóm (SO4) có hóa trị II
Áp dụng quy tắc hóa trị ta có: III.x = II.y hay 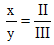
Chọn x = 2 thì y = 3.
- Cân bằng phương trình hóa học:
Thay x và y vào sơ đồ được:
Al + CuSO4 → Al2(SO4)3 + Cu
Vế phải có 2 nguyên tử Al để số nguyên tử Al ở hai về bằng nhau thêm 2 vào trước Al
2Al + CuSO4 → Al2(SO4)3 + Cu
Vế phải có 3 nhóm (SO4) để số nhóm (SO4) ở hai vế bằng nhau thêm 3 vào trước CuSO4.
2Al + 3CuSO4 → Al2(SO4)3 + Cu
Thấy phải thêm tiếp 3 vào trước Cu ở vế trái để số nguyên tử Cu ở hai vế bằng nhau.
Vậy phương trình hóa học là:
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Ví dụ 3: Cho sơ đồ phản ứng sau:
FeaOb + HCl → FeClc + H2O
Cho biết Fe có hóa trị III, hãy xác định a, b, c và cân bằng phương trình hóa học.
Hướng dẫn giải:
- Sắt có hóa trị III, vậy oxit của sắt là Fe2O3, muối sắt là FeCl3
⇒ a = 2; b = 3 và c = 3.
- Cân bằng phương trình:
Sơ đồ phản ứng: Fe2O3 + HCl → FeCl3 + H2O
Vế trái có 2 nguyên tử Fe, để số nguyên tử Fe ở hai vế bằng nhau thêm 2 vào trước FeCl3.
Fe2O3 + HCl → 2FeCl3 + H2O
Khi đó vế phải có 6 nguyên tử Cl, để số Cl ở hai vế bằng nhau thêm 6 vào trước HCl.
Fe2O3 + 6HCl → 2FeCl3 + H2O
Cuối cùng thêm 3 vào trước H2O để số nguyên tử H ở hai vế bằng nhau.
Vậy phương trình hóa học là:
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
C. Bài tập vận dụng
Câu 1: Cho sơ đồ phản ứng: Fe + … → FeCl2 + H2. Chất còn thiếu trong sơ đồ trên là
A. Cl2.
B. Cl.
C. HCl.
D. Cl2O.
Chọn C
Vế phải có chứa Fe, Cl, H do đó chất còn thiếu ở vế trái phải chứa cả H và Cl.
Vậy chất còn thiếu là HCl.
Câu 2: Cho sơ đồ phản ứng: FeClx + Cl2 → FeCl3. Giá trị của x là
A. 1.
B. 2.
C. 3.
D. 4.
Chọn B
Do sắt có 2 hóa trị là II và III nên FeClx có thể là FeCl2 hoặc FeCl3
⇒ Loại đáp án A và D.
Do vế phải là FeCl3 nên vế trái không thể là FeCl3 ⇒ loại đáp án C
Câu 3: Cho phương trình hóa học: Fe3O4 + aHCl → FeCl2 + 2FeCl3 + 4H2O.
Giá trị của a là
A. 4.
B. 6.
C. 8.
D. 10.
Chọn C
Vế phải có 8 nguyên tử H, để số H ở hai vế bằng nhau cần thêm 8 vào trước HCl.
Vậy a = 8.
Câu 4: Có sơ đồ phản ứng hóa học:
Al + AgNO3 → Al(NO3)3 + Ag. Hệ số thích hợp trong phản ứng là
A. 1 : 2 : 3 : 4.
B. 2 : 3 : 2 : 5.
C. 2 : 4 : 3 : 1.
D.1 : 3 : 1 : 3.
Đáp án D
Phương trình hóa học:
Al + 3AgNO3 → Al(NO3)3 + 3Ag.
Câu 5: Cho sơ đồ phản ứng sau:
CaO + ? HNO3 → Ca(NO3)2 + ?
Hệ số trước HNO3 và chất còn thiếu trong sơ đồ phản ứng lần lượt là
A. 1 và H2O.
B. 2 và H2O.
C. 2 và HNO3.
D. 2 và NO2.
Đáp án B
CaO + 2HNO3 → Ca(NO3)2 + H2O
Câu 6: Cho phương trình phản ứng hoá học sau: MnO2 + 4? → MnCl2 + Cl2 + 2H2O
Chất còn thiếu trong phương trình là
A. Cl2.
B. H2O.
C. HCl.
D. Cl2O.
Đáp án C
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Câu 7: Cho sơ đồ phản ứng sau:
K2CO3 + CaCl2 → CaCO3 + ?
Tỉ lệ số phân tử của các chất tham gia phản ứng là
A. 1 : 1.
B. 2 : 1.
C. 1 : 2.
D. 1 : 3.
Phương trình hóa học:
K2CO3 + CaCl2 → CaCO3 + 2KCl
Tỉ lệ số phân tử K2CO3 : số phân tử CaCl2 là 1 : 1.
Câu 8: Hoà tan nhôm (Al) trong dung dịch axit sunfuric (H2SO4) thu được nhôm sunfat (Al2(SO4)3) và khí là
A. H2.
B. O2.
C. CO2.
D. H2O.
Đáp án A
Khí là H2.
2Al + 3H2SO4 → Al2(SO4)3 + 3H2.
Câu 9: Có sơ đồ phản ứng sau: Al + Fe3O4 → ? + Al2O3. Đơn chất còn thiếu trong sơ đồ và tổng hệ số các chất sản phẩm lần lượt là
A. Fe và 10.
B. Al và 11.
C. Fe và 12.
D. Fe và 13.
Đáp án D
8Al + 3Fe3O4 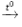
Tổng hệ số các chất sản phẩm là 9 + 4 = 13.
Câu 10: Cho sơ đồ phản ứng hóa học sau:
Zn + ? → ZnCl2 + H2
Tổng hệ số các chất tham gia phản ứng là
A. 1
B. 2
C. 3
D. 4
Đáp án C
Zn + 2HCl → ZnCl2 + H2
Tổng hệ số các chất tham gia phản ứng là: 1 + 2 = 3.

