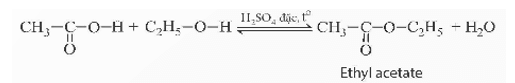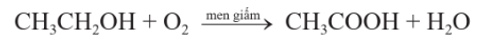Lý thuyết KHTN 9 Bài 24: Acetic acid - Cánh diều
Haylamdo biên soạn tóm tắt lý thuyết Khoa học tự nhiên 9 Bài 24: Acetic acid sách Cánh diều hay nhất, ngắn gọn sẽ giúp học sinh lớp 9 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn KHTN 9.
Lý thuyết KHTN 9 Bài 24: Acetic acid - Cánh diều
I. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT VẬT LÍ
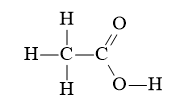
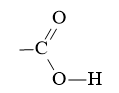
- Acetic acid có công thức phân tử C2H4O2 và có công thức cấu tạo:
Công thức cấu tạo thu gọn: CH3 – COOH hoặc CH3COOH.
Trong phân tử acetic acid, nguyên tử C liên kết với nguyên tử O và nhóm –OH tạo thành nhóm
- Nhóm – COOH tạo nên tính chất hoá học đặc trưng cho acetic acid.
- Ở điều kiện thường, acetic acid là chất lỏng, không màu, vị chua, tan vô hạn trong nước, sôi ở 118oC, có khối lượng riêng là 1,045 g/mL (ở 20oC).
II. TÍNH CHẤT HOÁ HỌC
1. Tính acid
- Acetic acid phản ứng được với các base, oxide base, muối carbonate và nhiều kim loại tạo ra muối acetate. Ví dụ:
+ Tác dụng với base:
CH3COOH + NaOH → CH3COONa + H2O
+ Tác dụng với oxide base:
2CH3COOH + CuO → (CH3COO)2Cu + H2O
+ Tác dụng với kim loại:
2CH3COOH + Zn → (CH3COO)2Zn + H2↑
+ Tác dụng với muối:
2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 + H2O
2. Tác dụng với alcohol tạo thành ester (phản ứng ester hoá)
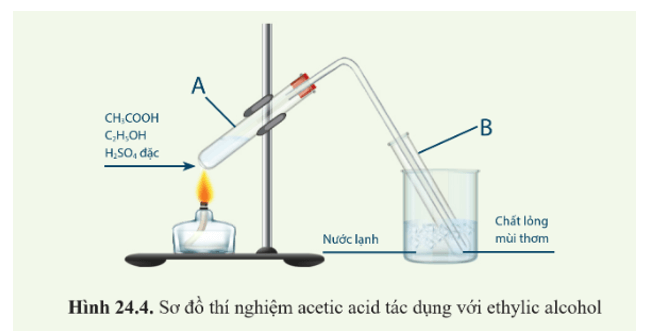
- Khi đun nóng và có H2SO4 đặc làm xúc tác, acetic acid tác dụng với ethylic alcohol tạo ra ester là ethyl acetate theo phương trình hoá học:
- Phản ứng giữa acetic acid và ethylic alcohol tạo ra ester (ethyl acetate) thuộc loại phản ứng ester hoá.
- Phản ứng ester hoá diễn ra với tốc độ chậm và không hoàn toàn.
3. Phản ứng cháy
- Acetic acid cháy theo phương trình hoá học:
III. ĐIỀU CHẾ ACETIC ACID
- Nhờ tác dụng của men giấm, ethylic alcohol được chuyển thành acetic acid theo phương trình hoá học sau:
- Acetic acid thu được theo phương pháp lên men dung dịch loãng của ethylic alcohol (rượu nhạt) chủ yếu được sử dụng làm giấm ăn và là nguyên liệu trong công nghiệp thực phẩm.
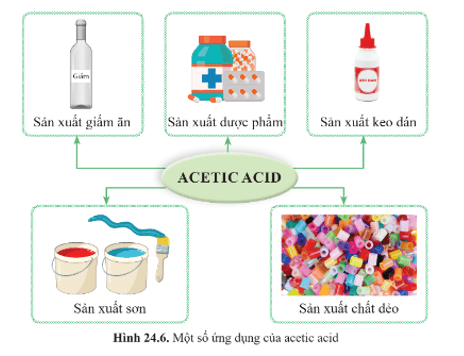
IV. ỨNG DỤNG CỦA ACETIC ACID
- Acetic acid có nhiều ứng dụng trong đời sống và sản xuất. Một số ứng dụng chủ yếu của acetic acid được trình bày trong hình: