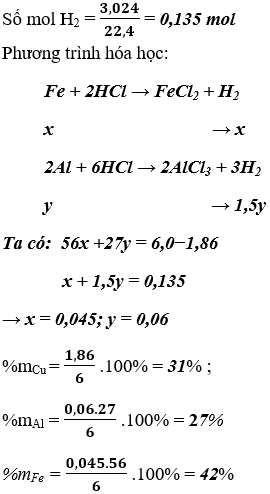Giải vở bài tập Hóa Học 9 Bài 22: Luyện tập chương 2: Kim loại
Giải vở bài tập Hóa Học 9 Bài 22: Luyện tập chương 2: Kim loại
Nhằm mục đích giúp học sinh dễ dàng làm bài tập về nhà trong Vở bài tập Hóa Học lớp 9, chúng tôi biên soạn giải vở bài tập Hóa Học lớp 9 Bài 22: Luyện tập chương 2: Kim loại hay nhất, ngắn gọn bám sát nội dung sách Vở bài tập Hóa Học 9.
Học theo Sách giáo khoa
1. Tính chất hoá học của kim loại
a) Dãy hoạt động hoá học của kim loại:
K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au
b) Tính chất:
+ Tác dụng với phi kim.
+ Tác dụng với nước.
+ Tác dụng với dung dịch axit.
+ Tác dụng với dung dịch muối.
2. Tính chất hoá học của kim loại nhôm và sắt có gì giống nhau và khác nhau ?
a) Giống nhau
+ Nhôm, sắt có những tính chất hoá học của kim loại.
+ Nhôm, sắt đều không phản ứng với HNO3 đặc, nguội và H2SO4 đặc, nguội.
b) Khác nhau
+ Nhôm có phản ứng với kiềm.
+ Khi tham gia phản ứng, nhôm tạo thành hợp chất trong đó nhôm chỉ có hoá trị (III), còn sắt tạo thành hợp chất, trong đó sắt có hoá trị (II) hoặc (III).
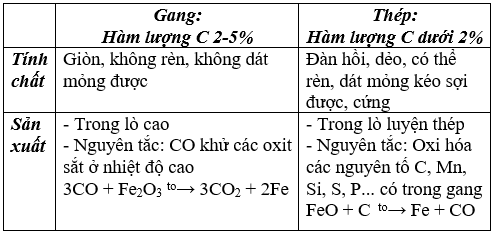
3. Hợp kim của sắt: thành phần, tính chất và sản xuất gang, thép.
4. Sự ăn mòn kim loại và bảo vệ kim loại (KL) không bị ăn mòn
Sự ăn mòn KL: là sự phá hủy kim loại, hợp kim do tác dụng hóa học trong môi trường
Các yếu tố ảnh hưởng đến ăn mòn KL: Ảnh hưởng của các chất trong môi trường; ảnh hưởng của nhiệt độ.
Bảo vệ KL bằng cách: Ngăn không cho kỉm loại tiếp xúc với môi trường; Sơn, mạ, bôi dầu mỡ... lên trên bề mặt kim loại; Chế tạo hợp kim ít bị ăn mòn
Bài tập
Bài 1. (Trang 65 Vở Bài Tập Hóa học 9 ) Hãy viết hai phương trình hoá học trong mỗi trường hợp sau đây :
a) Kim loại tác dụng với oxi tạo thành oxit bazơ.
b) Kim loại tác dụng với phi kim tạo thành muối.
c) Kim loại tác dụng với dung dịch axit tạo thành muối và giải phóng khí hiđro.
d) Kim loại tác dụng với dung dịch muối tạo thành muối mới và kim loại mới.
Lời giải:
Viết 2 phương trình hóa học trong mỗi trường hợp sau:
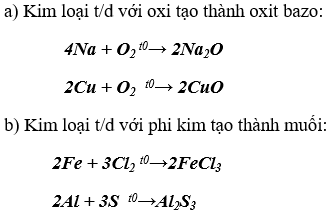
c) Kim loại t/d với dd axit tạo thành muối và giải phóng khí hidro:
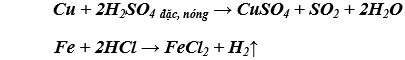
d) Kim loại t/d với dd muối tạo thành muối và kim loại mới:
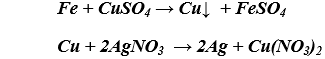
Bài 2. (Trang 65 Vở Bài Tập Hóa học 9 ) Hãy xét xem các cặp chất sau đây, cặp chất nào có phản ứng ? Không có phản ứng ?
a) Al và khí Cl2 ;
b) Al và HNO3 đặc, nguội;
c) Fe và H2SO4 đặc, nguội;
d) Fe và dung dịch Cu(NO3)2.
Viết các phương trình hoá học (nếu có).
Lời giải:
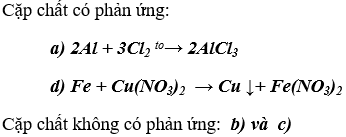
Bài 3. (Trang 65 Vở Bài Tập Hóa học 9 ) Có 4 kim loại: A,B,C,D đứng sau Mg trong dãy hoạt động hoá học. Biết rằng :
a) A và B tác dụng với dung dịch HCl giải phóng khí hiđro.
b) C và D không có phản ứng với dung dịch HCl.
c) B tác dụng với dung dịch muối của A và giải phóng A.
d) D tác dụng được với dung dịch muối của C và giải phóng C.
Hãy xác định thứ tự sắp xếp nào sau đây là đúng (theo chiều hoạt động hoá học giảm dần):
a) B, D, C, A; b) D, A, B, C;
c) B, A, D, C; d) A, B, C, D;
e) C, B, D, A.
Lời giải:
Đáp án C
Bài 4. (Trang 66 Vở Bài Tập Hóa học 9 ) Viết phương trình hoá học biểu diễn sự chuyển đổi sau đây:
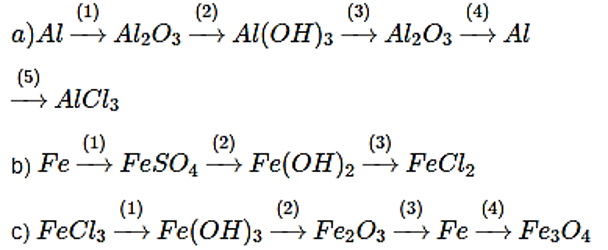
Lời giải:
Viết các phương trình hóa học cho dãy biến hóa:
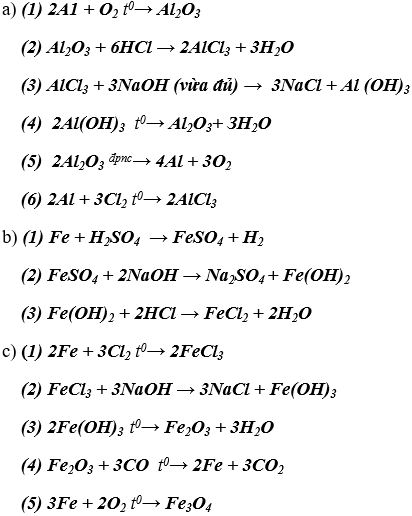
Bài 5. (Trang 66 Vở Bài Tập Hóa học 9 ) Cho 9,2 gam một kim loại A phản ứng với khí clo dư tạo thành 23,4 gam muối. Hãy xác định kim loại A, biết A có hoá trị I.
Lời giải:

Bài 6. (Trang 66 Vở Bài Tập Hóa học 9 ) Ngâm một lá sắt có khối lượng 2,5 gam trong 25 ml dung dịch CuSO4 15% có khối lượng riêng là 1,12 g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô thì cân nặng 2,58 gam.
a) Hãy viết phương trình hoá học.
b) Tính nồng độ phần trăm của các chất trong dung dịch sau phản ứng.
Lời giải:
Khối lượng của dung dịch CuSO4 = 25. 1,12 = 28 gam
mCuSO4 = (28. 15):100 = 4,2 gam;
nCuSO4 = 0,02625 mol
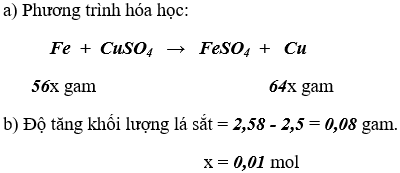
Dung dịch sau phản ứng chứa FeSO4 0,01 mol hay 1,52 gam và CuSO4 dư 0,02625 - 0,01 = 0,01625 mol hay 2,6 gam
Khối lượng dung dịch sau phản ứng = 25.1,12 + 0,01.56 - 0,01.64 = 27,91 g
Nồng độ C% chất tan:
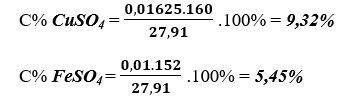
Bài 7. (Trang 67 Vở Bài Tập Hóa học 9 ) Cho 0,83 gam hỗn hợp gồm nhôm và sắt tác dụng với dung dịch H2SO4 loãng, dư. Sau phản ứng thu được 0,56 lít khí ở đktc.
a) Viết các phương trình hoá học.
b) Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hổn hợp ban đầu.
Lời giải:

Khối lượng nhôm = 2,7 gam và khối lượng sắt = 5,6 gam
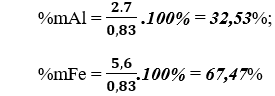
Bài tập bổ sung
Bài 1. (Trang 67 Vở Bài Tập Hóa học 9 ) Cho 6,5 gam muối sắt clorua tác dụng với dung dịch AgNO3 dư tạo ra 17,22 gam kết tủa. Hãy khoanh tròn vào một trong các chữ cái A, B, C, D đứng trước công thức phân tử đúng của muối sắt clorua.
A. FeCl2
B. FeCl3
C. FeCl
D. FeCl4
Lời giải:
Đáp án đúng là: B
Bài 2. (Trang 67 Vở Bài Tập Hóa học 9 ) Khi hòa tan 6,0 gam hợp kim gồm Cu, Fe và Al trong axit clohidric thấy thoát ra 3,024 lít hidro (đktc) và còn lại 1,86 gam kim loại không tan.
a) Viết các phương trình hóa học.
b) Xác định thành phần phần trăm khối lượng các kim loại trong hỗn hợp kim loại.
Lời giải: