Giải vở bài tập Hóa Học 9 Bài 5: Luyện tập: Tính chất hóa học của oxit và axit
Giải vở bài tập Hóa Học 9 Bài 5: Luyện tập: Tính chất hóa học của oxit và axit
Nhằm mục đích giúp học sinh dễ dàng làm bài tập về nhà trong Vở bài tập Hóa Học lớp 9, chúng tôi biên soạn giải vở bài tập Hóa Học lớp 9 Bài 5: Luyện tập: Tính chất hóa học của oxit và axit hay nhất, ngắn gọn bám sát nội dung sách Vở bài tập Hóa Học 9.
Học theo Sách giáo khoa
1. Tính chất hóa học của oxit
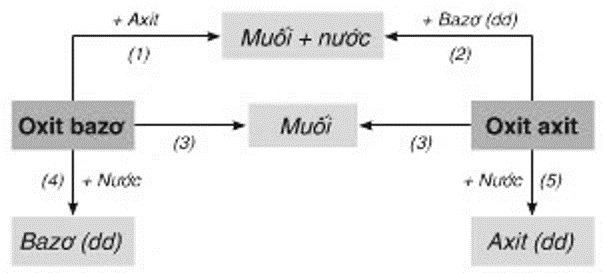
2. Tính chất hóa học của axit
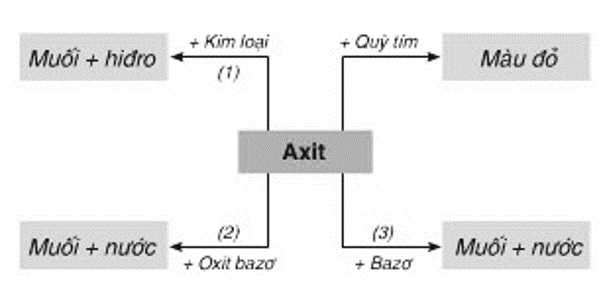
Chú ý: Axit sunfuric đặc có tính chất đặc trưng
* Tác dụng với nhiều kim loại, không giải phóng hiđro.
Phương trình hóa học: Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O
* Tính háo nước, hút ẩm:
C12H22O11 + H2SO4 ⟶ 12C + 11H2O
Bài tập
Bài 1. (Trang 21 Vở Bài Tập Hóa học 9 ) Có những oxit sau: SO2, CuO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với
a) Nước
b) Axit clohiđric
c) Natri hiđroxit
Lời giải:
a) Những oxit tác dụng với nước là: SO2, Na2O, CO2
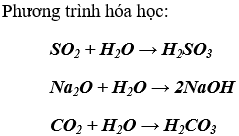
b) Những oxit tác dụng với HCl là CuO, Na2O
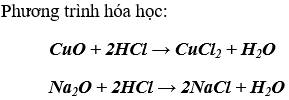
c) Những oxit tác dụng với natri hiđroxit là SO2 và CO2
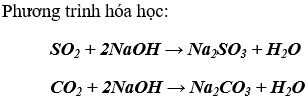
Bài 2. (Trang 21 Vở Bài Tập Hóa học 9 ) Những oxit nào dưới đây có thể điều chế bằng
a) phản ứng hóa hợp ? Viết phương trình hóa học
b) phản ứng hóa hợp và phản ứng phân hủy? viết phương trình hóa học.
(1) H2O; (2) CuO; (3) Na2O;
(4) CO2; (5) P2O5
Lời giải:
a) Những oxit có thể điều chế bằng phản ứng hóa hợp: H2O, CuO, Na2O, P2O5, CO2 .

b) Những oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, H2O
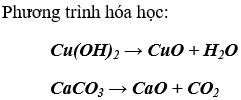
Bài 3. (Trang 21 Vở Bài Tập Hóa học 9 ) Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí SO2 và CO2. Làm thế nào có thể loại bỏ được những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất?
Lời giải:
Có thể loại bỏ các tạp chất SO2 và CO2 ra khỏi CO bằng cách: Dẫn hỗn hợp khí đi qua dung dịch Ca(OH)2 dư, toàn bộ SO2 và CO2 bị hấp thụ hết.
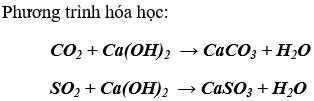
Bài 4. (Trang 22 Vở Bài Tập Hóa học 9 ) Cần phải điều chế một lượng muối đồng (II) sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric ?
a) Axit sunfuric tác dụng với đồng (II) oxit.
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Lời giải:
Phương pháp được lựa chọn để tiết kiệm axit sunfuric là: (a)
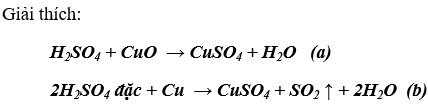
Bài 5. (Trang 22 Vở Bài Tập Hóa học 9 ) Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình hóa học.
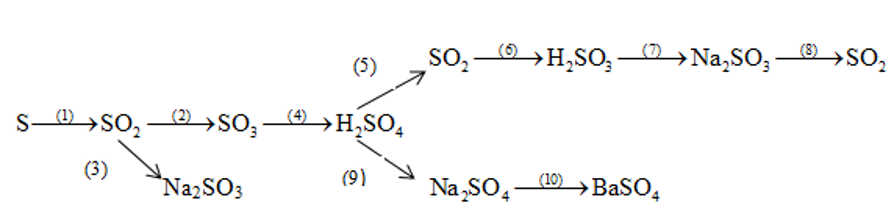
Lời giải:
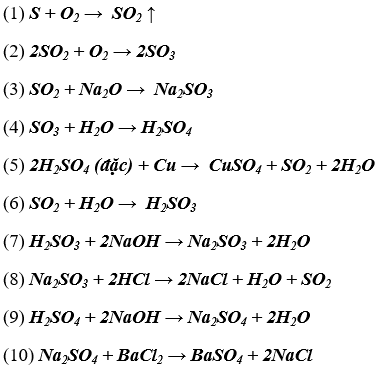
Bài tập bổ sung
Bài 1. (Trang 22 Vở Bài Tập Hóa học 9 ) Cho biết phương trình hóa học của phản ứng đốt cháy cacbon monooxit:
2CO + O2 → 2 CO2
Để tạo ra 0,50 mol CO2 thì số mol O2 tham gia phản ứng là:
A. 0,50;
B. 1,00;
C. 0,25;
D. 0,125
Lời giải:
Kết quả đúng: C
Theo PTHH ta có:
nO2=1/2nCO2 = 0,25mol
Bài 2. (Trang 22 Vở Bài Tập Hóa học 9 ) Phương trình hóa học của phản ứng trung hòa H2SO4 bằng NaOH:
2NaOH + H2SO4 → Na2SO4 + 2H2O
Số mol NaOH cần dùng để trung hòa 0,20 mol H2SO4 là
A. 0,10 mol
B. 0,20 mol
C. 0,05 mol
D. 0,40 mol
Lời giải:
Kết quả đúng: D
Theo PTHH ta có:
nNaOH = 2nH2SO4 = 0,4mol
Bài 3. (Trang 22 Vở Bài Tập Hóa học 9 ) Cho 0,20 mol Al tác dụng với dung dịch H2SO4 loãng, dư, số mol khí hiđro sinh ra là:
A. 0,20 mol
B. 0,30 mol
C. 0,10 mol
D. 0,15mol
Lời giải:
Kết quả đúng: B
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Theo PTHH ta có:
nH2 = 3/2nAl = 3/2.0,2 = 0,3mol
Bài 4. (Trang 22 Vở Bài Tập Hóa học 9 ) Chất khí có tỉ khối với khí oxi (O2) bằng 2 là:
A. CO2
B. NO2
C. SO2
D. CO
Lời giải:
Kết quả đúng: C
MA = 2.32 = 64


