Giải vở bài tập Hóa Học 9 Bài 32: Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Giải vở bài tập Hóa Học 9 Bài 32: Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Nhằm mục đích giúp học sinh dễ dàng làm bài tập về nhà trong Vở bài tập Hóa Học lớp 9, chúng tôi biên soạn giải vở bài tập Hóa Học lớp 9 Bài 32: Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hóa học hay nhất, ngắn gọn bám sát nội dung sách Vở bài tập Hóa Học 9.
Học theo Sách giáo khoa
I. TÍNH CHẤT HÓA HỌC CỦA PHI KIM
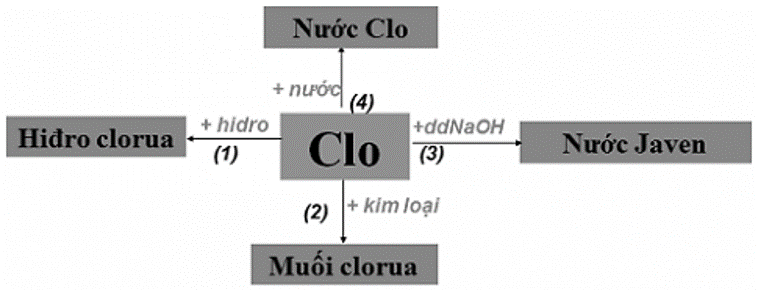
1. Tính chất hóa học của clo
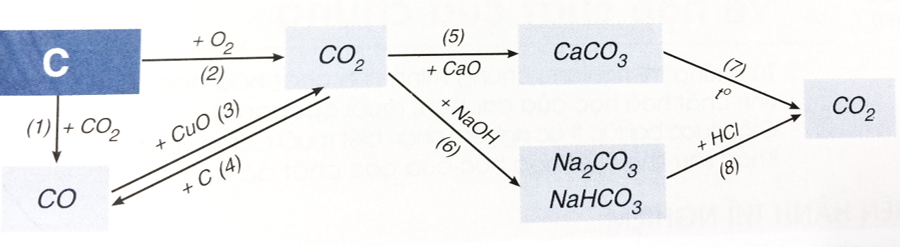
2. Tính chất hóa học của cacbon và hợp chất của cacbon
II. BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Cấu tạo bảng tuần hoàn
Ô: Ô nguyên tố cho biết số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố, nguyên tử khối của nguyên tố đó.
Chu kì: là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp theo chiều điện tích hạt nhân tăng dần.
Nhóm: gồm các nguyên tố mà nguyên tử của chúng có sô electron lớp ngoài cùng bằng nhau, do đó có tính chắt tương tự nhau.
2. Sự biến đổi tính chất của các nguyên tố trong bảng tuần hoàn
Trong chu kì:
Số e lớp ngoài cùng của nguyên tử tăng dần từ 1 đến 8 electron.
Tính kim loại của các nguyên tố giảm dần, đồng thời tính phi kim của các nguyên tố tăng dần.
Trong nhóm: Trong một nhóm, khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân. Số lớp electron trong nguyên tử tăng dần, tính kim loại của các nguyên tố tăng dần, đồng thời tính phi kim của các nguyên tố giảm dần.
3. Ý nghĩa của bảng tuần hoàn:
- Biết vị trí của nguyên tô ta có thể suy đoán cấu tạo nguyên tử và tính chất của nguyên tố.
- Biết cấu tạo nguyên tử của nguyên tố có thể suy đoán vị trí và tính chất nguyên tố đó.
Bài tập
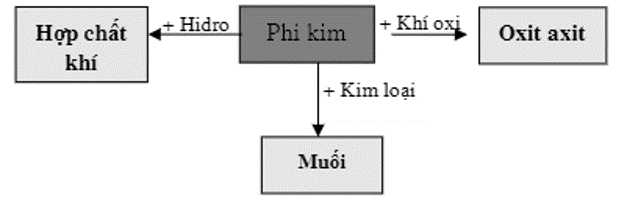
Bài 1. (Trang 97 Vở bài tập Hóa học 9 ) Căn cứ vào sơ đồ 1, hãy viết các phương trình hoá học với phi kim cụ thể là lưu huỳnh.
Lời giải:

Bài 2. (Trang 97 Vở bài tập Hóa học 9 ) Hãy viết các phương trình hoá học biểu diễn tính chất hoá học của clo theo sơ đồ 2.
Lời giải:
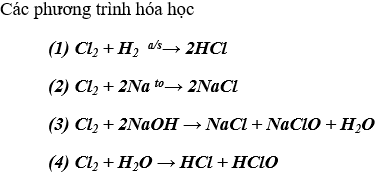
Bài 3. (Trang 97 Vở bài tập Hóa học 9 ) Hãy viết các phương trình hoá học biểu diễn tính chất hoá học của cacbon và một số hợp chất của nó theo sơ đồ 3. Cho biết vai trò của cacbon trong các phản ứng đó.
Lời giải:

Bài 4. (Trang 97 Vở bài tập Hóa học 9 ) Nguyên tố A có số hiệu nguyên tử là 11, chu kì 3, nhóm I trong bảng tuần hoàn các nguyên tố hoá học. Hãy cho biết:
- Cấu tạo nguyên tử của A.
- Tính chất hoá học đặc trưng của A.
- So sánh tính chất hoá học của A với các nguyên tố lân cận.
Lời giải:
* Cấu tạo nguyên tử:
- Số hiệu nguyên tử là 11 nên A có điện tích hạt nhân là 11+
- Chu kì 3 nên A có 3 lớp electron
- Nhóm I nên A có 1 electron lớp ngoài cùng
* Tính chất hóa học đặc trưng: A là một kim loại mạnh
* So sánh tính chất hóa học của A (Na) với các nguyên tố lân cận (Mg và K): Tính kim loại Mg<Na<K
Bài 5. (Trang 97 Vở bài tập Hóa học 9 ) a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Lời giải:

Bài 6. (Trang 98 Vở bài tập Hóa học 9 ) Cho 69,6 gam MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dần khí X vào 500 ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
Lời giải:

Bài tập bổ sung
Bài 1. (Trang 98 Vở bài tập Hóa học 9 ) Các chất trong cặp nào sau đây tồn tại được trong cùng một bình chứa:
A. Cl2 và KOH
B. KOH và HCl
C. Na2CO3 và Ba(OH)3
D. Na2CO3 và KOH
Lời giải:
Cặp D: Na2CO3 và KOH cùng tồn tại trong một bình chứa
Bài 2. (Trang 98 Vở bài tập Hóa học 9 ) Hãy ghép một số 1 hoặc 2, 3, 4 chỉ nội dung thí nghiệm với một trong các chữ A, B, C, D, E chỉ hiện tượng quan sát được sao cho phù hợp
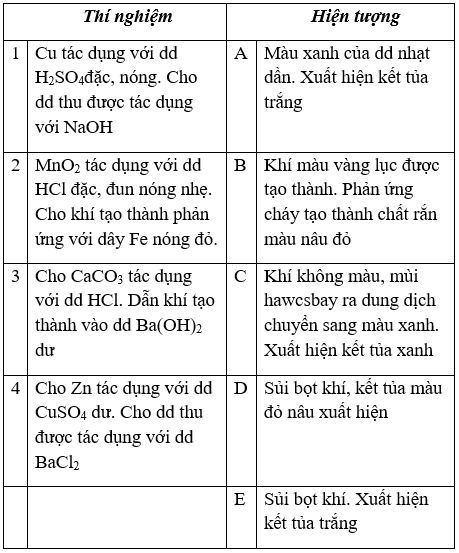
Lời giải:
1 – C ; 2 – B; 3 – E ; 4 – A
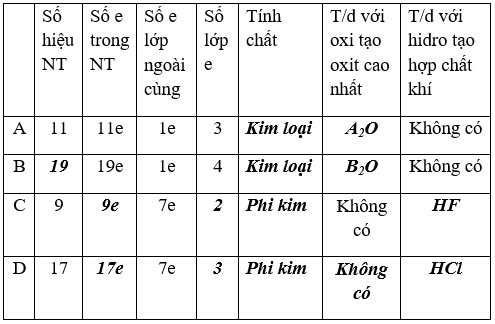
Bài 3. (Trang 98 Vở bài tập Hóa học 9 ) Hãy điền nội dung thích hợp vào ô trống trong bảng: A, B là hai nguyên tố ở nhóm I; C, D ở nhóm VII, chu kì 2, 3 của bảng tuần hoàn.
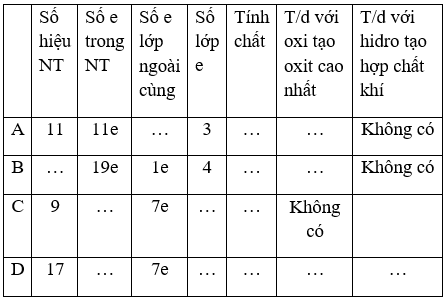
Lời giải: