Lý thuyết Hóa học 9 Bài 16: Tính chất hóa học của kim loại hay, chi tiết
Lý thuyết Hóa học 9 Bài 16: Tính chất hóa học của kim loại hay, chi tiết
Haylamdo biên soạn và sưu tầm tóm tắt lý thuyết Hóa học 9 Bài 16: Tính chất hóa học của kim loại hay, chi tiết nhất sẽ tóm tắt kiến thức trọng tâm bài học từ đó giúp học sinh ôn tập để nắm vững kiến thức môn Hóa 9.

1. Tác dụng với phi kim
a) Tác dụng với oxi:
Hầu hết kim loại (trừ Au, Pt, Ag,..) tác dụng với oxi ở nhiệt độ thường hoặc nhiệt độ cao, tạo thành oxit.
Ví dụ:
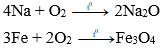
b) Tác dụng với phi kim khác (Cl2, S, ...):
Nhiều kim loại tác dụng với nhiều phi kim, tạo thành muối.
Ví dụ:
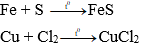
2. Tác dụng với dung dịch axit
Nhiều kim loại tác dụng với dung dịch axit (HCl, H2SO4 loãng...) tạo thành muối và H2.
Ví dụ:
Fe + 2HCl → FeCl2 + H2
2Al + 3H2SO4 (loãng) → Al2(SO4)3 + 3H2
3. Tác dụng với dung dịch muối
Kim loại hoạt động mạnh hơn (trừ các kim loại phản ứng với nước như Na, K, Ba, Ca...) tác dụng với muối của kim loại yếu hơn, tạo thành muối mới và kim loại mới.
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
Mg + FeCl2 → MgCl2 + Fe

