Tổng hợp kiến thức môn Hóa học lớp 9 đầy đủ, chi tiết
Tổng hợp kiến thức môn Hóa học lớp 9 đầy đủ, chi tiết
Loạt tài liệu tổng hợp kiến thức môn Hóa học lớp 9 đầy đủ, chi tiết theo từng bài học. Hi vọng tài liệu này sẽ giúp học sinh dễ dàng hệ thống lại kiến thức và học tốt môn Hóa học 9.

Tổng hợp lý thuyết Hóa học 9 Chương 1 chi tiết
- Lý thuyết Bài 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit (hay, chi tiết)
- Lý thuyết Bài 2: Một số oxit quan trọng (hay, chi tiết)
- Lý thuyết Bài 3: Tính chất hóa học của axit (hay, chi tiết)
- Lý thuyết Bài 4: Một số axit quan trọng (hay, chi tiết)
- Lý thuyết Bài 5: Luyện tập: Tính chất hóa học của oxit và axit (hay, chi tiết)
- Lý thuyết Bài 7: Tính chất hóa học của bazơ (hay, chi tiết)
- Lý thuyết Bài 8: Một số bazơ quan trọng (hay, chi tiết)
- Lý thuyết Bài 9: Tính chất hóa học của muối (hay, chi tiết)
- Lý thuyết Bài 10: Một số muối quan trọng (hay, chi tiết)
- Lý thuyết Bài 11: Phân bón hóa học (hay, chi tiết)
- Lý thuyết Bài 12: Mối quan hệ giữa các loại hợp chất vô cơ (hay, chi tiết)
- Lý thuyết Bài 13: Luyện tập chương 1: Các loại hợp chất vô cơ (hay, chi tiết)
Tổng hợp lý thuyết Hóa học 9 Chương 2 chi tiết
- Lý thuyết Bài 15: Tính chất vật lí của kim loại (hay, chi tiết)
- Lý thuyết Bài 16: Tính chất hóa học của kim loại (hay, chi tiết)
- Lý thuyết Bài 17: Dãy hoạt động hóa học của kim loại (hay, chi tiết)
- Lý thuyết Bài 18: Nhôm (hay, chi tiết)
- Lý thuyết Bài 19: Sắt (hay, chi tiết)
- Lý thuyết Bài 20: Hợp kim sắt: Gang, thép (hay, chi tiết)
- Lý thuyết Bài 21: Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn (hay, chi tiết)
- Lý thuyết Bài 22: Luyện tập chương 2: Kim loại (hay, chi tiết)
- Lý thuyết Bài 24: Ôn tập học kì 1 (hay, chi tiết)
Tổng hợp lý thuyết Hóa học 9 Chương 3 chi tiết
- Lý thuyết Bài 25: Tính chất của phi kim (hay, chi tiết)
- Lý thuyết Bài 26: Clo (hay, chi tiết)
- Lý thuyết Bài 27: Cacbon (hay, chi tiết)
- Lý thuyết Bài 28: Các oxit của cacbon (hay, chi tiết)
- Lý thuyết Bài 29: Axit cacbonic và muối cacbonat (hay, chi tiết)
- Lý thuyết Bài 30: Silic. Công nghiệp silicat (hay, chi tiết)
- Lý thuyết Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học (hay, chi tiết)
- Lý thuyết Bài 32: Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hóa học (hay, chi tiết)
Tổng hợp lý thuyết Hóa học 9 Chương 4 chi tiết
- Lý thuyết Bài 34: Khái niệm về hợp chất hữu cơ và hóa học hữu cơ (hay, chi tiết)
- Lý thuyết Bài 35: Cấu tạo phân tử hợp chất hữu cơ (hay, chi tiết)
- Lý thuyết Bài 36: Metan (hay, chi tiết)
- Lý thuyết Bài 37: Etilen (hay, chi tiết)
- Lý thuyết Bài 38: Axetilen (hay, chi tiết)
- Lý thuyết Bài 39: Benzen (hay, chi tiết)
- Lý thuyết Bài 40: Dầu mỏ và khí thiên nhiên (hay, chi tiết)
- Lý thuyết Bài 41: Nhiên liệu (hay, chi tiết)
- Lý thuyết Bài 42: Luyện tập chương 4 : Hiđrocacbon - Nhiên liệu (hay, chi tiết)
Tổng hợp lý thuyết Hóa học 9 Chương 5 chi tiết
- Lý thuyết Bài 44: Rượu etylic (hay, chi tiết)
- Lý thuyết Bài 45: Axit axetic (hay, chi tiết)
- Lý thuyết Bài 46: Mối liên hệ giữa etilen, rượu etylic và axit axetic (hay, chi tiết)
- Lý thuyết Bài 47: Chất béo (hay, chi tiết)
- Lý thuyết Bài 48: Luyện tập: Rượu etylic, axit axetic và chất béo (hay, chi tiết)
- Lý thuyết Bài 50: Glucozơ (hay, chi tiết)
- Lý thuyết Bài 51: Saccarozơ (hay, chi tiết)
- Lý thuyết Bài 52: Tinh bột và xenlulozơ (hay, chi tiết)
- Lý thuyết Bài 53: Protein (hay, chi tiết)
- Lý thuyết Bài 54: Polime (hay, chi tiết)
- Lý thuyết Bài 56: Ôn tập cuối năm (hay, chi tiết)
Hóa học 9 Bài 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit
I. Tính chất hóa học của oxit
1. Oxit bazơ: Oxit bazơ có những tính chất hóa học nào ?
a) Tác dụng với nước Một số oxit bazơ tác dụng với nước tạo thành dung dịch bazơ (kiềm).
Ví dụ:
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
Những oxit bazơ tác dụng với nước tạo thành dung dịch kiềm là: Li2O, Na2O, K2O, Rb2O, Cs2O, CaO, BaO, SrO.
b) Tác dụng với axit: Oxit bazơ + axit → muối + nước
Ví dụ:
BaO + 2HCl → BaCl2 + H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
c) Tác dụng với oxit axit: Một số oxit bazơ, là những oxit bazơ tan trong nước tác dụng với oxit axit tạo thành muối.
Ví dụ:
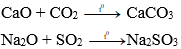
2. Oxit axit: Oxit axit có những tính chất hóa học nào ?
a) Tác dụng với nước: Nhiều oxit axit tác dụng với nước tạo thành dung dịch axit.
Ví dụ:
SO3 + H2O → H2SO4
P2O5 + 3H2O → 2H3PO4
Những oxit khác như SO2, N2O5 … cũng có phản ứng tương tự.
b) Tác dụng với dung dịch bazơ: Oxit axit + dung dịch bazơ → muối + nước.
Ví dụ:
CO2 + Ca(OH)2 → CaCO3 (↓) + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Những oxit khác như SO2, P2O5 …cũng có phản ứng tương tự.
c) Tác dụng với oxit bazơ: Oxit axit tác dụng với một số oxit bazơ (tan) tạo thành muối.
Ví dụ:
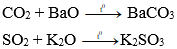
3. Oxit lưỡng tính: Một số oxit vừa tác dụng dung dịch axit, vừa tác dụng với dung dịch bazơ, gọi là oxit lưỡng tính như: Al2O3, ZnO, Cr2O3, PbO…
Ví dụ:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + 2NaOH → H2O + 2NaAlO2 (natri aluminat)
4. Oxit trung tính (hay là oxit không tạo muối): Một số oxit không tác dụng với axit, dung dịch bazơ, nước gọi là oxit trung tính như: NO, N2O, CO,…
II. Khái quát về sự phân loại oxit
Căn cứ vào tính chất hóa học của oxit, người ta phân loại oxit thành 4 loại như sau:
1. Oxit bazơ là những oxit tác dụng với dung dịch axit tạo thành muối và nước.
2. Oxit axit là những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
3. Oxit lưỡng tính là những oxit tác dụng với dung dịch axit và tác dụng với dung dịch bazơ tạo thành muối và nước.
4. Oxit trung tính hay còn gọi là oxit không tạo muối là những oxit không tác dụng với axit, bazơ, nước.
Hóa học 9 Bài 2: Một số oxit quan trọng
I. CANXI OXIT
- Công thức hóa học là CaO, tên thông thường là vôi sống, là chất rắn, màu trắng.
1. Tính chất hóa học
CaO có đầy đủ tính chất hóa học của oxit bazơ.
a) Tác dụng với nước: CaO (r) + H2O (l) → Ca(OH)2 (r)
Phản ứng của CaO với nước gọi là phản ứng tôi vôi, phản ứng này tỏa nhiều nhiệt.
Chất Ca(OH)2 tạo thành gọi là vôi tôi, là chất rắn màu trắng, ít tan trong nước, phần tan tạo thành dung dịch bazơ còn gọi là nước vôi trong.
CaO có tính hút ẩm mạnh nên được dùng để làm khô nhiều chất.
b) Tác dụng với axit tạo thành muối và nước.
Ví dụ:
CaO + 2HCl → CaCl2 + H2O
Nhờ tính chất này, CaO được dùng để khử chua đất trồng trọt, xử lý nước thải của nhiều nhà máy hóa chất, …
c) Tác dụng với oxit axit tạo thành muối.
Ví dụ:
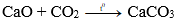
Vì vậy CaO sẽ giảm chất lượng nếu lưu giữ lâu ngày trong tự nhiên.
2. Ứng dụng của canxi oxit
CaO có những ứng dụng chủ yếu sau đây:
- Phần lớn canxi oxit được dùng trong công nghiệp luyện kim và làm nguyên liệu cho công nghiệp hóa học.
- Ngoài ra, canxi oxit còn được dùng để khử chua đất trồng trọt, xử lí nước thải công nghiệp, sát trùng, diệt nấm, khử độc môi trường,…
- Canxi oxit có tính hút ẩm mạnh nên được dùng để làm khô nhiều chất.
3. Sản xuất canxi oxit trong công nghiệp
Nguyên liệu để sản xuất canxi oxit là đá vôi (chứa CaCO3). Chất đốt là than đá, củi, dầu, khí tự nhiên,…
Các phản ứng hóa học xảy ra khi nung đá vôi:
- Than cháy sinh ra khí CO2 và tỏa nhiều nhiệt: 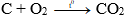
- Nhiệt sinh ra phân hủy đá vôi ở khoảng trên 900°C: 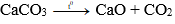
II. LƯU HUỲNH ĐIOXIT
- Công thức hóa học là SO2, tên gọi khác là khí sunfurơ.
1. Tính chất vật lí
Lưu huỳnh đioxit là chất khí không màu, mùi hắc, độc (gây ho, viêm đường hô hấp…), nặng hơn không khí.
2. Tính chất hóa học
Lưu huỳnh đioxit có đầy đủ tính chất hóa học của oxit axit.
a) Tác dụng với nước tạo thành dung dịch axit:
SO2 + H2O → H2SO3 (axit sunfurơ)
SO2 là chất gây ô nhiễm không khí, là một trong các nguyên nhân gây ra mưa axit.
b) Tác dụng với dung dịch bazơ tạo thành muối và nước:
Ví dụ:
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
Khi SO2 dư sẽ tiếp tục có phản ứng sau:
SO2 (dư) + H2O + CaSO3 ↓ → Ca(HSO3)2
Như vậy khi cho SO2 tác dụng với dung dịch bazơ tùy theo tỉ lệ về số mol mà sản phẩm thu được là muối trung hòa, muối axit hoặc hỗn hợp cả hai muối.
c) Tác dụng với oxit bazơ (tan) tạo thành muối:
Ví dụ:
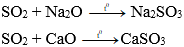
3. Ứng dụng của lưu huỳnh đioxit
- Phần lớn SO2 dùng để sản xuất axit sunfuric (H2SO4).
- Ngoài ra, SO2 còn dùng để làm chất tẩy trắng bột gỗ trong công nghiệp giấy, dùng làm chất diệt nấm mốc,…
4. Điều chế lưu huỳnh đioxit
a) Trong phòng thí nghiệm: Cho muối sunfit tác dụng với axit mạnh như HCl, H2SO4.
Ví dụ:
Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O
Khí SO2 được thu bằng phương pháp đẩy không khí.
b) Trong công nghiệp: Đốt lưu huỳnh hoặc quặng pirit sắt (FeS2) trong không khí.
Ví dụ:
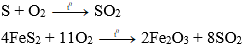
....................................
....................................
....................................

