Lý thuyết Hóa học 9 Bài 36: Metan hay, chi tiết
Lý thuyết Hóa học 9 Bài 36: Metan hay, chi tiết
Haylamdo biên soạn và sưu tầm tóm tắt lý thuyết Hóa học 9 Bài 36: Metan hay, chi tiết nhất sẽ tóm tắt kiến thức trọng tâm bài học từ đó giúp học sinh ôn tập để nắm vững kiến thức môn Hóa 9.

Công thức phân tử metan: CH4
Phân tử khối: 16
I. TRẠNG THÁI TỰ NHIÊN, TÍNH CHẤT VẬT LÍ
Trong tự nhiên, metan có nhiều trong các mỏ khí (khí thiên nhiên), trong mỏ dầu (khí mỏ dầu), trong các mỏ than (khí mỏ than), trong bùn ao (khí bùn ao), trong khí biogas.
Metan là chất khí, không màu, không mùi, nhẹ hơn không khí 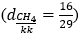
II. CẤU TẠO PHÂN TỬ
Trong phân tử metan chỉ có 4 liên kết đơn
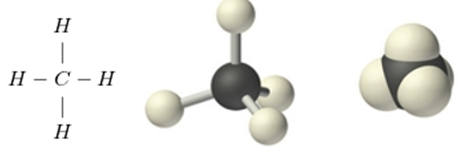
Hình 1: công thức cấu tạo và mô hình phân tử metan dạng rỗng và dạng đặc.
III. TÍNH CHẤT HÓA HỌC
1. Tác dụng với oxi
Khi đốt trong oxi, metan cháy tạo thành khí CO2 và H2O. Phản ứng tỏa nhiều nhiệt.
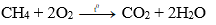
Hỗn hợp gồm 1 thể tích metan và 2 thể tích oxi là hỗn hợp nổ mạnh.
2. Tác dụng với clo khi có ánh sáng
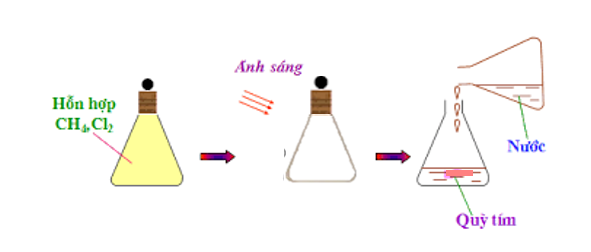
Hình 2: Minh họa thí nghiệm phản ứng của clo với metan.
Phương trình hóa học:
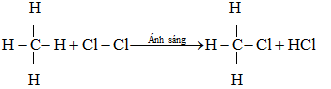
Viết gọn:
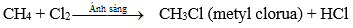
Ở phản ứng này, nguyên tử H của metan được thay thế bởi nguyên tử Cl, vì vậy phản ứng này được gọi là phản ứng thế.
IV. ỨNG DỤNG
- Metan cháy tỏa nhiều nhiệt nên được đùng làm nhiên liệu trong đời sống và trong sản xuất.
- Metan là nguyên liệu dùng điều chế hiđro theo sơ đồ:
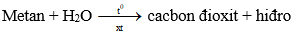
- Metan còn được dùng để điều chế bột than và nhiều chất khác.

