Các dạng bài tập Hóa học 9 Chương 1: Các loại hợp chất vô cơ cực hay, có lời giải
Các dạng bài tập Hóa học 9 Chương 1: Các loại hợp chất vô cơ cực hay, có lời giải
Haylamdo biên soạn và sưu tầm Các dạng bài tập Chương 1: Các loại hợp chất vô cơ cực hay, có lời giải môn Hoá học lớp 9 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Hóa 9.

Dạng 1: Phân loại, gọi tên và viết công thức hóa học các hợp chất vô cơ
Bài tập Phân loại, gọi tên và viết công thức hóa học các hợp chất vô cơ
Dạng 2: Viết phương trình hóa học - Biểu diễn các biến đổi hoá học
Bài tập Viết phương trình hóa học - Biểu diễn các biến đổi hoá học
Dạng 3: Xác định chất phản ứng, hoàn thành phương trình phản ứng
Bài tập xác định chất phản ứng, hoàn thành phương trình phản ứng
Cách viết phương trình hóa học
1. Phản ứng hoá học
Phản ứng hoá học: là quá trình biến đổi chất này thành chất khác.
2. Phương trình hoá học
Phương trình hoá học: biểu diễn ngắn gọn phản ứng hoá học.
◊ 3 bước lập phương trình hoá học:
- B1: Viết sơ đồ của phản ứng (CTHH của chất phản ứng và sản phẩm).
VD: Viết sơ đồ phản ứng: H2 + O2 → H2O
- B2: Cân bằng số nguyên tử mỗi nguyên tố: tìm hệ số thích hợp đặt trước các công thức.
VD: Cân bằng số nguyên tử của mỗi nguyên tố: Thấy vế phải có 1 nguyên tố oxi, vế trái có 2 nguyên tố oxi → Thêm hệ số 2 trước H2O để 2 vế cùng có 2 nguyên tố oxi. Tiếp theo cân bằng số nguyên tố hidro ở 2 vế bằng cách thêm hệ số 2 vào trước H2.
- B3: Viết phương trình hoá học.
VD: Viết phương trình hoá học
2H2 + O2 → 2H2O
Chú ý:
Ở B2, thường sử dụng phương pháp “Bội chung nhỏ nhất” để đặt hệ số bằng cách:
♦ Chọn nguyên tố có số nguyên tử ở hai vế chưa bằng nhau và có số nguyên tử nhiều nhất (cũng có trường hợp không phải vậy).
♦ Tìm bội chung nhỏ nhất của các chỉ số nguyên tử nguyên tố đó ở hai vế, đem bội chung nhỏ nhất chia cho chỉ số thì ta có hệ số.
♦ Trong quá trình cân bằng không được thay đổi các chỉ số nguyên tử trong các công thức hóa học.
Bài tập vận dụng
Bài 1: Viết các phương trình hoá học biểu diễn các phản ứng hoá học ở các thí nghiệm sau:
a) Nhỏ vài giọt axit clohiđric vào đá vôi.
b) Hoà tan canxi oxit vào nước.
c) Nhúng một thanh sắt vào dung dịch đồng(II) sunfat.
Hướng dẫn:
a) 2HCl + CaCO3 → CaCl2 + H2O + CO2.
b) CaO + H2O → Ca(OH)2.
c) Fe + CuSO4 → FeSO4 + Cu.
Bài 2: Có những bazơ sau: Fe(OH)3, Ca(OH)2, KOH, Mg(OH)2. Hãy cho biết những bazơ nào:
a) Bị nhiệt phân huỷ?
b) Tác dụng được với dung dịch H2SO4?
Hướng dẫn:
a) Bazơ bị nhiệt phân huỷ: Fe(OH)3, Mg(OH)2
b) Tác dụng được với dd H2SO4: Fe(OH)3, Ca(OH)2, KOH, Mg(OH)2.
Cách giải bài tập Oxit bazơ tác dụng với axit
Lý thuyết và Phương pháp giải
Oxit bazơ + axit → muối + nước
VD: FeO + H2SO4 → FeSO4 + H2O
CuO + HCl → CuCl2 + H2O
Phương pháp giải bài tập oxit bazơ tác dụng với axit:
- Bước 1: Viết PTHH.
- Bước 2: Tính toán theo PTPU (có thể đặt ẩn).
- Bước 3: Tính toán theo yêu cầu của đề bài.
Bài tập vận dụng
Bài 1: Cho 4,48g oxit bazơ CaO tác dụng vừa đủ với axit H2SO4. Sau khi cô cạn sản phẩm, thu được bao nhiêu gam muối khan?
Hướng dẫn:
- Bước 1: Viết PTHH
CaO + H2SO4 → CaSO4 + H2O
- Bước 2: Tính toán theo PTPU
Theo phương trình phản ứng: nCaO = nCaSO4
Theo đề bài:
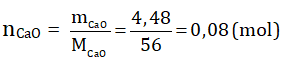
⇒ nCaSO4 = 0,08 (mol)
- Bước 3: Tính toán theo yêu cầu của đề bài
Vậy mmuối khan = mCaSO4 = 0,08.136 = 10,88 (gam)
Bài 2: Hòa tan hoàn toàn 2,81 gam hỗn hợp gồm Fe2O3, MgO, ZnO trong 500 ml H2SO4 0,1 M (vừa đủ). Sau phản ứng, hỗn hợp muối sunfat khan thu được khi cô cạn dung dịch có khối lượng là bao nhiêu?
Hướng dẫn:
♦ Cách 1 (Áp dụng định luật bảo toàn khối lượng)
- Bước 1: Viết PTHH
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O (1)
MgO + H2SO4 → MgSO4 + H2O (2)
ZnO + H2SO4 → ZnSO4 + H2O (3)
- Bước 2+3: Tính toán theo PTPU và tính kết quả theo yêu cầu của đề bài
Từ 3 PTHH trên, ta thấy nH2SO4 = nH2O = 0,1.0,5 =0,05 (mol)
Theo định luật bảo toàn khối lượng, ta có:
moxit + mH2SO4 = mmuối + mH2O
⇒ mmuối =(moxit + mH2SO4) - mH2O= (2,81 + 0,05.98) – 0,05.18 = 6,81 g
Vậy khối lượng muối khan thu được sau phản ứng là 6,81 g
♦ Cách 2 (Phương pháp tăng giảm khối lượng)
Áp dụng tăng giảm khối lượng, ta thấy 1 O được thay thế bởi 1 nhóm SO4:
Fe2O3 → Fe2(SO4)3
MgO → MgSO4
ZnO → ZnSO4
⇒ 1 mol oxit tăng 96-16 = 80 g
⇒ Khối lượng muối sau phản ứng là:
mmuối = moxit + nH2SO4 . 80 =2,81 + 0,1.0,5.80 = 6,81 g
Nhận xét:
-Trong phản ứng của oxit bazơ tác dụng với axit H2SO4 thì nH2SO4 = nH2O
⇒ Tương tự, trong phản ứng của oxit bazơ tác dụng với axit HCl thì nHCl = 2.nH2O
VD: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
-Trong bài toán oxit bazơ tác dụng với axit ta có thể áp dụng phương pháp bảo toàn khối lượng.
moxit + maxit = mmuối + mnước
-Trong bài toán oxit bazơ tác dụng với axit ta có thể áp dụng phương pháp tăng giảm khối lượng.
⇒ Với axit H2SO4, ta có công thức: mmuối = moxit + 80. nH2SO4
⇒ Với axit HCl, ta có công thức: mmuối clorua = moxit + 27,5.nHCl
Bài 3: Hòa tan hoàn toàn 2,8 gam hỗn hợp gồm Fe2O3, MgO, CuO cần dùng 200 ml HCl 0,5M. Hỗn hợp muối clorua khan thu được khi cô cạn dd có khối lượng là bao nhiêu?
Hướng dẫn:
♦ Cách 1 (Áp dụng định luật bảo toàn khối lượng)
Ta biết nHCl = 2.nH2O = 0,5.0,2 = 0,1 (mol)
⇒ nH2O = 0,05 (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
moxit + maxit clohiđric = mmuối clorua + mnước
mmuối clorua = (moxit + maxit clohiđric) - mnước
mmuối clorua = (2,8 + 0,1.36,5) - 0,05.18 = 5,55 g
Vậy khối lượng muối khan thu được là 5,55 g.
♦ Cách 2 (Phương pháp tăng giảm khối lượng)
Ta có: nHCl = 0,2.0,5 = 0,1 mol.
Áp dụng công thức
mmuối clorua = moxit + 27,5.nHCl
mmuối clorua = 2,8 + 27,5.0,1 = 5,55 g
Cách giải bài tập Oxit axit tác dụng với bazo
Lý thuyết và Phương pháp giải
TH1: Khi oxit axit (CO2, SO2…) tác dụng với dung dịch kiềm (KOH, NaOH…)
PTHH:
CO2 + NaOH → NaHCO3 (1)
CO2 + 2NaOH → Na2CO3 + H2O (2)
Phương pháp giải
Bước 1: Xét tỉ lệ: .

- Nếu T ≤ 1 thì sản phẩm thu được là muối axit ⇒ Chỉ xảy ra phản ứng (1)
- Nếu 1 < T < 2 thì sản phẩm thu được là muối axit và muối trung hòa ⇒ Xảy ra cả 2 phản ứng (1) và (2)
- Nếu T ≥ 2 thì sản phẩm thu được là muối trung hòa ⇒ Chỉ xảy ra phản ứng (2).
Bước 2: Viết PTHH và tính toán theo PTHH (nếu xảy ra cả 2 phản ứng thì cần đặt ẩn và giải theo hệ phương trình)
Bước 3: Tính toán theo yêu cầu của đề bài
TH2: Khi oxit axit (CO2, SO2…) tác dụng với dung dịch kiềm thổ (Ca(OH)2, Ba(OH)2…)
PTHH:
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
Phương pháp giải
Bước 1: Xét tỉ lệ: .
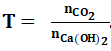
-Nếu T ≤ 1 thì sản phẩm thu được là muối trung hòa ⇒ Chỉ xảy ra phản ứng (1)
-Nếu 1 < T < 2 thì sản phẩm thu được là muối axit và muối trung hòa ⇒ Xảy ra cả 2 phản ứng (1) và (2)
-Nếu T ≥ 2 thì sản phẩm thu được là muối axit ⇒ Chỉ xảy ra phản ứng (2).
Bước 2: Viết PTHH và tính toán theo PTHH (nếu xảy ra cả 2 phản ứng thì cần đặt ẩn và giải theo hệ phương trình).
Bước 3: Tính toán theo yêu cầu của đề bài.trên.
Lưu ý: Nếu không đủ dữ kiện để xét T, ta chia trường hợp có thể xảy ra và giải theo từng trường hợp như các bước ở trên.
Bài tập vận dụng
Bài 1: Nung 20 g CaCO3 và hấp thụ hoàn toàn khí CO2 sinh ra vào 0,5 lit dung dịch NaOH 0,56 M .Tính nồng độ mol của muối thu được. (thể tích thay đổi không đáng kể)
Hướng dẫn:
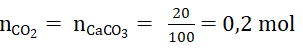
nNaOH = 0,56 . 0.5 = 0,28 mol

Do 1 < 1,4 < 2 ⇒ sản phảm gồm muối axit và muối trung hoà
PTHH:
CO2 + NaOH → NaHCO3 (1)
x x x
CO2 + 2NaOH → Na2CO3 + H2O (2)
y 2y
Đặt số mol CO2 phản ứng ở PT (1), (2) lần lượt là x và y mol.
Ta có hệ phương trình:
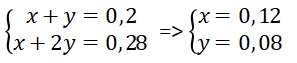
Vậy số mol của NaHCO3 là 0,12 mol.
⇒CM(NaHCO3)= 0,12:0,5 = 0,24 M
Bài 2: Sục từ từ V lít khí SO2 ở đktc vào 100 ml dung dịch Ba(OH)2 1,5M, thu được 23,3 gam kết tủa. Tính giá trị của V.
Hướng dẫn:
Ta có: nBa(OH)2 = 0,15 mol; nBaSO3 = 0,1 mol.
Vì n↓ < nBa(OH)2 nên kết tủa chưa cực đại ⇒ Có các trường hợp sau:
- Trường hợp 1: Ba(OH)2 dư ⇒ muối tạo thành chỉ có BaSO3
PTHH: SO2 + Ba(OH)2 → BaSO3 + H2O
0,1 0,1 (mol)
⇒ VSO2 = 0,1 x 22,4 = 2,24 lít
- Trường hợp 2: SO2 hết nhưng đã hòa tan 1 phần kết tủa.
PTHH: SO2 + Ba(OH)2 → BaSO3 + H2O (1)
0,15 0,15 0,15 (mol)
Theo (1) thì nBaSO3 = 0,15mol, nhưng theo đề thì nBaSO3 = 0,1mol ⇒ nBaSO3 bị hòa tan: 0,15 – 0,05 = 0,1 mol
SO2 + H2O + BaSO3 → Ba(HSO3)2 (2)
0,05 0,05 (mol)
⇒ VSO2 = (0,15 + 0,05) x 22,4 = 4,48 lít

