Lý thuyết Lớp và phân lớp electron - Hoá học lớp 10
Lý thuyết Lớp và phân lớp electron
Tài liệu Lý thuyết Lớp và phân lớp electron Hoá học lớp 10 sẽ tóm tắt kiến thức trọng tâm về Lớp và phân lớp electron từ đó giúp học sinh ôn tập để nắm vứng kiến thức môn Hoá học lớp 10.

I. Lớp electron
- Lớp electron gồm các electron có mức năng lượng gần bằng nhau.
- Các lớp electron xếp theo thứ tự mức năng lượng từ thấp đến cao (từ gần nhân ra ngoài):
| Lớp thứ n | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Tên lớp | K | L | M | N | O | P | Q |
- Lớp K (n = 1) là lớp gần hạt nhân nhất và có năng lượng thấp nhất.
II. Phân lớp electron
- Mỗi lớp electron chia thành các phân lớp s, p, d, f gồm các electron có mức năng lượng bằng nhau.
- Trong 1 lớp electron thì số phân lớp = số thứ tự lớp:
| Lớp thứ | 1 | 2 | 3 | 4 |
| Tên lớp | K | L | M | N |
| Có phân lớp | 1s | 2s2p | 3s3p3d | 4s4p4d4f |
- Phân lớp electron chứa electron tối đa gọi là phân lớp electron bão hòa.

III. Số obitan nguyên tử trong một phân lớp electron
- Trong một phân lớp, các obitan có cùng mức năng lượng, khác nhau về định hướng trong không gian.
| Phân lớp | s | p | d | f |
| Có số obitan | 1 | 3 | 5 | 7 |
| Có số electron tối đa | 2 | 6 | 10 | 14 |
- Phân lớp s: Chỉ có 1 obitan, có đối xứng cầu trong không gian.
- Phân lớp p: Có 3 obitan px, py, pz định hướng theo các trục x, y, z.
- Phân lớp d: Có 5 obtitan, định hướng khác nhau trong không gian.
- Phân lớp f: Có 7 obitan, có định hướng khác nhau trong không gian.
IV. Số obitan nguyên tử trong một lớp electron
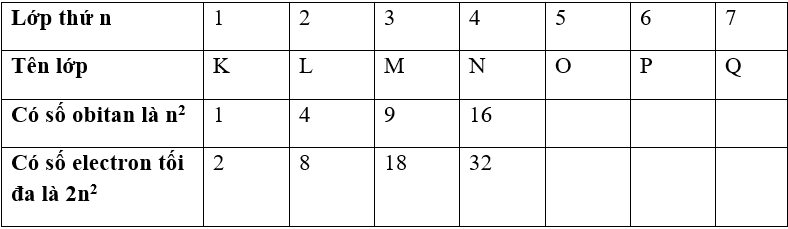
- Số obitan trong lớp eltron thứ n là n2 obitan:
+ Lớp K có 1 obitan 1s.
+ Lớp L có 22 = 4 obitan gồm 1 obitan 2s và 3 obitan 2p.
+ Lớp M có 32 = 9 obitan gồm 1 obitan 3s, 3 obitan 3p và 5 obitan 3d.
+ Lớp L có 42 = 16 obitan gồm 1 obitan 4s, 3 obitan 4p, 5 obitan 4d và 7obitan 4f.