Lý thuyết Oxi - Hoá học lớp 10
Lý thuyết Oxi
Tài liệu Lý thuyết Oxi Hoá học lớp 10 sẽ tóm tắt kiến thức trọng tâm về Oxi từ đó giúp học sinh ôn tập để nắm vứng kiến thức môn Hoá học lớp 10.

I. Cấu tạo phân tử oxi
Nguyên tố oxi có số hiệu nguyên tử là 8, thuộc nhóm VIA, chu kì 2 của bảng tuần hoàn các nguyên tố hoá học.
Nguyên tử oxi có cấu hình electron là 1s22s22p4, lớp ngoài cùng có 6e.
Trong điều kiện bình thường, phân tử oxi có 2 nguyên tử liên kết với nhau bằng liên kết cộng hoá trị không cực.
Công thức cấu tạo của phân tử oxi là O=O.
II. Tính chất vật lý và trạng thái tự nhiên của oxi
1. Tính chất vật lý
Khí oxi không màu, không mùi, không vị, hơi nặng hơn không khí.
Dưới áp suất khí quyển, oxi hoá lỏng ở nhiệt độ -183oC.
Khí oxi tan ít trong nước (100ml nước ở 20oC, 1 atm hoà tan được 3,1ml khí oxi. Độ tan của khí oxi ở 20oC và 1 atm là 0,0043 g trong 100g H2O).
2. Trạng thái tự nhiên
Oxi trong không khí là sản phẩm của quá trình quang hợp.
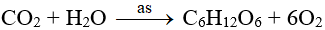
III. Tính chất hóa học của oxi
Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, ...) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
1. Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ au và Pt), cần có to tạo oxit:
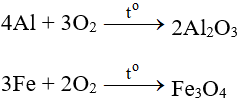
2. Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
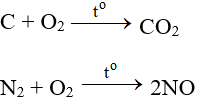
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
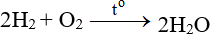
3. Tác dụng với hợp chất
- Tác dụng với các chất có tính khử:
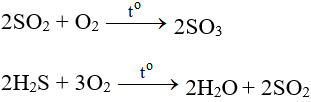
- Tác dụng với các chất hữu cơ:
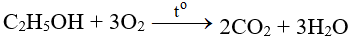

IV. Ứng dụng của oxi
Oxi có vai trò quyết định sự sống của con người và động vật.
Mỗi người mỗi ngày cần 20-30m3 không khí để thở.
V. Điều chế oxi
1. Trong phòng thí nghiệm
Trong phòng thí nghiệm, khí oxi được điều chế bằng cách phân huỷ những hợp chất giầu oxi và ít bền đối với nhiệt như KMnO4 (rắn), KClO3 (rắn), ...
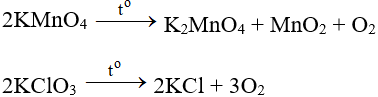
2. Trong công nghiệp
a. Từ không khí: Không khí sau khi đã loại bỏ hết hơi nước, bụi, khí cacbon đioxit, được hoá lỏng. Chưng cất phân đoạn không khí lỏng, thu được oxi. Oxi được vận chuyển trong những bình thép có dung tích 100 lít dưới áp suất 150 atm.
b. Từ nước: Điện phân nước (nước có hoà tan một ít H2SO4 hoặc NaOH để tăng tính dẫn điện của nước), người ta thu được khí oxi ở cực dương và khí hiđro ở cực âm.

