150 câu trắc nghiệm Nitơ, Photpho có lời giải chi tiết (nâng cao) - Hoá học lớp 11
150 câu trắc nghiệm Nitơ, Photpho có lời giải chi tiết (nâng cao)
Với 150 câu trắc nghiệm Nitơ, Photpho có lời giải chi tiết (nâng cao) Hoá học lớp 11 tổng hợp 150 bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Nitơ, Photpho từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

Bài 1: Cho 8,96 lít khí NH3 (ở đktc) đi qua bình đựng 40 gam CuO nung nóng thu được chất rắn X. Cho toàn bộ chất rắn X vào 800 ml dung dịch HCl 1M, sau phản ứng hoàn toàn thì thấy số mol HCl giảm đi một nửa. Hiệu suất của phản ứng khử CuO bởi NH3 là:
A. 50% B. 40% C. 60% D. 33,33%
Lời giải:
Hướng dẫn:
2NH3+ 3CuO → N2+ 3Cu + 3H2O
nNH3= 0,4 mol, nCuO =0,5 mol
Do 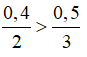
Đặt số mol NH3 phản ứng là x mol
2NH3+ 3CuO → N2+ 3Cu + 3H2O
x 1,5x 1,5x mol
Chất rắn X có chứa 0,5-1,5x mol CuO dư và 1,5xmol Cu
nHCl ban đầu= 0,8mol
CuO + 2HCl→ CuCl2+ H2O
Số mol HCl giảm đi một nửa → nHCl pứ= 0,8/2=0,4 mol
Theo PT: nHCl pứ= 2.n CuO= 2.(0,5-1,5x)=0,4 → x= 0,2 mol
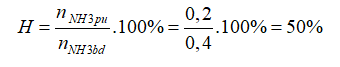
Đáp án A
Bài 2: Cho 4 lít N2 và 12 lít H2 vào bình kín để thực hiện phản ứng tổng hợp NH3. Biết hiệu suất phản ứng là 25%, hỗn hợp thu được sau phản ứng có thể tích là bao nhiêu (các thể tích khí đo trong cùng điều kiện)?
A. 12 lít B. 14 lít C. 16 lít D. 18 lít
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do hiệu suất phản ứng là 25% nên
VN2 pứ= 4.25%= 1 lít; VH2 pứ= 12.25%= 3 lít; VNH3 sinh ra= 2VN2 pứ= 2 lít
VN2 dư= 4-1=3 lít, VH2 dư= 12-3=9 lít
Hỗn hợp thu được sau phản ứng có thể tích là
V= VN2 dư+ VH2 dư+ VNH3 sinh ra= 3 +9+2=14 lít
Đáp án B
Bài 3: Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,0 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25%?
A. 22,4 lít N2 và 67,2 lít H2 B. 22,4 lít N2 và 134,4 lít H2
C. 44,8 lít N2 và 67,2 lít H2 D. 44,8 lít N2 và 134,4 lít H2
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
n2NH3= 1mol
Theo PTHH: nN2 (PT)= ½.nNH3= 0,5 mol; nH2 (PT)= 3/2. nNH3=1,5 mol
Công thức tính hiệu suất:
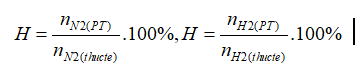
→nN2(thực tế)=2mol; nH2 (thực tế)= 6 mol
→ VN2(thực tế)=44,8 lít; VH2 (thực tế)= 134,4 lít
Đáp án D
Bài 4: Cho 25 lít N2 và 60 lít H2 vào bình phản ứng, hỗn hợp thu được sau phản ứng có thể tích bằng 75 lít (thể tích các khí đo ở cùng điều kiện). Hiệu suất phản ứng là:
A. 20% B. 25% C. 40% D. 50%
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do 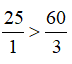
Đặt thể tích H2 phản ứng là x lít
→VN2 pứ= x/3 lít, VNH3 sinh ra=2x/3 lít
VN2 dư= 25-x/3 (lít), VH2 dư= 60- x(lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
V khí= VH2 dư+ VN2 dư+ VNH3= 60-x+ 25-x/3+ 2x/3= 75 → x=15 lít
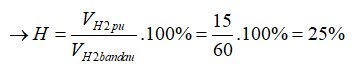
Đáp án B
Bài 5: Một hỗn hợp gồm 8 mol N2 và 16 mol H2 được nạp vào một bình kín có dung tích 4 lít và giữ ở nhiệt độ không đổi. Khi phản ứng đạt trạng thái cân bằng thì áp suất bằng 9/10 áp suất ban đầu. Hiệu suất phản ứng là?
A. 15% B. 17,5% C. 20% D. 22,5%
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
Dựa vào công thức: PV=nRT
Ở nhiệt độ và thể tích không đổi (thể tích bình chứa luôn là 4 lít) và R là hằng số thì áp suất (P) tỉ lệ với số mol (n)
Theo đề áp suất sau bằng 9/10 áp suất ban đầu
→nkhí sau pứ= 9/10.nkhí ban đầu= 9/10. (8+16)= 21,6 mol
nNH3= nkhí trước pứ- nkhí sau pứ= (8+16)- 21,6= 2,4 mol
Vì 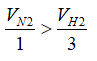
nH2 pứ= 3/2. nNH3= 1,5. 2,4= 3,6 mol
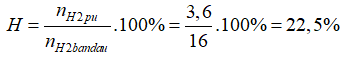
Đáp án D
Bài 6: Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác) thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 3,913. Hiệu suất của phản ứng tổng hợp NH3 là?
A. 15% B. 20% C. 25% D. 30%
Lời giải:
Hướng dẫn:
Giả sử ban đầu hỗn hợp có 1 mol trong đó có x mol N2 và y mol H2
Ta có x + y =1 mol (1)
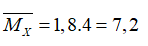
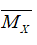
→28x+ 2y= 7,2 gam (2)
Giải hệ gồm (1) và (2) suy ra x= 0,2 và y= 0,8
N2+ 3H2 → 2NH3
Do 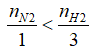
Đặt số mol N2 phản ứng là a mol
N2+ 3H2 → 2NH3
Ban đầu 0,2 0,8 mol
Phản ứng a 3a 2a mol
Sau pứ (0,2-a) (0,8-3a) 2a mol
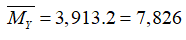
→mY= 28 (0,2-a)+ 2. (0,8-3a) + 17.2a= nY. MY= (1-2a).7,826
→a= 0,04 mol
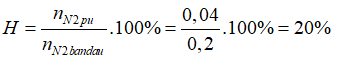
Đáp án B
Bài 7: Cho hỗn hợp gồm N2, H2, NH3 đi qua dung dịch H2SO4 đặc, dư thì thấy thể tích khí còn lại một nửa. Thành phần % theo thể tích của NH3 trong hỗn hợp đầu là bao nhiêu?
A. 25% B. 50% C. 75% D. 90%
Lời giải:
Hướng dẫn:
Cho hỗn hợp gồm N2, H2, NH3 đi qua dung dịch H2SO4 đặc, dư thì chỉ có NH3 phản ứng
2NH3+ H2SO4→ (NH4)2SO4
Sau phản ứng thể tích khí còn một nửa → %VNH3= 50%
Bài 8: Cho 4 lít N2 và 14 lít H2 vào bình phản ứng, hỗn hợp thu được sau phản ứng có thể tích bằng 16,4 lít (các thể tích khí được đo trong cùng điều kiện). Hiệu suất phản ứng là bao nhiêu?
A. 20% B. 30% C. 40% D. 50%
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do 
Đặt thể tích N2 phản ứng là x lít
→VH2 pứ= 3x lít, VNH3 sinh ra=2xlít
VN2 dư= 4-x (lít), VH2 dư= 14-3x (lít)
Sau phản ứng thu được N2 dư , H2 dư , NH3
Tổng thể tích khí thu được là
Vkhí = VH2 dư+ VN2 dư+ VNH3= 14-3x + 4-x+ 2x= 16,4 → x=0,8 lít
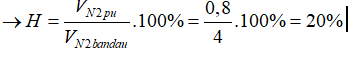
Đáp án A
Bài 9: Điều chế NH 3 từ hỗn hợp gồm N2 dư và H2 dư (tỉ lệ mol 1:3). Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9. Hiệu suất phản ứng là:
A. 20% B. 30% C. 40% D. 50%
Lời giải:
Hướng dẫn:
Ta có 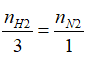
N2+ 3H2 ⇄ 2NH3
Ban đầu a 3a mol
Phản ứng x 3x 2x mol
Sau pứ (a-x) (3a-3x) 2x mol
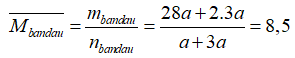
Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9.
→Khối lượng mol của hỗn hợp khí sau phản ứng là 8,5 : 0,9=85/9 (g/mol)
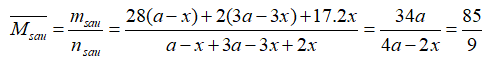
→ x= 0,2a
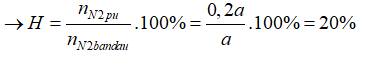
Đáp án A
Bài 10: Trong một bình kín dung tích 56 lít chứa đầy N2 và H2 theo tỉ lệ thể tích 1:4 ở 00C và 200 atm, có một ít bột xúc tác Ni. Nung nóng bình một thời gian, sau đó đưa về 00C thì áp suất trong bình giảm 10% so với áp suất ban đầu. Hiệu suất của phản ứng là:
A. 18,75% B. 20% C. 30% D. 25%
Lời giải:
Hướng dẫn:
Ban đầu: nhỗn hợp= PV/RT= 56.200/0,082.273= 500 mol
→nN2=100 mol, nH2= 400 mol
Ta có 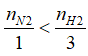
N2+ 3H2 ⇄ 2NH3
Ban đầu 100 400 mol
Phản ứng x 3x 2x mol
Sau pứ (100-x) (400-3x) 2x mol
Sau khi phản ứng xảy ra đưa về 00C thì áp suất trong bình giảm 10% so với áp suất ban đầu
→Số mol khí cũng giảm 10%
→nkhí sau pứ= 500- 10%.500= 450 mol
Mà nkhí sau pứ= (100-x)+ (400-3x)+2x= 450
→x=25 mol
→H= (x/100).100%=25%
Bài 11: Cho 5 lít N2 và 15 lít H2 vào một bình kín dung tích không đổi . Ở 00C, áp suất trong bình là P1 atm. Đun nóng bình một thời gian thấy có 20% N2 tham gia phản ứng, đưa bình về nhiệt độ ban đầu thấy áp suất trong bình lúc này là P2 atm. Tỉ lệ P1 và P2 là:
A. 6 : 10 B. 10: 6 C. 10:9 D. 9: 10
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
Vì có 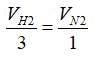
Giả sử ban đầu có 1 mol N2 và 3 mol H2, nkhí ban đầu= 4 mol
→nN2 pứ= 1.20%= 0,2 mol
N2+ 3H2 ⇄ 2NH3
Ban đầu 1 3 mol
Phản ứng 0,2 0,6 0,4 mol
Sau pứ 0,8 2,4 0,4 mol
nkhí sau pứ= 0,8 + 2,4 + 0,4= 3,6 mol
Trong cùng điều kiện nhiệt độ và thể tích thì tỉ lệ về số mol chính là tỉ lệ về áp suất
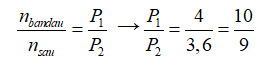
Đáp án C
Bài 12: Một bình kín có thể tích 0,5 lít chứa 0,5 mol H2 và 0,5 mol N2 ở nhiệt độ thích hợp, khi đạt tới trạng thái cân bằng có 0,2 mol NH3 được tạo thành. Hiệu suất của phản ứng là bao nhiêu?
A. 20% B. 30% C. 60% D. 50%
Lời giải:
Hướng dẫn:
N2+ 3H2 ⇄ 2NH3
Vì 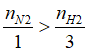
N2+ 3H2 ⇄ 2NH3
Ban đầu 0,5 0,5 mol
Phản ứng x/3 x 2x/3 mol
Sau pứ 0,2 mol
Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành nên 2x/3= 0,2
→x=0,3
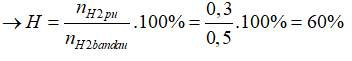
Đáp án C
Bài 13: Một hỗn hợp khí X gồm N2 và H2 có tỉ khối so với hiđro là 4,9. Cho hỗn hợp đi qua xúc tác thích hợp, nung nóng được hỗn hợp mới Y có tỉ khối so với hiđro là 6,125. Hiệu suất tổng hợp NH3 là:
A. 42,85% B. 16,67% C. 40% D. 33,33%
Lời giải:
Hướng dẫn:
Giả sử ban đầu hỗn hợp có 1 mol trong đó có x mol N2 và y mol H2
Ta có x + y =1 mol (1)
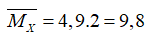
→28x+ 2y= 9,8 gam (2)
Giải hệ gồm (1) và (2) suy ra x= 0,3 và y= 0,7
N2+ 3H2 → 2NH3
Do 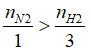
Đặt số mol H2 phản ứng là a mol
N2+ 3H2 → 2NH3
Ban đầu 0,3 0,7 mol
Phản ứng a/3 a 2a/3 mol
Sau pứ (0,3-a/3) (0,7-a) 2a/3 mol
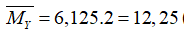
→mY= 28 (0,3-a/3)+ 2. (0,7-a) + 17.2a/3= nY. MY= (1-2a/3).12,25
→49/6a -2,45=0
→a= 0,3 mol
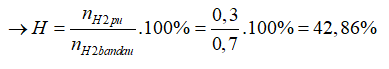
Đáp án A
Bài 14: Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là:
A. 15% và 85% B. 82,35% và 77,5%
C. 25% và 75% D. 22,5% và 77,5%
Lời giải:
Hướng dẫn:
Giả sử có 1 mol hỗn hợp đầu. Gọi x và y (mol) lần lượt là số mol của N2 và H2 trong 1 mol hỗn hợp đầu
Gọi n1, P1 và n2, P2 lần lượt là số mol hỗn hợp khí + áp suất trong bình ban đầu và lúc sau
→ n1 = x + y = 1 (1)
Khi nhiệt độ không đổi
→ n1 / n2 = P1 / P2
Áp suất khí trong bình giảm 5% so với áp suất ban đầu → P1 / P2 = 20 / 19
→ n1/ n2 = 20 / 19 (2)
Số mol của nito đã phản ứng là 10% → N2 pứ 0,1x mol
Phương trình: N2 + 3H2 → 2NH3
Trước: -----------x-------y---------0
Pứ: -------------0,1x---0,3x-----0,2x
Sau: nN₂ = 0,9x ; n H₂ = y - 0,3x ; nNH₃ = 0,2x
→ n2 = 0,9x + y - 0,3x + 0,2x
→ n2 = 0,8x + y (3)
Từ (1) (2) và (3) ta có:
(x + y) / (0,8x + y) = 20 / 19
→ 3x - y = 0 (4)
Giải hệ (1) và (4) cho ta: x = 0,25 mol và y = 0,75 mol
Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là %N₂ = 25% và %H₂ = 75%
Bài 15: Một bình kín dung tích không đổi chứa hỗn hợp cùng thể tích khí N2 và H2 ở 00C, 100 atm. Sau khi tiến hành tổng hợp NH3, đưa nhiệt độ bình về 00C, áp suất mới của bình là 90 atm. Hiệu suất phản ứng tổng hợp NH3 là:
A. 10% B. 25% C. 20% D. 30%
Lời giải:
Hướng dẫn:
Đặt nH2= nN2= a mol (ban đầu) → Tổng số mol khí ban đầu n1= a+a=2a (mol)
Do 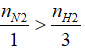
Đặt nH2 pứ= x mol
N2+ 3H2 ⇄ 2NH3
Ban đầu a a mol
Phản ứng x/3 x 2x/3 mol
Sau pứ (a-x/3) (a-x) 2x/3 mol
Tổng số mol khí sau phản ứng n2= (a-x/3) + (a-x) + 2x/3= 2a- 2x/3 (mol)
Trong cùng điều kiện về nhiệt độ, tỉ lệ số mol bằng tỉ lệ áp suất
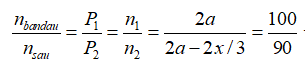
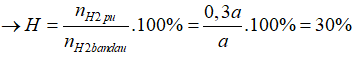
Đáp án D
Bài 16: Nung nóng 0,5 mol hỗn hợp X gồm H2, N2 trong bình kín có xúc tác thích hợp, sau một thời gian thu được hỗn hợp Y. Cho 1/2 hỗn hợp Y đi qua ống sứ đựng CuO dư, nung nóng thấy khối lượng chất rắn trong ống giảm nhiều nhất là 3,2 gam. Tỉ khối hơi của X so với H2 là:
A. 3,9 B. 7,2 C. 3,6 D. 11,4
Lời giải:
Hướng dẫn:
Đặt số mol N2 , H2 ban đầu lần lượt là a, b mol. Ta có a+b= 0,5 (*1)
N2+ 3H2 ⇄ 2NH3 (1)
Ban đầu a b mol
Phản ứng x 3x 2x mol
Sau pứ (a-x) (b-3x) 2x mol
½ hỗn hợp Y chứa (a-x)/2 mol N2, (b-3x)/2 mol H2, x mol NH3
Cho 1/2 hỗn hợp Y đi qua ống sứ đựng CuO dư, nung nóng
2NH3+ 3CuO→ N2+ 3Cu + 3H2O (2)
x 3x/2 x/2 3x/2 3x/2 mol
H2 + CuO → Cu + H2O (3)
(b-3x)/2 (b-3x)/2 (b-3x)/2 mol (b-3x)/2
khối lượng chất rắn trong ống giảm chính là khối lượng oxi trong oxit bị tách ra → mO tách= 3,2 gam
Theo PT (2), (3): nO(tách)= nH2O= 3x/2+ (b-3x)/2= b/2 mol = 3,2/16
→ b=0,4 mol. Từ (*1) ta có a= 0,1 mol
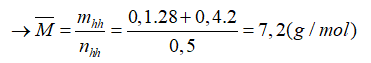
Tỉ khối hơi của X so với H2 là: 7,2/2= 3,6
Đáp án C
Bài 17: Nung nóng hỗn hợp gồm 0,5 mol N2 và 1,5 mol H2 trong bình kín (có xúc tác) rồi đưa về nhiệt độ toC thấy áp suất trong bình lúc này là P1. Sau đó cho một lượng dư H2SO4 đặc vào bình (nhiệt độ lúc này trong bình là t0C) đến khi áp suất ổn định thì thấy áp suất trong bình lúc này là P2 (P1= 1,75P2). Hiệu suất tổng hợp NH3 là:
A. 65% B. 70% C. 50% D. 60%
Lời giải:
Hướng dẫn:
Ta có số mol khí ban đầu là
n = 0,5 + 1,5 = 2 (mol)
Vì có 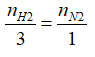
Gọi x là số mol N2 phản ứng. Ta có:
N2 + 3H2 ↔ 2NH3
x .... 3x ...... 2x (mol)
Số mol N2 còn lại là: (0,5 - x) (mol)
Số mol H2 còn lại là: (1,5 - 3x) (mol)
Số mol NH3 sinh ra là: 2x (mol)
=> Số mol ở áp suất P1 là
n1 = (0,5 - x) + (1,5 - 3x) + 2x = (2 - 2x) (mol)
Áp dụng công thức n = PV/RT
Do phản ứng trong bình có thể tích V không đổi , sau phản ứng đưa về nhiệt độ t°C ban đầu nên:
P2/P1 = n2/n1 = số mol sau phản ứng / số mol trước phản ứng (*)
H2SO4 hấp thụ hoàn toàn NH3 theo PT : 2NH3+ H2SO4→ (NH4)2SO4 nên khí sau phản ứng chỉ có N2 và H2 với tổng số mol là :
n2 = (0,5 - x) + (1,5 - 3x) = 2 - 4x
Thay vào (*)
P2/P1 = (2 - 2x) / (0,2 - 4x)
→ P2(2 - 4x) = (2 - 2x)P1
Do P1=1,75P2
→ P2(2 - 4x) = (2 - 2x).1,75P2
→ x = 0,3 (mol)
Hiệu suất phản ứng là:
H% = (0,3/0,5).100% = 60 %
Đáp án D
Bài 18: Muối amoni đicromat bị nhiệt phân theo phương trình:
(NH4)2Cr2O7 →Cr2O3+ N2+ 4H2O
Khi nhiệt phân 48 gam muối này thấy còn 30 gam hỗn hợp chất rắn và tạp chất không bị biến đổi. Phần trăm tạp chất trong muối là:
A. 8,5 B. 6,5 C. 7,5 D. 5,5
Lời giải:
Hướng dẫn:
Đặt n(NH4)2Cr2O7= x mol
(NH4)2Cr2O7 →Cr2O3+ N2+ 4H2O
x x x 4x mol
Khối lượng chất rắn giảm chính là khối lượng N2 và H2O bay hơi
mchất rắn giảm= 28x+ 18.4x= 48-30 (gam)→ x=0,18 mol
→ m(NH4)2Cr2O7=252x=45,36 gam
Phần trăm tạp chất trong muối là: 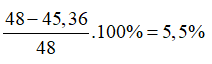
Đáp án D
Bài 19: Có 2 dung dịch A, B . Mỗi dung dịch chỉ chứa 2 cation và 2 anion (không trùng lặp giữa các loại ion) trong số các ion sau: K+ (0,15 mol), H+ (0,2 mol), Mg2+ (0,1 mol), NH4+ (0,25 mol), Cl- (0,1 mol), SO42- (0,075 mol), NO3- (0,25 mol), CO32- (0,15 mol). Làm bay hơi (không xảy ra phản ứng hóa học) của 2 dung dịch A, B thì thu được chất rắn khan lần lượt là:
A. 22,9 gam và 25,3 gam B. 25,4 gam và 25,3 gam
C. 22,9 gam và 12,7 gam D. 25,4 gam và 12,7 gam
Lời giải:
Hướng dẫn:
Nhận thấy Mg2+ và H+ không thể tồn tại cùng với CO32-
→Dung dịch A chứa K+, NH4+, CO32- và ion âm An-
Theo định luật bảo toàn điện tích: 0,15+ 0,25=0,15.2+ n.nAn-
→ n.nAn-= 0,1 mol → Anion còn lại trong dung dịch A là Cl-
→Dung dịch A chứa K+, NH4+, CO32- và Cl-
→mchất rắn khan= 0,15.39 + 0,25.18+ 0,15.60 + 0,1.35,5= 22,9 gam
Dung dịch B chứa H+, Mg2+, SO42- và NO3-
Chú ý khi cô cạn thì axit HNO3 (0,2 mol) sẽ bay hơi cùng nước
→mchất rắn khan= mMg2++ mSO4(2-)+ mNO3- dư= 0,1.24+ 96.0,075+ 0,05.62=12,7 gam
Đáp án C
Bài 20: Hòa tan 1,37 gam Ba vào 30 gam dung dịch (NH4)2SO4 5,38%. Sau khi phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch sau phản ứng giảm m gam. Giá trị của m là:
A. 1,30 gam B. 1,32 gam C. 0,96 gam D. 1,45 gam
Lời giải:
Hướng dẫn:
nBa=0,01 mol, n(NH4)2SO4= 0,0122 mol
Ba+ H2O → Ba(OH)2+ H2↑ (1)
0,01 0,01 0,01 mol
Ba(OH)2+(NH4)4SO4 → BaS04↓ + 2NH3↑+ 2H2O(2)
0,01 0,0122 0,01 0,02
Ta có nBa(OH)2 ❬ n(NH4)2SO4→ Ba(OH)2 hết → Tính theo Ba(OH)2
khối lượng dung dịch sau phản ứng giảm
mdd giảm=(mkết tủa+ mkhí= mBaSO4+ mNH3+ mH2)- mBa
= (233. 0,01+ 0,02.17+0,01.2)- 1,37=1,32 gam
Đáp án B
Bài 21: Nhiệt phân hoàn toàn hỗn hợp X gồm NH4NO3, NH4HCO3 thu được hỗn hợp khí Y có tỉ khối so với H2 là 18,625. Dẫn hỗn hợp Y qua dung dịch Ca(OH)2 dư thấy thu được 10 gam kết tủa. Hàm lượng % của nguyên tố N trong hỗn hợp X là?
A. 12,78% B. 30,45% C. 17,57% D. 29,28%
Lời giải:
Hướng dẫn:
NH4NO3→ N2O + 2H2O (1)
x x mol
NH4HCO3 →NH3+ CO2+ H2O(2)
0,1 0,1 0,1 mol
Khi cho Y qua dung dịch Ca(OH)2 dư thì
CO2+ Ca(OH)2 → CaCO3 ↓ + H2O(3)
0,1← 0,1 mol
→nNH4NO3= nCO2= 0,1 mol
Hỗn hợp Y có x mol N2O, 0,1 mol NH3 và 0,1 mol CO2
MY= 18,625.2=37,25 g/mol
→mY= nY.MY= (x+0,1+0,1).37,25= 44x+ 0,1.17+ 0,1.44
→x=0,2 mol → mX= 0,2.80+0,1.79=23,9 gam
mN=2.nNH4NO3+ nNH4HCO3= 2.0,2+0,1=0,5 mol → mN= 7 gam
→ %mN=29,28%
Đáp án D
Bài 22: Lấy V ml dung dịch HNO3 67% (d=1,4 g/ml) pha loãng bằng nước được dung dịch mới hòa tan vừa đủ 4,5 gam Al và giải phóng hỗn hợp khí X gồm NO và N2O (sản phẩm khử duy nhất) có tỉ khối so với H2 bằng 16,75. Thể tích khí đo ở đktc. Giá trị của V bằng:
A. 22,33 ml B. 23,23 ml C. 44,33 ml D. 43,46 ml
Lời giải:
Hướng dẫn:
nAl=1/6 mol. Đặt nNO= xmol; nN2O= y mol
Quá trình cho e :
Al → Al3++ 3e
1/6→ 0,5 mol
Quá trình nhận e :
NO3-+ 3e+ 4H+ → NO + 2H2O
3x 4x← x mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O
8y 10y← y mol
Theo ĐL bảo toàn electron: 0,5= 3x+8y (1)
M2X=16,75.2=33,5
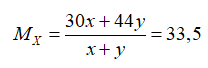
Giải hệ ( 1) và (2) ta có x=3/34 ; y=1/34
→nH+= 4x+10y=11/17 mol= nHNO3→ mHNO3=693/17 gam
→mdd HNO3=60,843 gam → Vdd= mdd/d=43,46 ml
Bài 23: Cho 3,76 gam hỗn hợp X gồm Mg và MgO có tỉ lệ mol tương ứng là 14:1 tác dụng hết với dung dịch HNO3 thì thu được 0,448 lít một khí duy nhất (đo ở đktc) và dung dịch Y. Cô cạn cẩn thận dung dịch Y thu được 23 gam chất rắn khan T. Xác định số mol HNO3 đã phản ứng:
A. 0,28 B. 0,36 C. 0,32 D. 0,34
Lời giải:
Hướng dẫn:
Đặt số mol Mg là 14 x mol và MgO là x mol
→mhỗn hợp=14x.24+40x=3,76 gam→ x=0,01 mol
Bảo toàn nguyên tố Mg ta có : nMg(NO3)2= nMg+ nMgO=14x+x=0,15 mol
→ mMg(NO3)2=22,2 gam ❬ mT → T phải chứa NH4NO3
→ mNH4NO3= 23-22,2=0,8 gam → nNH4NO3=0,01 mol
nkhí=0,02 mol. Giả sử số oxi hóa của N trong sản phẩm khí là a
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,14→ 0,28 mol
Quá trình nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (2)
0,08 0,1 0,01 mol
-Nếu khí có 1 nguyên tử N:
N+5 + (5-a) e→ N+a
(5-a).0,02 0,02
Theo ĐL bảo toàn electron có: 0,28= 0,08 + 0,02. (5-a)→ a= -5 loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,04 0,02
Theo ĐL bảo toàn electron có: 0,28= 0,08 + 0,04. (5-a)→ a= 0→ Khí là N2
2NO3-+ 10e+12H+→ N2+ 6H2O (3)
0,24 0,02
TheoPT (2) và (3):
nH+= 10nNH4++ 12nN2= 0,1+0,24= 0,34 mol= nHNO3 pứ với Mg
MgO + 2HNO3→ Mg(NO3)2+H2O
0,01 0,02
Vậy tổng số mol HNO3 phản ứng là 0,34+ 0,02= 0,36 mol
Đáp án B
Bài 24: Hòa tan 12 gam Mg trong V (lít ) dung dịch HNO3 2M thu được 2,24 lít khí N2O (đktc) và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 74 B. 76 C. 70 D. 72
Lời giải:
Hướng dẫn:
nMg=0,5 mol= nMg(NO3)2, nN2O= 0,1 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,5→ 1 mol
Quá trình nhận e:
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,8 1,0 0,1 mol
Do số mol e cho ở (1) khác số mol e nhận ở (2) nên phải có quá trình tạo NH4+
Theo ĐLBT e: necho= ne nhận= 1 mol → ne nhận ở (3)= 1-0,8=0,2 mol
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,2 0,25 0,025 mol
Vậy cô cạn X thu được 2 muối là 0,5 mol Mg(NO3)2 và 0,025 mol NH4NO3→m=76 gam
Đáp án B
Bài 25: Cho 9,55 gam hỗn hợp gồm Mg, Al và Zn tác dụng vừa đủ với 870 ml dung dịch HNO3 1M thu được dung dịch chứa m gam muối và 0,06 mol hỗn hợp khí N2 và N2O. Tỉ khối của hỗn hợp khí so với H2 là 20,667. Giá trị của m là:
A. 54,95 B. 42,55 C. 40,55 D. 42,95
Lời giải:
Hướng dẫn:
nHNO3pu= 0,87 mol
Đặt số mol N2 là x mol; số mol N2O là y mol
→x+y=0,06
mhỗn hợp= 28x+44y= 0,06.20,667.2=2,48 gam
Giải hệ trên được x=0,01 ; y= 0,05
2NO3-+ 8e+ 10H+ → N2O + 5H2O (1)
0,4 0,5 ← 0,05 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (2)
0,12← 0,01
Theo PT (1), (2): nH+= 0,5+0,12= 0,62 mol= nHNO3
Mà đề cho nHNO3pu= 0,87 mol
→Có phản ứng tiếp :
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,2 0,25 0,025 mol
nH+ pứ 3= 0,87- 0,62= 0,25 mol
bảo toàn nguyên tố H: nH (HNO3)= nH(NH4NO3)+ nH(H2O)
→0,87= 0,025.4+ 2.nH2O→ nH2O=0,385 mol
Áp dụng định luật bảo toàn khối lượng:
mkim loại+ mHNO3= m +mkhí+ mH2O
↔ 9,55+ 0,87.63=m+2,48 + 0,385.18 → m=54,95 gam
Đáp án A
Bài 26: Cho 9,6 gam kim loại R tác dụng với 500 ml dung dịch HNO3 cM vừa đủ thu được 2,24 lít khí A (sản phẩm khử duy nhất, đktc) và dung dịch B. Cô cạn dung dịch B thu được 59,2 gam muối khan. A là khí nào đây?
A. NH4NO3 B. NO C. NO2 D. N2O
Lời giải:
Hướng dẫn:
Do khí A là sản phẩm khử duy nhất nên muối khan chỉ có R(NO3)n (n là hóa trị cao nhất của kim loại R)
Ta luôn có nR= nR(NO3)n nên
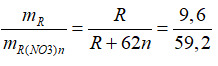
→R=12n
Vì n chỉ nhận giá trị 1, 2, 3 nên ta thấy chỉ có n=2, R=24(Mg) là thỏa mãn
nMg=0,4mol, nkhí= 0,1mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,4→ 0,8 mol
Quá trình nhận e:
-Nếu khí có 1 nguyên tử N:
N+5 + (5-a) e→ N+a
(5-a).0,1 0,1
Theo ĐL bảo toàn electron có: 0,8= 0,1. (5-a)→ a= -3 loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,2 0,1
Theo ĐL bảo toàn electron có: 0,8= 0,2. (5-a)→ a= 1→ Khí là N2O
Đáp án D
Bài 27: Hòa tan 5,95 gam hỗn hợp Zn, Al có tỉ lệ mol 1:2 bằng dung dịch HNO3 loãng dư thu được 0,896 lít một sản phẩm khử X duy nhất chứa nitơ. Sản phẩm X là:
A. N2O B. N2 C. NO D. NO2
Lời giải:
Hướng dẫn:
Ta tính được nZn= 0,05 mol, nAl= 0,1 mol, nkhí= 0,04 mol
Quá trình cho e:
Zn→ Zn2++ 2e (1)
0,05→ 0,1 mol
Al→ Al3++ 3e (1)
0,1→ 0,3 mol
→Tổng số mol e cho là 0,4 mol
Quá trình nhận e:
-Nếu khí có 1 nguyên tử N:
N+5 + (5-a) e→ N+a
(5-a).0,04 0,04
Theo ĐL bảo toàn electron có: 0,4= 0,04. (5-a)→ a= -5 loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,08 0,04
Theo ĐL bảo toàn electron có: 0,4= 0,08. (5-a)→ a= 0→ Khí là N2
Đáp án B
Bài 28: Hòa tan hoàn toàn m gam kim loại X bằng 200 ml dung dịch HNO3 loãng, lạnh vừa đủ thu được dung dịch Y. Cho Y tác dụng với lượng dư dung dịch NaOH, đun nhẹ thấy có 224 ml khí (đktc). Nồng độ mol của dung dịch HNO3 là:
A. 0,05 B. 0,3 C. 0,5 D. 1,0
Lời giải:
Hướng dẫn:
X+ HNO3→ Dung dịch Y
Dung dịch Y + NaOH→ Khí
→Dung dịch Y phải có NH4NO3
NH4NO3+ NaOH → NaNO3+ NH3↑ + H2O
0,01← 0,01 mol
QT nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,1 0,01 mol
nHNO3= nH+= 0,1 mol →CMHNO3 = 0,1/0,2= 0,5 (M)
Đáp án C
Bài 29: Chia m gam hỗn hợp gồm 3 kim loại Mg, Al, Cu thành 2 phần bằng nhau:
-Phần 1: Cho tác dụng với dung dịch HNO3 đặc nóng dư thu được 10,528 lít khí NO2 (sản phẩm khử duy nhất).
-Phần 2: Tác dụng vừa đủ với Cl2 thu được 27,875 gam hỗn hợp muối clorua.
Khối lượng m gam hỗn hợp kim loại là:
A. 22,38 gam B. 11,19 gam C. 44,56 gam D. 5,628 gam
Lời giải:
Hướng dẫn:
QT cho e: Xét với ½ khối lượng hỗn hợp
Mg→ Mg2++ 2e (1)
x 2x mol
Al→ Al3++ 3e (2)
y 3y mol
Cu→ Cu2++ 2e (3)
z 2z mol
→ne cho= 2x+ 3y+2z mol
QT nhận e:
-Phần 1: nNO2=0,47 mol
N+5+ 1e→ NO2
0,47 0,47 mol
Theo ĐL bảo toàn e: ne cho= 2x+ 3y+2z = ne nhận= 0,47
-Phần 2:
Cl2+ 2e→ 2Cl-
0,47 0,47
Theo ĐL bảo toàn e: ne cho= 2x+ 3y+2z = ne nhận= 0,47
mmuối clorua= mkim loại+ mCl-= mkim loại+ 0,47.35,5=27,875 → mkim loại=11,19 gam → m= 11,19.2=22,38 gam
Bài 30: Hòa tan 6,21 gam kim loại M trong V ml dung dịch HNO3 0,2M vừa đủ thu được 1,68 lít hỗn hợp khí X (ở đktc) gồm 2 khí không màu, không hóa nâu ngoài không khí (không còn sản phẩm khử nào khác). Tỉ khối hơi của X so với H2 là 17,2. Kim loại M và giá trị của V là:
A. Al và 8,4 lít B. Mg và 8,4 lít
C. Mg và 4,2 lít D. Al và 4,2 lít
Lời giải:
Hướng dẫn:
X gồm 2 khí không màu, không hóa nâu ngoài không khí và là sản phẩm khử của N nên X là N2, N2O
Đặt nN2= x mol; nN2O= y mol
Ta có nX= x+ y= 0,075 mol
mX= nX.MX= 0,075.17,2.2= 28x+ 44y
Giải hệ trên có : x= 0,045 ; y=0,03
QT nhận e :
2NO3-+ 8e+ 10H+ → N2O + 5H2O (1)
0,24 0,3 ← 0,03 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (2)
0,45 0,54← 0,045
Theo PT (1), (2): nH+= 0,3+0, 54= 0,84 mol= nHNO3→ VddHNO3 = 4,2 lít
QT cho e:
M → Mn++ ne
0,69/n 0,69 mol
Theo ĐL bảo toàn e : ne cho = ne nhận= 0,24+0,45= 0,69 mol
MM= mM/nM= 6,21 : 0,69/n=9n
Xét n=1, 2, 3 thì thấy chỉ có n=3, M=27 (Al) thỏa mãn
Đáp án D

Bài 31: Cho 4,86 gam bột nhôm tác dụng với lượng dư dung dịch HNO2. Sau khi phản ứng kết thúc thu được 2,24 lít khí NO (đktc) và dung dịch X.
Đem cô cạn cẩn thận dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 40,74 B. 21,3 C. 38,34 D. 23,46
Lời giải:
Hướng dẫn:
Ta có: nAl= 0,18 mol= nAl(NO3)3; nNO= 0,1 mol
QT cho e :
Al→ Al3++ 3e (1)
0,18 0,54 mol
QT nhận e :
N+5+ 3e → NO (2)
0,3 0,1
Nếu chỉ có quá trình nhận e (2) thì số mol e cho khác số mol e nhận
Do đó phải có quá trình :
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,24→ 0,03
Theo ĐL BT e : ne cho= ne nhận nên 0,54= 0,3+ ne nhận ở quá trình 3
→ ne nhận ở quá trình 3= 0,24 mol
Muối khan thu được có Al(NO3)3 : 0,18 mol; NH4NO3: 0,03 mol
→m=0,18. 213 + 0,03.80=40,74 gam
Đáp án A
Bài 32: Cho một lượng Al phản ứng vừa đủ với 2 lít dung dịch HNO3 nồng độ a M, thu được 0,2 mol N2 và dung dịch X. Cho NaOH dư vào dung dịch X, đun nóng thu được 0,1 mol khí. Giá trị của a là:
A. 1,4M B. 3,4M C. 2,8M D. 1,7M
Lời giải:
Hướng dẫn:
Cho NaOH dư vào dung dịch X, đun nóng thu được 0,1 mol khí.
→Dung dịch X có chứa NH4NO3
NH4NO3+ NaOH → NaNO3+ NH3↑ + H2O
0,1← 0, 1 mol
QT nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (1)
1,0 0,1 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (2)
2,4← 0,2mol
Theo 2 bán phản ứng (1), (2):
nH+= 10nNH4++ 12.nN2= 10.0,1+ 12.0,2= 3,4 mol=nHNO3
→a= 3,4/2=1,7M
Bài 33: Hòa tan 1,68 gam kim loại Mg vào V lít dung dịch HNO3 0,25M vừa đủ thu được dung dịch X và 0,448 lít một chất khí Y duy nhất. Cô cạn cẩn thận dung dịch X thu được 11,16 gam muối khan. Công thức phân tử của khí Y và thể tích dung dịch HNO3 đã dùng là:
A. NO và 0,32 lít B. NO và 0,72 lít
C. N2O và 0,32 lít D. N2O và 0,72 lít
Lời giải:
Hướng dẫn:
nMg= 0,07 mol=nMg(NO3)2 → mMg(NO3)2= 0,07. 148= 10,36 gam≠ 11,16 gam
→Muối khan phải chứa cả Mg(NO3)2 và NH4NO3
mNH4NO3=11,16- 10,36= 0,8 gam →nNH4NO3= 0,01 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,07→ 0,14 mol
Quá trình nhận e: nkhí= 0,02mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (2)
0,08 0,1 0,01 mol
-Nếu khí có 1 nguyên tử N:
N+5 + (5-a) e→ N+a
(5-a).0,02 0,02
Theo ĐL bảo toàn electron có: 0,14= 0,02. (5-a)+0,08→ a= 2 → NO
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,04 0,02
Theo ĐL bảo toàn electron có: 0,14= 0,04. (5-a) + 0,08→ a= 3,5 loại
Ta có:
NO3-+ 3e+4H+→ NO+ 2H2O (3)
0,06 0,08 0,02 mol
Theo các bán phản ứng (2) và (3)
nH+= 10nNH4++ 4.nNO= 10.0,01+ 4.0,02= 0,18 mol=nHNO3
→V= 0,18/0,25= 0,72 lít
Đáp án B
Bài 34: Cho m gam Al phản ứng vừa đủ với dung dịch có chứa 0,58 mol HNO3 thu được hỗn hợp gồm 0,03 mol N2O và 0,02 mol NO. Giá trị của m là:
A. 2,7 B. 16,2 C. 27 D. 4,14
Lời giải:
Hướng dẫn:
QT cho e :
Al→ Al3++ 3e (1)
QT nhận e:
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,24 0,3 ← 0,03 mol
NO3-+ 3e + 4H+→ NO+ 2H2O (4)
0,06 0,08 ← 0,02
Theo bán phản ứng (3) và (4) ta có:
nH+= 10.nN2O+ 4.nNO= 10.0,03 + 4.0,02= 0,38 mol≠ 0,58 mol
Do đó còn có thêm quá trình nhận e tạo NH4+
NO3-+ 8e + 10H+ → NH4+ + 3H2O (5)
0,16 ← 0,2
nH+ pt5= 0,58- 0,38= 0,2 mol
Theo bán phản ứng (3), (4), (5) ta có:
ne nhận= 8. nN2O+ 3.nNO+ 8/10.nH+= 0,24+ 0,06+ 0,16= 0,46 mol
Theo ĐL bảo toàn e : ne cho= ne nhận= 0,46 mol → nAl= 0,46/3 mol
→mAl= 4,14 gam
Đáp án D
Bài 35: Hòa tan hoàn toàn 7,15 gam kim loại M hóa trị 2 vào lượng dư dung dịch HNO3 loãng, thu được 0,448 lít(đktc) hỗn hợp 2 khí không màu, không hóa nâu trong không khí (số mol hai khí bằng nhau) và dung dịch chứa 21,19 gam muối. Kim loại M là:
A. Fe B. Ca C. Mg D. Zn
Lời giải:
Hướng dẫn:
2 khí không màu, không hóa nâu trong không khí và là sản phẩm khử của N+5 chỉ có thể là N2 và N2O
-TH1: 21,19 gam muối không có muối NH4NO3
Theo bảo toàn nguyên tố M ta có: n3M= nM(NO3)2
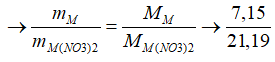
→M= 63,148 Loại
Do đó trường hợp này loại
-TH2: 21,19 gam muối có muối NH4NO3
QT cho e:
M → M2++ ne (1)
7,15/M 7,15.2/M
QT nhận e : nkhí= 0,02 mol. Mà số mol hai khí bằng nhau nên nN2O= nN2=0,01mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,08 0,1 ← 0,01 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (3)
0,1 0,12← 0,01 mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (4)
8x xmol
Đặt số mol muối NH4+ là x mol
Theo ĐL BT e: ne cho= ne nhận nên 7,15.2/M= 0,08 + 0,1+8x (*1)
Mặt khác : mmuối= mM(NO3)2+ mNH4NO3= 7,15/M. (M+124)+80x= 21,19 (*2)
Từ (*1) và (*2) ta có: x= 5.10-3 và M=65. M là Zn
Đáp án D
Bài 36: Khi cho 26,4 gam Mg tác dụng hết với dung dịch HNO3 dư thấy thoát ra 8,96 lít hỗn hợp X gồm hai khí có tỉ lệ mol 1:1, trong đó có một khí màu nâu (phản ứng không tạo muối amoni, khí đo ở đktc). Xác định các khí có trong X.
A. NO và NO2 B. N2 và N2O
C. NO2 và N2 D. NO2 và N2O
Lời giải:
Hướng dẫn:
Ta có: nMg= 1,1 mol; nX= 0,4 mol
Hỗn hợp X có 1 khí màu nâu nên phải chứa NO2
Số mol mỗi khí trong X là 0,2 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
1,1→ 2,2 mol
Quá trình nhận e:
NO3-+ 1e + 2H+ → NO2 + H2O (2)
0,2 ← 0,2mol
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí
N+5 + (5-a) e→ N+a
(5-a).0,2 0,2
Theo ĐL bảo toàn electron có: 2,2= 0,2. (5-a)+0,2→ a= -5 → Loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0, 4 0,2
Theo ĐL bảo toàn electron có: 2,2= 0,4. (5-a) + 0,2→ a= 0→ Khí là N2
Vậy trong X chứa NO2 và N2
Đáp án C
Bài 37: Hòa tan 12 gam Mg trong V ml dung dịch HNO3 2M vừa đủ thu được 2,24 lít khí N2O (đktc) và dung dịch X. Giá trị của V là:
A. 500 B. 600 C. 625 D. 725
Lời giải:
Hướng dẫn:
nMg=0,5 mol= nMg(NO3)2, nN2O= 0,1 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,5→ 1 mol
Quá trình nhận e:
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,8 1,0 0,1 mol
Do số mol e cho ở (1) khác số mol e nhận ở (2) nên phải có quá trình tạo NH4+
Theo ĐLBT e: necho= ne nhận= 1 mol → ne nhận ở (3)= 1-0,8=0,2 mol
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,2 0,25 0,025 mol
Theo bán phản ứng (2) và (3) ta có
nH+= nH+PT 2+ nH+PT3= 1 + 0,25= 1,25 mol→ V= 1,25/2= 0,625 lít= 625 ml
Đáp án C
Bài 38: Hòa tan 0,03 mol FexOy trong dung dịch HNO3 dư thấy sinh ra 0,672 lít khí X duy nhất (đktc). X là:
A. NO2 B. NO C. N2O D. N2
Lời giải:
Hướng dẫn:
QT cho e:
FexOy → xFe+3+ (3x-2y) e
0,03 0,03(3x-2y) mol
QT nhận e: n2khí X= 0,03 mol
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí
N+5 + (5-a) e→ N+a
(5-a).0,03 0,03
Theo ĐL bảo toàn electron có:
0,03 (3x-2y)= 0,03 (5-a)
Nếu x=y=1 thì a= 4→ NO2
Nếu x=3, y=4 thì a= 4→ NO2
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,06 0,03
Theo ĐL bảo toàn electron có:
0,03(3x-2y)= (5-a).0,06 hay 3x-2y= 2(5-a)
Nếu x=y=1 thì a= 4,5 Loại
Nếu x=3, y=4thì a= 4,5 Loại
Vậy X là NO2
Đáp án A
Bài 39: Hòa tan hoàn toàn 21,6 gam kim loại M vào dung dịch HNO3 thu được dung dịch D và không có khí thoát ra. Cho dung dịch D tác dụng với dung dịch NaOH dư, đun nóng thu được 6,72 lít khí (đktc). M là kim loại nào dưới đây?
A. Fe B. Al C. Cu D. Mg
Lời giải:
Hướng dẫn:
X+ HNO3→ Dung dịch D
Dung dịch D + NaOH→ Khí
→Dung dịch D phải có NH4NO3
NH4NO3+ NaOH → NaNO3+ NH3↑ + H2O
0,3← 0,3 mol
QT nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
2,4 0,3 mol
ne nhận= 8nNH4+= 2,4 mol
QT cho e: Gọi số oxi hóa cao nhất của kim loại M là n (n=1,2,3)
M → Mn++ ne
Theo ĐLBT e : ne cho= ne nhận nên ne cho= 2,4 mol → nM= 2,4/ n mol
→M3M= m3M: n3M= 21,6: 2,4/n=9n
Thay các giá trị n và M ta thấy chỉ có n=3, M=27 thỏa mãn
Vậy M là Al.
Đáp án B
Bài 40: Hòa tan hoàn toàn 1,35 gam Al bằng dung dịch HNO3 thoát ra 336 ml khí X (đktc) là sản phẩm khử duy nhất. Công thức phân tử của khí X là:
A. N2 B. N2O C. NO D. NO2
Lời giải:
Hướng dẫn:
Quá trình cho e: nAl= 0,05mol
Al→ Al3+ + 3e (1)
0,05→ 0,15 mol
Quá trình nhận e: nkhí X= 0,015 mol
-Nếu khí X có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí
N+5 + (5-a) e→ N+a
(5-a).0,015 0,015
Theo ĐL bảo toàn electron có: 0,15= 0,015. (5-a)→ a= -5 → Loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a). 0,03 0,015
Theo ĐL bảo toàn electron có: 0,15= 0,03. (5-a) → a= 0→ Khí X là N2
Đáp án A
Bài 41: Cho hỗn hợp gồm 0,14 mol Mg và 0,01 mol MgO phản ứng vừa đủ với dung dịch HNO3 thu được 0,448 lít (đktc) khí N2 và dung dịch X. Khối lượng muối trong X là:
A. 23 gam B. 24,5 gam
C. 22,2 gam D. 20,8 gam
Lời giải:
Hướng dẫn:
Bảo toàn nguyên tố Mg ta có : nMg(NO3)2= nMg+ nMgO=0,15 mol
nkhí N2=0,02 mol.
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,14 → 0,28 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,2 ← 0,02 mol
Nểu chỉ có 1 quá trình nhận e (2) thì số mol e cho khác số mol e nhận
Do đó phải có quá trình nhận e (3) và số mol e nhận ở (3) bằng:
0,28- 0,2=0,08 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (3)
0,08 → 0,01 mol
Muối trong X gồm 0,15 mol Mg(NO3)2 và 0,01 mol NH4NO3
→mmuối= 0,15.148+ 0,01.80=23 gam
Đáp án A
Bài 42: Cho 15,6 gam hỗn hợp X gồm Mg và Al hòa tan hết trong V lít dung dịch HNO3 1M vừa đủ thu được 3,136 lít hỗn hợp N2O và N2 (có tỉ lệ thể tích là 5:2 và ở đktc) và dung dịch Z chứa 118,8 gam muối. Thể tích HNO3 cần dùng là:
A. 1,88 lít B. 1,98 lít C. 1,74 lít D. 2,28 lít
Lời giải:
Hướng dẫn:
Ta có nhỗn hợp khí= 0,14 mol
Vì tỉ lệ thể tích chính là tỉ lệ số mol (trong cùng điều kiện)
Nên nN2O : nN2= 5 :2 do đó nN2O = 0,1 và nN2= 0,04 mol
2NO3-+ 8e+ 10H++ 8NO3- → N2O + 5H2O + 8NO3(muối)-(1)
0,8 1,0 ← 0,1mol → 0,8 mol
2NO3-+ 10e+ 12H++ 10NO3- → N2 + 6H2O + 10NO3 muối- (2)
0,4 0,48 0,04 0,4 mol
Gọi nMg=a mol ; nAl =b mol
mhhX =24a+27b=15,6 (1)
Gỉa sử muối tạo thành không có NH4NO3
ne nhường=nenhận =2a+3b=0,1.2.4+0,04.2.5=1,2 (2)
Giải hệ (1) và (2) trên ta có b ⟨ 0 nên loại
Vậy muối tạo thành có NH4NO3 c mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (3)
8c → c mol
Tổng nNO3− tạo muối =ne nhường=8c+1,2=2a+3b (3)
mmuối =mAl(NO3)3 +mMg(NO3)2+mNH4NO3
=213b+148a+80c=118,8 (4)
Giải hệ (1), (3) và (4) ta có a=0,2 b=0,4, c=0,05 mol
Bảo toàn Nitơ ta có:
nHNO3=0,1.2+0,04.2+0,05.2+0,2.2+0,4.3=1,98 mol
→V=1,98 lít
Đáp án B
Bài 43: Hòa tan hoàn toàn 12,15 gam Al bằng dung dịch HNO3 loãng (dư) thu được dung dịch X và 1,344 lít (đktc) hỗn hợp khí Y gồm hai khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là:
A. 103,95 B. 106,65 C. 45,63 D. 95,85
Lời giải:
Hướng dẫn:
Đặt nN2O= x mol; nN2= y mol
Ta có nhhY= x+y= 1,344/ 22,4= 0,06 mol
mhhY=44x + 28y= 0,06.18.2
Giải hệ trên được x= 0,03 và y= 0,03
nAl= 0,45 mol= nAl(NO3)3
Quá trình cho e:
Al→ Al3++ 3e (1)
0,45 → 1,35 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,3 ← 0,03 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,24 ← 0,03 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,3+ 0,24= 0,54 mol ⟨1,35 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 1,35- 0,54= 0,81 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,81 → 0, 10125 mol
Dung dịch X chứa 0,45 mol Al(NO3)3 và 0,10125 mol NH4NO3
→m=103,95 gam
Đáp án A
Bài 44: Cho 12 gam Mg tác dụng với dung dịch HNO3 vừa đủ thu được dung dịch A và V lít hỗn hợp khí (đktc) gồm N2O và N2 có tỉ khối so với H2 bằng 18. Cô cạn cẩn thận toàn bộ dung dịch A thu được 75 gam muối khan. Giá trị của V là:
A. 2,48 B. 2,016 C. 2,24 D. 2,688
Lời giải:
Hướng dẫn:
nMg=0,5 mol= nMg(NO3)2,
→ mMg(NO3)2= 0,5. 148= 74 gam ⟨75 gam → Muối khan chứa Mg(NO3)2 và NH4NO3
mNH4NO3= 75-74= 1gam → nNH4NO3= 0,0125 mol
Đặt nN2O= x mol, nN2= y mol, M hỗn hợp khí=36
Theo sơ đồ đường chéo suy ra x = y
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,5 → 1 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
10x x mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
8x ← x mol
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (4)
0,1 0,0125 mol
Theo ĐLT BT e: ne cho= ne nhận nên 1= 10x+ 8x+ 0,1→ x= 0,05 mol
→V= (0,05+0,05).22,4= 2,24 lít
Đáp án C
Bài 45: Hòa tan hoàn toàn hỗn hợp X gồm 0,2 mol Mg và 0,03 mol MgO bằng dung dịch HNO3 thu được dung dịch Y và 0,896 lít một chất khí Z nguyên chất duy nhất. Cô cạn cẩn thận dung dịch Y thu được 34,84gam muối khan. Xác định công thức phân tử của Z?
A. N2 B. N2O C. NO2 D. NO
Lời giải:
Hướng dẫn:
Bảo toàn nguyên tố Mg ta có:
nMg(NO3)2= 0,2+ 0,03= 0,23 mol → mMg(NO3)2= 0,23. 148= 34,04 gam≠ 34,84 gam
→Muối khan phải chứa cả Mg(NO3)2 và NH4NO3
mNH4NO3=34,84- 34,04= 0,8 gam →nNH4NO3= 0,01 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,2→ 0, 4 mol
Quá trình nhận e: nkhí= 0,04mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (2)
0,08 0,1 0,01 mol
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí
N+5 + (5-a) e→ N+a
(5-a).0,04 0,04
Theo ĐL bảo toàn electron có: 0,4= 0,04. (5-a)+0,08→ a= -3 → Loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,08 0,04
Theo ĐL bảo toàn electron có: 0, 4= 0,08. (5-a) + 0,08→ a= 1→Khí N2O
Đáp án B
Bài 46: Lấy 15,7 gam hỗn hợp Al, Zn (tỉ lệ mol 1:2) tác dụng với dung dịch HNO3 dư thì thu được 15,68 lít (đktc) khí X là sản phẩm khử duy nhất. Xác định X?
A. NO2 B. N2 C. NO D. N2O
Lời giải:
Hướng dẫn:
Đặt số mol nAl=x mol, nZn= 2x mol→ 27x+ 65.2x=15,7 → x= 0,1 mol
Quá trình cho e:
Al→ Al3++ 3e (1)
0,1 → 0, 3 mol
Zn→ Zn2++ 2e (1)
0,2 → 0, 4 mol
Tổng số mol e cho = 0,3+0,4= 0,7 mol
Quá trình nhận e: nkhí= 0,7mol
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí
N+5 + (5-a) e→ N+a
(5-a).0,7 0,7
Theo ĐL bảo toàn electron có: 0,7= 0,7. (5-a)→ a= 4 → NO2
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).1,4 0,7
Theo ĐL bảo toàn electron có: 0, 7= 1,4. (5-a) → a= 4,5→LOại
Vậy X là NO2
Đáp án A
Bài 47: Hòa tan hết 2,16 gam FeO trong 0,1 mol HNO3 vừa đủ thấy thoát ra khí X là sản phẩm khử duy nhất. Xác định khí X?
A. N2 B. N2O C. NO2 D. NO
Lời giải:
Hướng dẫn:
Ta có nFeO=0,03 mol= nFe(NO3)3
Bảo toàn nguyên tố N:
nN (HNO3)= nN (Fe(NO3)3)+ nN (khí X)→ 0,1=0,03.3+ nN(khí X)
→ nN(khí X)= 0,01 mol
QT cho e:
Fe+2→ Fe+3+ 1e
0,03 0,03 mol
Quá trình nhận e:
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí X
N+5 + (5-a) e→ N+a
(5-a).0,01 0,01
Theo ĐL bảo toàn electron có: 0,03= 0,01(5-a) → a= +2 → X là khí NO
-Nếu khí X có 2 nguyên tử N: → nKhí= nN(khí)/2= 0,005 mol
2N+5 + 2(5-a) e→ N2+a
(5-a).0,01 0,005
Theo ĐL bảo toàn electron có: 0, 03= 0,01.(5-a) → a= +2→LOại
Vậy X là NO
Đáp án D
Bài 48: Hòa tan hoàn toàn 7,29 gam Al bằng dung dịch HNO3 loãng, dư thu được dung dịch X và 1,792 lít khí (đltc) hỗn hợp Y gồm 2 khí là N2O và N2. Tỉ khối hơi của hỗn hợp khí Y so với H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là:
A. 51,12 B. 62,48 C. 76,68 D. 58,41
Lời giải:
Hướng dẫn:
Đặt nN2O= x mol; nN2= y mol
Ta có nhhY= x+y= 1,792/ 22,4= 0,08 mol
mhhY=44x + 28y= 0,08.18.2
Giải hệ trên được x= 0,04 và y= 0,04
nAl= 0,27 mol= nAl(NO3)3
Quá trình cho e:
Al→ Al3++ 3e (1)
0,27 → 0,81 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,4 ← 0,04 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,32 ← 0,04 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,4+ 0,32= 0,72 mol ⟨0,81 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,81- 0,72= 0,09 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,09 → 0, 01125 mol
Dung dịch X chứa 0,27 mol Al(NO3)3 và 0,01125 mol NH4NO3
→m=0,27.213+ 0,01125.80=58,41 gam
Đáp án D
Bài 49: Cho 2,7 gam Al tan hoàn toàn trong dung dịch HNO3 loãng, nóng thu được 0,448 lít khí X duy nhất (đktc). Cô cạn dung dịch thu được 22,7 gam chất rắn khan. Khí X là:
A. N2 B.NO2 C. NO D. N2O
Lời giải:
Hướng dẫn:
nAl= 0,1 mol=nAl(NO3)3 → mAl(NO3)3= 0,1. 213= 21,3 gam≠ 22,7 gam
→Muối khan phải chứa cả Al(NO3)3 và NH4NO3
mNH4NO3=22,7- 21,3= 1,4 gam →nNH4NO3= 0,0175 mol
Quá trình cho e:
Al → Al3++ 3e (1)
0,1 → 0,3mol
Quá trình nhận e: nkhí= 0,02mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (2)
0,14 ← 0,0175 mol
-Nếu khí X có 1 nguyên tử N: Gọi số oxi hóa của N trong X là a
N+5 + (5-a) e → N+a
(5-a).0,02 0,02
Theo ĐL bảo toàn electron có: 0,3= 0,02. (5-a)+0,14 → a= -3 → Loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e → N2+a
(5-a).0,04 0,02
Theo ĐL bảo toàn electron có: 0,3= 0,04. (5-a) + 0,14 → a= +1
→ Khí X là N2O
Đáp án D
Bài 50: Cho 5,04 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 3:2 tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí có tỉ khối hơi so với H2 bằng 18. Số mol HNO3 bị khử trong quá trình trên là:
A. 0,095 mol B. 0,11 mol C. 0,1 mol D. 0,08 mol
Lời giải:
Hướng dẫn:
Ta đặt nMg= 3x, nAl= 2x mol → mhh= 24.3x+ 27.2x=126x= 5,04 →x=0,04 mol→ nMg= 0,12 mol; nAl= 0,08 mol
Sản phẩm khử gồm 2 khí không màu, không hóa nâu ngoài không khí. Đó là N2 (a mol) và N2O (b mol)
Ta có a+b= 0,896/22,4= 0,04
Và mhh= 28a+ 44b= 18.2.0,04
Giải hệ trên có a= 0,02, b=0,02
QT cho e:
Mg→ Mg2++ 2e
0,12 0,24
Al→ Al3++ 3e
0,08 0,24
Tổng số mol e cho ne cho= 0,24+ 0,24= 0,48 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,2 ← 0,02 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,16 ← 0,02mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,2+ 0,16= 0,36mol ⟨0,48 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,48- 0,36= 0,12 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,12 → 0, 015 mol
Theo các bán phản ứng (2), (3), (4) thì
nNO3-bị khử= 2.nN2+ 2. nN2O+nNH4+= 2.0,02+2.0,02+0,015= 0,095 mol
=nHNO3 bị khử
Đáp án A
Bài 51: Hòa tan hoàn toàn 19,5 gam Zn bằng dung dịch HNO3 loãng dư thu được dung dịch X và 1,12 lít (ở đktc) hỗn hợp khí Y gồm hai khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là:
A. 56,7 B. 58,2 C. 47,4 D. 48,9
Lời giải:
Hướng dẫn:
Đặt nN2O= x mol; nN2= y mol
Ta có nhhY= x+y= 1,12/ 22,4= 0,05 mol
mhhY=44x + 28y= 0,05.18.2
Giải hệ trên được x= 0,025 và y= 0,025
nZn= 0,3 mol= nZn(NO3)2
Quá trình cho e:
Zn→ Zn2++ 2e (1)
0,3 → 0,6 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,25 ← 0,025 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,2 ← 0,025 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,25+ 0,2= 0,45 mol ⟨ 0,6 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,6- 0,45= 0,15mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,15 → 0, 01875 mol
Dung dịch X chứa 0,3 mol Zn(NO3)2 và 0,01875 mol NH4NO3
→m=0,3.189+ 0,01875.80=58,2 gam
Đáp án B
Bài 52: Cho m gam hỗn hợp Al và Mg hòa tan vừa hết với dung dịch có 0,275 mol HNO3 không có khí bay ra và thu được 18,25 gam muối khan. Giá trị của m là:
A. 2,41 B. 2,28 C. 1,97 D. 3,25
Lời giải:
Hướng dẫn:
Vì cho Al và Mg vào HNO3 không có khí bay ra nên sản phẩm khử là NH4NO3
Đặt nAl= xmol, nMg= y mol
8Al+ 30HNO3→8Al(NO3)3+3 NH4NO3+ 9H2O
x 30x/8 x 3x/8 mol
4Mg+ 10HNO3→ 4Mg(NO3)2+ NH4NO3+ 3H2O
y 10y/4 y y/4 mol
Khối lượng muối khan là
mmuối= mAl(NO3)3+ mMg(NO3)2+ mNH4NO3=213x+148y+ 80(3x/8+y/4)=18,25 gam
nHNO3= 30x/8+ 10y/4= 0,275 mol
Giải hệ trên ta có x= 23/900 mol và y= 43/600 mol
→m=27x+ 24y= 2,41 gam
Đáp án A
Bài 53: Hòa tan hoàn toàn 15,2 gam hỗn hợp X gồm Fe và Cu vào dung dịch HNO3 dư thu được 6,72 lít (đktc) khí Y gồm NO và NO2, có dY/H2= 19 và dung dịch Z (không chứa NH4+). Tính % khối lượng kim loại Fe trong X?
A. 40,24% B. 37,78% C. 36,84% D. 30,56%
Lời giải:
Hướng dẫn:
Ta đặt: nNO= x mol; nNO2= y mol
Ta có : nY= x+y= 6,72/22,4= 0,3 mol
mY= 30x+ 46y= nY.MY= 0,3.19.2
Giải hệ có x= 0,15 và y= 0,15
Đặt nFe= a mol ; nCu= b mol
QT cho e:
Fe → Fe3++ 3e
a 3a mol
Cu → Cu2++ 2e
b 2b mol
QT nhận e:
N+5+ 3e→ NO
0,45 0,15
N+5+ 1e→ NO2
0,15 0,15
Theo ĐL bảo toàn e có: ne cho= ne nhận nên 3a+2b= 0,45+ 0,15= 0,60
Mặt khác mkim loại= 56a+ 64b= 15,2
Giải hệ trên có a= 0,1, b= 0,15 →%mFe=36,84%
Đáp án C
Bài 54: Nung m gam bột sắt trong oxi, thu được 3 gam hỗn hợp rắn X. Hòa tan hết hỗn hợp X trong dung dịch HNO3 dư thoát ta 0,56 lít khí NO (đktc, là sản phẩm khử duy nhất). Giá trị của m là:
A. 2,52 B. 2,22 C. 2,32 D. 2,62
Lời giải:
Hướng dẫn:
Fe + O2 → hỗn hợp rắn X
Theo ĐL Bảo toàn khối lượng có mO2= 3-m (gam) → nO2= (3-m)/32 mol
Ta có nNO= 0,025 mol
QT cho e:
Fe→ Fe3++ 3e
m/56 3m/56 mol
QT nhận e :
O2+ 4e→ 2O-2
(3-m)/32 (3-m)/8
N+5+ 3e → NO
0,075 ← 0,025
Theo ĐL BT electron thì : ne cho= ne nhận
Nên 3m/56= (3-m)/8+ 0,075 Suy ra m= 2,52 gam
Đáp án A
Bài 55: Cho 11,36 gam hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư, thu được 1,344 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 35,50 B. 34,36 C. 49,09 D. 38,72
Lời giải:
Hướng dẫn:
Coi như hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 gồm có x mol Fe và y mol O
Ta có 56x+16y= 11,36 (1)
Ta có nNO= 0,06 mol
QT cho e :
Fe → Fe3++ 3e
x 3x mol
QT nhận e :
O+ 2e → O-2
y 2y mol
N+5+ 3e → NO
0,18 ← 0,06
Theo ĐL BT electron thì : ne cho= ne nhận nên 3x= 2y+ 0,18 (2)
Từ (1) và (2) ta có x= 0,16 và y= 0,15
Bảo toàn nguyên tố Fe có nFe(NO3)3= nFe= x= 0,16 mol→ mFe(NO3)3=38,72 gam
Đáp án D
Bài 56: Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch HNO3 đặc nóng thu được dung dịch X và 6,496 lít khí NO2 (sản phẩm khử duy nhất, ở đktc). Cô cạn dung dịch X, thu được m gam muối nitrat khan. Giá trị của m là:
A. 35,09 B. 105,27 C. 70,18 D. 210,54
Lời giải:
Hướng dẫn:
Quy đổi oxit sắt gồm có x mol Fe và y mol O
Ta có 56x+16y= 20,88 (1)
Ta có nNO2= 0,29 mol
QT cho e :
Fe → Fe3++ 3e
x 3x mol
QT nhận e :
O+ 2e→ O-2
y 2y mol
N+5+ 1e → NO2
0,29 ← 0,29
Theo ĐL BT electron thì : ne cho= ne nhận nên 3x= 2y+ 0,29 (2)
Từ (1) và (2) ta có x= 0,29 và y= 0,29
Bảo toàn nguyên tố Fe có nFe(NO3)3= nFe= x= 0,29 mol→ mFe(NO3)3=70,18 gam
Đáp án C
Bài 57: Nung m gam bột Cu trong oxi thu được 24,8 gam hỗn hợp chất rắn X gồm Cu, CuO, Cu2O. Hòa tan hoàn toàn X trong dung dịch HNO3 đặc nóng thoát ra 8,96 lít khí NO2 duy nhất (đktc). Giá trị của m là:
A. 9,6 B. 14,72 C. 21,12 D. 22,4
Lời giải:
Hướng dẫn:
Cu + O2 → hỗn hợp rắn X
Theo ĐL Bảo toàn khối lượng có mO2= 24,8-m (gam)
→ nO2= (24,8-m)/32 mol
Ta có nNO2= 0,4 mol
QT cho e:
Cu→ Cu2++ 2e
m/64 2m/64 mol
QT nhận e :
O2+ 4e→ 2O-2
(24,8-m)/32 (24,8-m)/8
N+5+ 1e → NO2
0,4 ← 0,4
Theo ĐL BT electron thì : ne cho= ne nhận
Nên 2m/64= (24,8-m)/8+ 0,4 Suy ra m= 22,4 gam
Đáp án D
Bài 58: Hòa tan hoàn toàn 25,6 gam chất rắn X gồm Fe, FeS, FeS2 và S bằng dung dịch HNO3 dư, thoát ra V lít khí NO duy nhất (đktc) và dung dịch Y. Thêm Ba(OH)2 dư vào Y thu được 126,25 gam kết tủa. Giá trị của V là:
A. 17,92 B. 19,04 C. 24,64 D. 27,58
Lời giải:
Hướng dẫn:
Quy đổi hỗn hợp X thành Fe: x mol và S: y mol
Ta có: m2X= 56x+ 32y= 25,6 gam (1)
QT cho e :
Fe → Fe3++ 3e
x 3x mol
S0 → SO42-+ 6e
y y 6y
Dung dịch Y có Fe3+, SO42-, H+, NO-3
Khi cho Ba(OH)2 dư vào dung dịch Y thì:
Ba2++ SO42- → BaSO4
y y mol
Fe3++ 3OH- → Fe(OH)3
x x mol
mkết tủa= mFe(OH)3+ mBaSO4= 107x+ 233y=126,25 (2)
Từ (1) và (2) có x= 0,2 và y= 0,45
Tổng số mol e cho 3x+6y= 3,3 mol
Theo ĐL BT e : ne cho= ne nhận= 3,3 mol
QT nhận e :
N+5+ 3e → NO
3,3 → 1,1 mol
VNO=24,64 lít
Đáp án C
Bài 59: Hòa tan hoàn toàn 30,4 gam chất rắn X gồm Cu, CuS, Cu2S và S bằng HNO3 dư thoát ra 20,16 lít khí NO duy nhất (đktc) và dung dịch Y. Thêm Ba(OH)2 dư vào Y thu được m gam kết tủa. Giá trị của m là:
A. 81,55 B. 104,20 C. 110,95 D. 115,85
Lời giải:
Hướng dẫn:
Quy đổi hỗn hợp X thành Cu: x mol và S: y mol
Ta có: mX= 64x+ 32y= 30,4 gam (1)
QT cho e :
Cu → Cu2++ 2e
x 2x mol
S0 → SO42-+ 6e
y y 6y
QT nhận e : nNO= 0,9 mol
N+5+ 3e → NO
2,7 ← 0,9 mol
Theo ĐL BT e : ne cho= ne nhận nên 2x+6y= 2,7 (2)
Từ (1) và (2) suy ra x= 0,3 và y= 0,35
Dung dịch Y có Cu2+, SO42-, H+, NO-3
Khi cho Ba(OH)2 dư vào dung dịch Y thì:
Ba2++ SO42- → BaSO4
y y mol
Cu2++ 2OH- → Cu(OH)2
x x mol
mkết tủa= mCu(OH)2+ mBaSO4= 98x+ 233y=98.0,3+ 233.0,35=110,95 gam
Đáp án C
Bài 60: Đem nung hỗn hợp X gồm hai kim loại: a mol Fe và 0,15 mol Cu trong không khí một thời gian thu được 63,2 gam hỗn hợp Y gồm 2 kim loại trên và hỗn hợp các oxit của chúng. Đem hòa tan hết lượng hỗn hợp Y trên bằng dung dịch HNO3 đậm đặc thì thu được 0,2 mol NO. Trị số của a là:
A. 0,64 mol B. 0,60 mol C. 0,70 mol D. 0,67 mol
Lời giải:
Hướng dẫn:
Fe, Cu + O2 → hỗn hợp rắn X
Theo ĐL Bảo toàn khối lượng có mO2= 63,2-56a-0,15.64= 53,6-56a (gam) → nO2= (53,6-56a)/32 mol
Ta có nNO= 0,2 mol
QT cho e:
Fe→ Fe3++ 3e
a 3a mol
Cu → Cu2++ 2e
0,15 0,3
QT nhận e :
O2+ 4e→ 2O-2
(53,6-56a)/32 (53,6-56a)/8
N+5+ 3e → NO
0,6 ← 0,2
Theo ĐL BT electron thì : ne cho= ne nhận
Nên 3a+ 0,3= (53,6-56a)/8+ 0,6 Suy ra a= 0,7
Đáp án C
Bài 61: Hòa tan hoàn toàn 2,44 gam hỗn hợp bột X gồm FexOy và Cu bằng dung dịch HNO3 đặc nóng (dư). Sau phản ứng thu được 0,336 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch chứa 7,93 gam hỗn hợp muối nitrat. Phần trăm khối lượng của Cu trong X là:
A. 39,34% B. 65,57% C. 26,23% D. 13,11%
Lời giải:
Hướng dẫn:
Quy hỗn hợp X gồm có a mol Fe, b mol Cu và c mol O
Ta có 56a + 64b + 16c= 2,44
Bảo toàn nguyên tố Fe và Cu có nFe(NO3)3= nFe= a mol;nCu(NO3)2= nCu= b mol
Khối lượng muối nitrat là
mmuối= mFe(NO3)3+ mCu(NO3)2=242a + 188b= 7,93 gam
QT cho e:
Fe→ Fe3++ 3e
a 3a mol
Cu → Cu2++ 2e
b 2b
QT nhận e :
O+ 2e→ O-2
c 2c
N+5+ 3e → NO
0,045 ← 0,015
Theo ĐL BT electron thì : ne cho= ne nhận nên 3a+ 2b= 2c+ 0,045 (3)
Giải hệ gồm (1), (2) và (3) có a= 0,025; b= 0,01 và c= 0,025
→%mCu= 0,01.64.100%/2,44=26,23%
Đáp án C
Bài 62: Khi cho m gam hỗn hợp gồm 3 kim loại Al, Mg, Cu tan vừa hết trong dung dịch HNO3 loãng, thu được 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc) và dung dịch X. Cô cạn cẩn thận dung dịch X thu được khối lượng muối nitrat là:
A. (m+ 62) gam B. (m+9,3 ) gam
C. (m+13,95) gam D. (m+ 27,9) gam
Lời giải:
Hướng dẫn:
Ta có nNO= 0,15 mol
QT nhận e:
NO3-+ 3e+ 4H+ → NO+ 2H2O
Ta có nNO3- trong muối= ne= 3.nNO= 3.0,15= 0,45 mol
→mmuối nitrat= mkim loại+ mNO3-trong muối= m+ 0,45.62= m+27,9 (gam)
Đáp án D
Bài 63: 4,86 gam Al phản ứng vừa đủ với dung dịch HNO3 thu được V lít khí NO duy nhất (đktc) và dung dịch X. Để phản ứng với dung dịch X đến khi kết tủa tan vừa hết tạo dung dịch muối trong suốt cần dùng 750 ml dung dịch NaOH 1M. Giá trị của V là:
A. 3,36 B. 4,48 C. 4,032 D. 2,24
Lời giải:
Hướng dẫn:
Ta có nAl= 0,18 mol= nAl(NO3)3, nNaOH= 0,75 mol
Dung dịch X chứa Al(NO3)3, có thể có NH4NO3
Al3++ 3OH-→ Al(OH)3↓ (1)
0,18 0,54 0,18
Al(OH)3+ OH- → AlO2-+ 2H2O (2)
0,18 0,18
Tổng mol OH- ở (1) và (2) là nOH-= 0,54+ 0,18= 0,72 mol ⟨ 0,75 mol
Nên có PT (3) với nOH- PT3= 0,75- 0,72= 0,03 mol
NH4++ OH- → NH3+ H2O (3)
0,03 0,03 mol
QT cho e:
Al → Al3++ 3e (1)
0,18 0,54
QT nhận e:
NO3-+ 8e+ 10H+ → NH4++ 3H2O (2)
0,24 ← 0, 03 mol
NO3-+ 3e+ 4H+ → NO+ 2H2O (3)
Theo ĐL bảo toàn e: ne cho= ne nhận nên 0,54=8.nNH4++ 3.nNO
Hay 0,54=8. 0,03+ 3.nNO suy ra nNO= 0,1 mol → V= 2,24 lít
Đáp án D
Bài 64: Hòa tan hoàn toàn 3,76 gam hỗn hợp H gồm: S, FeS, FeS2 trong HNO3 dư được 0,48 mol NO2 và dung dịch X. Cho dung dịch Ba(OH)2 dư vào X, lọc kết tủa nung đến khối lượng không đổi thì khối lượng chất rắn thu được là:
A. 17,545 gam B. 18,355 gam
C. 15,145 gam D. 2,4 gam
Lời giải:
Hướng dẫn:
Gọi x, y lần lượt là tổng số mol Fe và S trong hỗn hợp (cũng có thể coi x, y là số mol Fe và S đã tham gia phản ứng với nhau tạo ra hỗn hợp trên)
Ta có: 56x + 32y = 3,76
Mặt khác: ne (cho) = 3x + 6y = 0,48 = ne (nhận) (vì hỗn hợp H bị oxi hóa tạo muối Fe3+ và H2SO4)
Từ đó có: x = 0,03; y = 0,065
Khi thêm Ba(OH)2 dư kết tủa thu được có: Fe(OH)3 (0,03 mol) và BaSO4 (0,065 mol).
Sau khi nung chất rắn có: Fe2O3 (0,015 mol) và BaSO4 (0,065 mol).
mchất rắn = 160.0,015 + 233.0,065 = 17,545 (gam)
Đáp án A
Bài 65: Hòa tan hoàn toàn hỗn hợp gồm 0,01 mol FeS2 và y mol Cu2S vào axit HNO3 (vừa đủ) thu được dung dịch X (chỉ chứa hai muối sunfat) và V lít khí NO2 (đktc, sản phẩm khử duy nhất). Giá trị của V là:
A. 2,912 B. 2,24 C. 4,48 D. 3,136
Lời giải:
Hướng dẫn:
Ta có sơ đồ phản ứng :
FeS2, Cu2S+ HNO3 →Fe2(SO4)3+ CuSO4+ NO2+ H2O
Bảo toàn nguyên tố Fe ta có: nFe2(SO4)3= 1/2. nFeS2= 0,01/2= 0,005 mol
Bảo toàn nguyên tố Cu ta có: nCuSO4= 2.nCu2S= 2 y mol
Bảo toàn nguyên tố S có nS( FeS2, Cu2S)= nS (trong 2 muối sunfat)
Nên 2.0,01+ y= 3.0,005+ 2y → y=0,005 mol
QT cho e :
FeS2 → Fe3++ 2S+6+15 e
Cu2S → 2Cu2++ S+6+ 10e
Tổng số mol e cho là
ne cho= 15.nFeS2+ 10. nCu2S = 15.0,01+10.0,005=0,2 mol
QT nhận e :
N+5+ 1e → NO2
0,2 → 0,2 mol
Theo ĐL BT e : ne cho= ne nhận= 0,2 mol →V= 4,48 lít
Đáp án C
Bài 66: Cho 61,2 gam hỗn hợp X gồm Cu và Fe3O4 tác dụng với dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc), dung dịch Y và còn lại 2,4 gam kim loại. Cô cạn dung dịch Y, thu được m gam muối khan. Xác định giá trị của m?
A. 145,5 gam B. 151,5 gam C. 159,5 gam D. 147,5 gam
Lời giải:
Hướng dẫn:
n3NO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B
Bài 67: Hòa tan hoàn toàn hỗn hợp gồm 1,44 gam Mg và 1,8 gam Al bằng dung dịch HNO3 vừa đủ, thu được 0,04 mol khí X (sản phẩm khử duy nhất). X là chất nào sau đây?
A. NO2 B. NO C. N2O D. N2
Lời giải:
Hướng dẫn:
Ta có nMg= 0,06 mol; nAl= 1/15 mol
QT cho e :
Mg → Mg2++ 2e
Al→ Al3++ 3e
Có ne cho=2.nMg+ 3.nAl= 0,32 mol
QT nhận e
-Nếu khí X có 1 nguyên tử N: Gọi số oxi hóa của N trong X là a
N+5 + (5-a) e→ N+a
(5-a).0,04 0,04
Theo ĐL bảo toàn electron có: 0,32= 0,04. (5-a)→ a= -3→ Loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,08 0,04
Theo ĐL bảo toàn electron có: 0,32= 0,08. (5-a) → a= +1
→ Khí X là N2O
Đáp án C
Bài 68: Cho 18,5 gam hỗn hợp gồm Fe và Fe3O4 tác dụng với 200 ml dung dịch HNO3 loãng , đun nóng. Sau phản ứng thu được 2,24 lít khí NO duy nhất (đktc), dung dịch D và còn lại 1,46 gam kim loại. Nồng độ mol của dung dịch HNO3 là
A. 3,2M B. 3,5M C. 2,6M D. 5,1M
Lời giải:
Hướng dẫn:
Khối lượng Fe dư là 1,46g, do đó khối lượng Fe và Fe3O4 đã phản ứng là 17,04g. Vì sau phản ứng sắt còn dư nên trong dung dịch D chỉ chứa muối sắt (II).
Sơ đồ phản ứng:
Fe, Fe3O4 + HNO3 → Fe(NO3)2 + NO + H2O
Mol: 2n+0,1 n 0,1 0,5( 2n+0,1)
Đặt số mol của Fe(NO3)2 là n, áp dụng định luật bảo toàn nguyên tố đối với nitơ ta có số mol của axit HNO3 là 2n+ 0,1. Số mol H2O bằng một nửa số mol của HNO3.
Áp dụng định luật bảo toàn khối lượng ta có:
17,04 + 63(2n + 0,1) = 242n + 0,1.30 + 18.0,5(2n + 0,1)
giải ra ta có n = 2,7, suy ra [ HNO3 ] = (2.2,7 + 0,1): 0,2 = 3,2M
Đáp án A
Bài 69: Lấy m gam P2O5 cho tác dụng với 338 ml dung dịch NaOH 2M. Sau phản ứng cô cạn dung dịch thu được 3m gam chất rắn. Giá trị của m gần nhất với:
A. 11,5 B. 17,5 C. 12,5 D.14,5
Lời giải:
Hướng dẫn:
TH 1: P2O5 và NaOH pứ vừa đủ tạo muối: nH2O = nNaOH = 0,676mol.
P2O5 + H2O → 2H3PO4
m/142 → 2m/142 mol
Có thể xảy ra các PT:
H3PO4+ NaOH →NaH2PO4+ H2O (3)
H3PO4+ 2NaOH →Na2HPO4+ 2H2O (4)
H3PO4+ 3NaOH →Na3PO4+ 3H2O (5)
BKTL: mH3PO4 + mNaOH = mrắn + mH2O
(2m/142).98 + 0,676x40 = 3m + 0,676x18 → m = 9,182gam (loại).
TH2:Chất rắn gồm: NaOHdư; Na3PO4
P2O5 + 6NaOH → 2Na3PO4 + 3H2O
m/142 0,676 2m/142 3m/142
BTKL: mP2O5+ mNaOHbđ = m rắn + mH2O
m + 0,676x40 = 3m + 18x3m/142→ m = 11,36 gam gần nhất với 11,5.
Đáp án A
Bài 70: Oxi hóa hoàn toàn 3,1 gam photpho trong khí oxi dư. Cho toàn bộ sản phẩm vào 200 ml dung dịch NaOH 1M đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch X. Khối lượng muối trong X là:
A. 12 gam B. 14,2 gam C. 11, 1 gam D. 16,4 gam
Lời giải:
Hướng dẫn:
Ta có nP =0,1 mol, nNaOH= 0,2 mol
4P + 5O2→ 2P2O5 (1)
0,1 0,05 mol
Cho P2O5 vào dung dịch NaOH thì:
P2O5+ 3H2O→ 2H3PO4 (2)
0,05 0,1 mol
Có thể xảy ra các PT:
H3PO4+ NaOH →NaH2PO4+ H2O (3)
H3PO4+ 2NaOH →Na2HPO4+ 2H2O (4)
H3PO4+ 3NaOH →Na3PO4+ 3H2O (5)
Ta có T= nNaOH/ nH3PO4= 0,2/0,1=2→ Phản ứng theo PT (2)
nNa2HPO4= nH3PO4= 0,1 mol → mNa2HPO4=0,1.142=14,2 gam
Đáp án B
Bài 71: Cho m gam P2O5 tác dụng với 253,5 ml dung dịch NaOH 2M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X.. Cô cạn dung dịch X thu được 3m gam chất rắn. Giá trị của m là:
A. 21,3 B. 8,52 C. 12,78 D. 7,81
Lời giải:
Hướng dẫn:
TH 1: P2O5 và NaOH pứ vừa đủ tạo muối: nH2O = nNaOH = 0,507mol.
P2O5 + H2O → 2H3PO4
m/142 → 2m/142 mol
Có thể xảy ra các PT:
H3PO4+ NaOH →NaH2PO4+ H2O (3)
H3PO4+ 2NaOH →Na2HPO4+ 2H2O (4)
H3PO4+ 3NaOH →Na3PO4+ 3H2O (5)
BKTL: mH3PO4 + mNaOH = mrắn + mH2O
(2m/142).98 + 0,507x40 = 3m + 0,507x18 →m = 6,886gam (loại).
TH2:Chất rắn gồm: NaOHdư; Na3PO4
P2O5 + 6NaOH → 2Na3PO4 + 3H2O
m/142 0,507 2m/142 3m/142
BTKL: mP2O5+ mNaOHbđ = m rắn + mH2O
m + 0,2535x2x40 = 3m + 18x3m/142 → m = 8,52g.
Đáp án B

Bài 72: Cho m gam P2O5 tác dụng với 400 ml dung dịch NaOH 0,3M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X. Cô cạn dung dịch X thu được 1,55m gam chất rắn. Giá trị của m gần nhất với:
A. 15,6 B. 15,5 C. 15,8 D. 15,7
Lời giải:
Hướng dẫn:
TH 1: P2O5 và NaOH pứ vừa đủ tạo muối: nH2O = nNaOH = 0,12mol.
P2O5 + H2O → 2H3PO4
m/142 → 2m/142 mol
Có thể xảy ra các PT:
H3PO4+ NaOH →NaH2PO4+ H2O (3)
H3PO4+ 2NaOH →Na2HPO4+ 2H2O (4)
H3PO4+ 3NaOH →Na3PO4+ 3H2O (5)
BKTL: mH3PO4 + mNaOH = mrắn + mH2O
(2m/142).98 + 0,12x40 = 1,55m + 0,12x18 →m = 15,555gam gần nhất với 15,6 gam
TH2:Chất rắn gồm: NaOHdư; Na3PO4
P2O5 + 6NaOH → 2Na3PO4 + 3H2O
m/142 0,12 2m/142 3m/142
BTKL: mP2O5+ mNaOHbđ = m rắn + mH2O
m + 0,12x40 = 1,55m + 18x3m/142 m = 5,16g. Loại
Đáp án A
Bài 73: Có ba dung dịch riêng biệt: H2SO4 1M; KNO3 1M; HNO3 1M được đánh số ngẫu nhiên là (1), (2), (3).
-Trộn 5 ml dung dịch (1) với 5 ml dung dịch (2), thêm bột Cu dư thu được V1 lít khí NO
-Trộn 5 ml dung dịch (1) với 5 ml dung dịch (3), thêm bột Cu dư thu được 2V1 lít khí NO
-Trộn 5 ml dung dịch (2) với 5 ml dung dịch (3), thêm bột Cu dư thu được V2 lít khí NO
Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất, các thể tích khí đo ở cùng điều kiện. So sánh nào sau đây đúng?
A. V2 = V1 B. V2 = 3V1
C. V2 = 2V1 D. 2V2 = V1
Lời giải:
Hướng dẫn:
Suy luận:
3Cu+ 8H++ 2NO3- → 3Cu2++ 2NO + 4 H2O
TN1: 4V1 ← V1 lít
TN2: 8V1 ← 2V1 lít
Nhận thấy: nH+ (TN2)= 2nH+ (TN1) → (1) là KNO3; (2) là HNO3; (3) là H2SO4
3Cu+ 8H++ 2NO3- → 3Cu2++ 2NO + 4 H2O
TN1: ban đầu 5.10-3 10.10-3
Phản ứng 5.10-3 1,25.10-3
TN3: ban đầu 15.10-3 5.10-3
Phản ứng 15.10-3 3,75.10-3
Các thể tích khí đo ở cùng điều kiện nên nNO(TN3)= 3nNO (TN1) → VNO(TN3)= 3VNO (TN1) hay V2= 3 V1
Đáp án B
Bài 74: Đun nóng m gam Cu(NO3)2 một thời gian rồi dừng lại, làm nguội và đem cân thấy khối lượng chất rắn giảm 0,54 gam so với ban đầu. Khối lượng Cu(NO3)2 đã bị nhiệt phân là:
A. 1,88 gam B. 0,47 gam C. 9,40 gam D. 0,94 gam
Lời giải:
Hướng dẫn:
Đặt số mol Cu(NO3)2 đã phản ứng là x mol
Cu(NO3)2 → CuO + 2NO2+ ½ O2
X 2x x/2 mol
Khối lượng chất rắn giảm chính là khối lượng NO2 và O2 thoát ra
Ta có: mrắn giảm= mNO2+ mO2= 46.2x+ 32.x/2=108x= 0,54
suy ra x=0,005 mol→ mCu(NO3)2 pứ= 188x=0,94 gam
Đáp án D
Bài 75: Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2thu được hỗn hợp khí X (tỉ khối hơi của X so với khí H2 bằng 18,8). Tính khối lượng Cu(NO3)2 trong hỗn hợp ban đầu?
A. 8,60 gam B. 20,50 gam C. 11,28 gam D. 9,4 gam
Lời giải:
Hướng dẫn:
Đặt số mol Cu(NO3)2 và KNO3 lần lượt là x, y mol
→188 x+101y= 34,65 (1)
Cu(NO3)2 → CuO + 2NO2+ ½ O2
x 2x x/2 mol
KNO3 → KNO2 + ½ O3
y y/2 mol
Hỗn hợp khí X thu được gồm 2x mol NO2 và x/2+ y/2 mol O2
Ta có: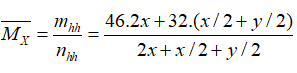
Từ (1) và (2) ta có x= 0,05, y=0,25 → mCu(NO3)2=9,4 gam
Đáp án D
Bài 76:Cho 3,2 gam bột Cu tác dụng với 100 ml dung dịch hỗn hợp gồm HNO3 0,8M và H2SO4 0,2M. Sau khi các phản ứng hoàn toàn sinh ra V lít khí NO (sản phẩm khử duy nhất ở đktc). Giá trị của V là:
A. 0,764 B. 0,448 C. 1,792 D. 0,672
Lời giải:
Hướng dẫn:
Ta có nCu=0,05 mol, nHNO3=0,08 mol; nH2SO4=0,02 mol, nH+= 0,12 mol, nNO3-= 0,08 mol
3Cu + 8H+ + 2NO3-→ 3Cu2+ + 2NO + 4H2O
0,05 0,12 0,08 0,03 mol
Ta có 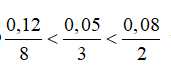
→V= 0,672 lít
Đáp án D
Bài 77: Cho m gam bột Fe vào 800 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và H2SO4 0,25M. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,6m gam hỗn hợp bột kim loại và V lít khí NO (sản phẩm khử duy nhất ở đktc). Giá trị của m và V là:
A. 10,8 và 4,48 B. 10,8 và 2,24
C. 17,8 và 2,24 D. 17,8 và 4,48
Lời giải:
Hướng dẫn:
nCu2+ = 0,16; nNO3- = 0,32 ; nH+ = 0,4. Kim loại dư muối Fe2+
3Fe + 2NO3- + 8H+ → 3Fe2+ + 2NO + 4H2O (1)
0,15← ----- 0,4 ------------→ 0,1
Fe + Cu2+ → Fe2+ + Cu (2)
0,16← 0,16 -------→ 0,16
m – 0,15.56 (1) + mtăng(2) = 0,6m → m = 17,8 g và V = 0,1.22,4 = 2,24 lít
Đáp án C
Bài 78: Cho hỗn hợp gồm 1,12 gam Fe và 1,92 gam Cu vào 400 ml dung dịch chứa hỗn hợp gồm H2SO4 0,5M và NaNO3 0,2M. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho V ml dung dịch NaOH 1M vào dung dịch X thì lượng kết tủa thu được là lớn nhất. Giá trị tối thiểu của V là:
A. 360 B. 240 C. 400 D. 120
Lời giải:
Hướng dẫn:
Ta có: nFe=0,02 mol; nCu= 0,03 mol, nH2SO4= 0,2 mol, nNaNO3= 0,08 mol
nH+= 2nH2SO4= 0,4 mol, nNO3-= 0,08 mol
3Cu + 8H+ + 2NO3-→ 3Cu2+ + 2NO + 4H2O (1)
0,03 0,08 0,02 0,03 mol
Fe + 4H+ + NO3- → Fe3+ + NO + 2H2O (2)
0,02 0,08 0,02 0,02 mol
Tổng số mol H+ tham gia phản ứng (1) và (2) là 0,08+ 0,08= 0,16 mol
→nH+ dư= 0,4-0,16= 0,24 mol
Dung dịch X có chứa Cu2+, Fe3+ và H+
H++ OH-→H2O (3)
Cu2++ 2OH- → Cu(OH)2 (4)
Fe3++ 3OH- → Fe(OH)3 (5)
Theo PT (3), (4), (5) ta có
nOH-= nH++ 2nCu2++ 3nFe3+= 0,24+ 2.0,03+ 3.0,02= 0,36 mol= nNaOH
→V= 0,36 lít= 360 ml
Đáp án A
Bài 79: Cho 3,48 gam bột Mg tan hết trong dung dịch hỗn hợp gồm HCl dư và KNO3, thu được dung dịch X chứa m gam muối và 0,56 lít hỗn hợp khí Y gồm N2 và H2 ở đktc. Khí Y có tỉ khối so với H2 bằng 11,4. Giá trị của m là:
A. 16,085 B. 18,300 C. 14,485 D. 18,035
Lời giải:
Hướng dẫn:
Ta có nMg=0,145 mol
Gọi x và y lần lượt là số mol của H2 và N2
Ta có: x+ y= 0,025; 2x+ 28y= 0,025.(11,4.2) → x= 0,005; y= 0,02
Vì có khí H2 thoát ra → NO3- hết → Muối thu được là muối clorua
QT cho e:
Mg → Mg2++ 2e (1)
0,145 → 0,29 mol
QT nhận e:
2N+5+ 10e →N2 (2)
0,2 ← 0,02 mol
2H+1+2e→ H2 (3)
0,01 ← 0,005 mol
Nếu chỉ có quá trình nhận (2) và (3) thì
ne nhận= 0,2+ 0,01= 0,21 mol≠ 0,29 mol
→ Còn có quá trình nhận e tạo muối NH4+
Theo ĐL bảo toàn e: ne cho=ne nhận = 0,29 mol → e nhận ở (4)= 0,29-0,21=0,08 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,08 → 0, 01 mol
Bảo toàn nguyên tố N ta có
nN(KNO3)= nN(N2)+ nN (NH4+)=2.0,02+ 0,01= 0,05 mol= nKNO3= nK+
Muối chứa Mg2+: 0,145 mol, NH4+: 0,01 mol, K+: 0,05 mol, Cl-
Dùng bảo toàn điện tích: 0,145.2+ 0,01.1+ 0,05= nCl-= 0,35 mol
→mmuốimuối=m= 0,145.24+ 0,01.18+ 0,05.39+ 0,35.35,5= 18,035 gam
Đáp án D
Bài 80: Cho m gam P2O5 vào dung dịch chứa 0,1 mol NaOH và 0,05 mol KOH thu được dung dịch X. Cô cạn X, thu được 8,56 gam hỗn hợp chất rắn khan. Giá trị của m là:
A. 1,76 B. 2,13 C. 4,46 D. 2,84
Lời giải:
Hướng dẫn:
Đặt nP= x mol, nOH- =0,15 mol
TH1: Axit dư, x > 0,15
Dễ thấy chất rắn gồm
(x-0,15)/2 mol P2O5, 0,1 mol NaH2PO4, 0,05 mol KH2PO4
→mrắn= 142. (x-0,15)/2+ 99.0,1+ 136.0,05 > 8,56 gam (Vô lí)
TH2: Kiềm dư, x ⟨ 0,15/3= 0,05
Chất rắn gồm: x mol PO43-, 0,15-3x mol OH-, 0,1 mol Na+, 0,05 mol K+
→ mrắn= 95x+ 17. (0,15-3x)+ 23.0,1+ 39.0,05= 8,56 gam
→ x= 0,04
Vậy nP2O5= 0,02 mol→m= 2,84 gam
TH3: Tạo hỗn hợp muối, 0,05 ⟨ x⟨ 0,15
Chất rắn gồm:
H2PO4 -, HPO42-, PO43- (hai trong 3 gốc này): x mol; K+: 0,05 mol, Na+: 0,1 mol
→mrắn= M.x+ 23.0,1+ 39.0,05
Vì x> 0,05 và M> 95 nên mrắn > 95.0,05+ 2,3+1,95=9 >8,56
→Không thỏa mãn
Đáp án D
Bài 81: Cho 0,87 gam hỗn hợp gồm Fe, Cu và Al vào bình đựng 300 ml dung dịch H2SO4 0,1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,32 gam chất rắn và có 448 ml khí (đktc) thoát ra. Thêm tiếp vào bình 0,425 gam NaNO3, khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là:
A.0,224 lít và 3,750 gam B. 0,112 lít và 3,750 gam
C. 0,224 lít và 3,865 gam D. 0,112 lít và 3,865 gam
Lời giải:
Hướng dẫn:
Cho 0,87 gam hỗn hợp gồm Fe, Cu và Al vào dung dịch H2SO4
→ Chất rắn không tan là Cu, mCu= 0,32 gam, nCu=0,005 mol
2Al+ 3H2SO4 → Al2(SO4)3+ 3H2
Fe+ H2SO4 → FeSO4+ H2
Ta có mFe + mAl = 0,87 - 0,32 = 0,55 gam
Đặt nFe= x mol, nAl= y mol → 56x + 27y= 0,55
nH2= 1,5.x+ y= 0,448/22,4= 0,02 mol
→ x = 0,005; y= 0,01
ta có nH2SO4 ban đầu= 0,3.0,1=0,03 mol, nH2= 0,448/22,4=0,02 mol
nH+ còn lại = nH+ ban đầu- nH+ pứ= 2.nH2SO4- 2.nH2= 2. 0,03- 2.0,02= 0,02 mol
nNO3- =nNaNO3= 0,005 mol
Ta có các bán phản ứng sau
Fe2+ → Fe3+ + 1e
0,005 0,005
Cu -→ Cu2+ + 2e
0,005 0,01
=> ne cho = 0,015 mol= ne nhận
4H+ + NO3- + 3e → NO + 2H2O (3)
0,02 0,005 0,015 0,005
V = 0,005.22,4 = 0,112 lít
Theo bán phản ứng (3) thì cả H+ và NO3- đều hết
Khối lượng muối=Khối lượng kim loại + mNa+ + mSO4
= 0,87 + 0,005.23 + 0,03.96 = 3,865 gam
Đáp án D
Bài 82: Hòa tan hết một lượng S và 0,01 mol Cu2S trong dung dịch HNO3 đặc, nóng, sau phản ứng hoàn toàn dung dịch thu được chỉ có 1 chất tan và sản phẩm khử là khí NO2 duy nhất. Hấp thụ hết lượng NO2 này vào 200 ml dung dịch NaOH 1M, rồi cô cạn dung dịch sau phản ứng thì được m gam chất rắn khan. Giá trị của m là
A. 18,4. B. 12,64.
C. 13,92. D. 15,2.
Lời giải:
Hướng dẫn:
Dễ dàng thấy chất tan là CuSO4 = 0,02 mol (bảo toàn nguyên tố Cu)
=> Quy đổi ban đầu có 0,02 mol S (bảo toàn nguyên tố S) và 0,02 mol Cu
Bảo toàn e => n NO2 = 0,02.6 + 0,02.2 = 0,16 mol
QT cho e :
Cu → Cu2++ 2e
0,02 0,04 mol
S0 → SO42-+ 6e
0,02 0,12 mol
Số mol e cho là ne cho= 0,16 mol
Theo bảo toàn e : ne cho= ne nhận= 0,16 mol
QT nhận e :
N+5+ 1e → NO2
0,16 → 0,16 mol
2NaOH + 2NO2 => NaNO2 + NaNO3 + H2O
Do 0,2> 0,16 nên NO2 hết và NaOH dư
Vì NO2 hết nên n H2O = 0,08 mol (= ½ n NO2)
→ m chất rắn = mNO2+ mNaOH- mH2O= 40.0,2 + 0,16.46 – 0,08.18 = 13,92 gam
Đáp án C
Bài 83: Thực hiện 2 thí nghiệm:
TN 1: Cho 3,84 gam Cu phản ứng với 80 ml dung dịch HNO3 1,0M thoát ra a lít NO.
TN2: Cho 3,84 gam Cu phản ứng với 80 ml dung dịch chứa HNO3 1,0M và H2SO4 0,5 M thoát b lít NO.
Biết NO là sản phẩm khử duy nhất, các thể tích khí đo ở cùng điều kiện. Quan hệ giữa a và b là
A. b = a. B. b = 2a. C. 2b = 5a. D. 2b = 3a.
Lời giải:
Hướngdẫn:
(*) TN1 :
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + H2O
0,06 0,08 → 0,02 mol
(*) TN2 :
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
0,06 0,16 0,08 → 0,04 mol
→ b= 2a
Đáp án B
Bài 84: Cho m gam hỗn hợp Cu, Fe, Al tác dụng hoàn toàn với dung dịch HNO3 loãng dư thu được (m+31) gam muối nitrat. Nếu cũng cho m gam hỗn hợp trên tác dụng với oxi thu được các oxit CuO, Fe2O3, Al2O3 thì khối lượng oxit là:
A.m + 32 B. m+16 C. m+4 D. m+48
Lời giải:
Hướng dẫn:
Ta có: mNO3-= mmuối nitrat- mkim loại= (m+31)-m= 31 gam → nNO3-= 0,5 mol
Ta thấy số oxi hóa của Cu, Fe, Al trong muối nitrat và trong các oxit tương ứng là bằng nhau
→nNO3-= nđiện tích dương của cation= 2.nO2- → nO2-= 0,25 mol
→ moxit= mkim loại+ mO2-= m+ 0,25.16= m+ 4 (gam)
Đáp án C
Bài 85: X là hỗn hợp các muối Cu(NO3)2, Fe(NO3)2, Fe(NO3)3, Mg(NO3)2 trong đó O chiếm 55,68% về khối lượng. Cho dung dịch KOH dư vào dung dịch chứa 50 gam muối, lọc kết tủa thu được đem nung trong chân không đến khối lượng không đổi thu được m gam oxit. Giá trị của m là
A. 31,44. B. 18,68. C. 23,32. D. 12,88.
Lời giải:
Hướng dẫn:
Khối lượng O có trong 50 gam hỗn hợp muối A là:
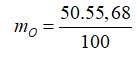
Bảo toàn nguyên tố O ta có: nNO3- (muối)= 1/3.nO= 0,58 mol
→ mkim loại= mA- mNO3-= 50- 0,58.62=14,04 gam
Bảo toàn điện tích ta có: nNO3-= nđiện tích dương kim loại= 2.nO2- trong oxit
→ nO2- trong oxit= 0,58/2= 0,29 mol
→moxit= mkim loại+ mO2- trong oxit= 14,04 + 0,29.16=18,68 gam
Đáp án B
Bài 86: A là hỗn hợp muối Cu(NO3)2, Fe(NO3)3, Fe(NO3)2, Al(NO3)3. Trong đó N chiếm 16,03% về khối lượng. Cho dung dịch KOH dư vào dung dịch chứa 65,5 gam muối. Lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được bao nhiêu gam oxit?
A. 27 B. 34 C. 25 D. 31
Lời giải:
Hướngdẫn:
Khối lượng N có trong 65,5 gam hỗn hợp muối A là:
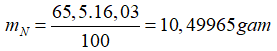
Bảo toàn nguyên tố N ta có: nNO3- (muối)= nN= 0,75 mol
→ mkim loại= mA- mNO3-= 65,5- 0,75.62=19 gam
Bảo toàn điện tích ta có: nNO3-= nđiện tích dương kim loại= 2.nO2- trong oxit
→ nO2- trong oxit= 0,75/2= 0,375 mol
→moxit= mkim loại+ mO2- trong oxit= 19 + 0,375.16=25 gam
Đáp án C
Bài 87: Hòa tan hoàn toàn hỗn hợp gồm 0,12 mol FeS2 và a mol Cu2S vào axit HNO3 (vừa đủ) thu được dung dịch X (chỉ chứa hai muối sunfat) và khí duy nhất NO. Giá trị của a là:
A. 0,04 B. 0,075 C. 0,12 D. 0,06
Lời giải:
Hướng dẫn:
Ta có sơ đồ phản ứng :
FeS2, Cu2S+ HNO3 →Fe2(SO4)3+ CuSO4+ NO+ H2O
Bảo toàn nguyên tố Fe ta có: nFe2(SO4)3= 1/2. nFeS2= 0,12/2= 0,06 mol
Bảo toàn nguyên tố Cu ta có: nCuSO4= 2.nCu2S= 2 a mol
Bảo toàn nguyên tố S có nS( FeS2, Cu2S)= nS (trong 2 muối sunfat)
Nên 2.0,12+ a= 3.0,06+ 2a→ a= 0,06 mol
Đáp án D
Bài 88: Cho 10,62 gam hỗn hợp gồm Fe, Zn vào 800 ml dung dịch hỗn hợp X gồm NaNO3 0,45 M và H2SO4 0,9M. Đun nóng cho phản ứng xảy ra hoàn toàn thu được dung dịch Y và 3,584 lít khí NO (sản phẩm khử duy nhất, đo ở đktc). Tính % khối lượng Fe trong hỗn hợp ban đầu.
A. 63,28% B. 36,72% C. 58,26% D. 41,74%
Lời giải:
Hướng dẫn:
Số mol NaNO3 = 0,36 mol
số mol H2SO4 = 0,72 mol → số mol H+ = 1,44 mol
Ta có các bán phản ứng:
NO3- + 4H+ + 3e → NO + 2H2O (1)
mol 0,16 ← 4.0,16 0,16.3 ← 0,16
Số mol NO = 0,16 mol => H+ và NO3- dư, kim loại phản ứng hết.
Số mol NO3- phản ứng = 0,16 mol; số mol H+ phản ứng = 0,64 mol
Fe → Fe3+ + 3e(1)
Zn → Zn2+ + 2e(2)
Gọi số mol Fe là x mol, số mol Zn là y mol
Theo khối lượng hỗn hợp ban đầu ta có phương trình
56 x + 65 y = 10,62 (I)
Theo định luật bảo toàn electron ta có phương trình
3x + 2y = 0,16.3 (II)
Giải hệ phương trình (I), (II) ta có: x = 0,12 và y = 0,06 mol
mFe = 0,12.56 = 6,72 g => % mFe = 63,28%
Bài 89: Khi cho cùng một lượng kim loại M vào dung dịch HNO3 đặc nóng dư và dung dịch H2SO4 loãng dư, phản ứng hoàn toàn thì thể tích khí NO2 (sản phẩm khử duy nhất) thu được gấp 3 lần thể tích khí H2 ở cùng điều kiện nhiệt độ và áp suất. Khối lượng muối sunfat thu được bằng 62,81% khối lượng muối nitrat tạo thành. Xác định kim loại M?
A. Zn B. Fe C. Mg D. Ca
Lời giải:
Hướngdẫn:
Gọi n, m là hóa trị của R khi tác dụng HNO3 và H2SO4 loãng ( 1≤ m≤ n≤ 3)
Chọn nR= 1 mol
2R + mH2SO4 →R2(SO4)m + mH2↑
1 → 0,5 0,5m
R + 2nHNO3 →R(NO3)n + nNO2 + nH2O
1 1 n
Ta có: n=3.0,5m → n=1,5m → m=2, n=3 là phù hợp.
Ta có: (R + 96)=(R + 186). 0,6281 → R=56 R là Fe.
Đáp án B
Bài 90: Cho 4,48 lít khí NH3 (đktc) qua lượng dư CuO nung nóng, sau một thời gian phản ứng thu được hỗn hợp khí và hơi Y có tỉ khối so với H2 bằng 9,5. Hiệu suất của phản ứng trên là:
A. 30% B. 40% C. 50% D. 60%
Lời giải:
Hướng dẫn:
Ta có: n NH3= 0,2 mol
2NH3+ 3CuO → N2+ 3Cu+ 3H 2O
nPỨ 2x x 3x mol
Hỗn hợp khí và hơi Y thu được có :
x mol N2, 3x mol H2O, 0,2-2x mol NH3 dư
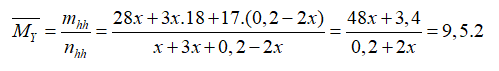
→x= 0,04 mol
→
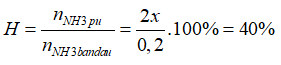
Đáp án B
Bài 91: Cho 7,68 gam Cu vào 200 ml dung dịch gồm HNO3 0,6M và H2SO4 0,5M. Sau khi các phản ứng xảy ra hoàn toàn (sản phẩm khử duy nhất là NO), cô cạn cẩn thận toàn bộ dung dịch sau phản ứng thì khối lượng muối khan thu được là:
A. 19,76 gam B. 20,16 gam
C. 19,20 gam D. 22,56 gam
Lời giải:
Hướngdẫn:
nCu= 0,12 mol; nHNO3= 0,12 mol; nH2SO4= 0,1 mol
3Cuhết + 8H+hết + 2NO3-dư→ 3Cu2+ + 2NO + 4H2O
0,12 0,32 0,12 → 0,12
nNO3- dư= 0,12- 0,12.2/3= 0,04 mol
Muối khan thu được có chứa: 0,12 mol Cu2+, 0,04 mol NO3- và 0,1 mol SO42-
→ mmuối khan= 0,12.64+ 0,04.62+ 0,1.96= 19,76 gam
Bài 92: Cho Zn tới dư vào dung dịch gồm HCl; 0,05 mol NaNO3 và 0,1 mol KNO3. Sau khi kết thúc các phản ứng thu được dung dịch X chứa m gam muối; 0,125 mol hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí. Tỉ khối của Y so với H2 là 12,2. Giá trị của m gần nhất với:
A. 64 gam B. 65 gam C. 70 gam D. 75 gam
Lời giải:
Hướngdẫn:
MY= 24,4 → Y chứa H2. Khí không màu hóa nâu ngoài không khí là NO → Y chứa NO và H2.
Gọi x và y lần lượt là số mol của H2 và NO
Ta có: x+ y= 0,125; 2x+ 30y= 0,125.24,4 → x= 0,025; y= 0,1
Vì có khí H2 thoát ra và Zn dư → H+ và NO3- hết → Muối thu được là muối clorua
Do nNO3(-)ban đầu= 0,15 mol > nNO= 0,1 mol→ X chứa NH4+
Theo bảo toàn nguyên tố N → nNH4+= 0,15-0,1= 0,05 mol
Theo bảo toàn electron: 2.nZn pứ= 3.nNO+ 8nNH4++ 2nH2= 0,75 mol→ nZn pứ= nZn2+= 0,375 mol
→mmuối= mZnCl2+ mNH4Cl+ mNaCl+ mKCl= 136. 0,375+ 53,5.0,05+ 58,5.0,05+ 74,5.0,1= 64,05 gam
Đáp án A
Bài 93: Hòa tan hết 14,6 gam hỗn hợp gồm Zn và ZnO có tỉ lệ mol 1:1 trong 250 gam dung dịch HNO3 12,6% thu được dung dịch X và 0,336 lít khí Y (đktc). Cho từ từ 740 ml dung dịch KOH 1M vào dung dịch X thu được 5,94 gam kết tủa. Nồng độ phần trăm của Zn(NO3)2 trong dung dịch X là:
A. 28,02% B. 14,29%
C. 14,32% D. 12,37%
Lời giải:
Hướng dẫn:
Ta có nZn = nZnO = 0,1 mol, nHNO3 = 0,5 mol
Kết tủa thu được là Zn(OH)2: 0,06 mol
Vậy dung dịch sau phản ứng + KOH chứa K2ZnO2: (0,1 + 0,1 - 0,06) = 0,14 mol và KNO3: (0,74 - 2 × 0,14) = 0,46 mol
Bảo toàn nguyên tố N → nN(Y) + nNH4 + = 0,5 - 0,46 = 0,04 mol
Nếu khí Y chứa 1 nguyên tố N (NO và NO2) → nNH4+ = 0,04 - 0,015 = 0,025
Bảo toàn electron→ số electron trao đổi của Y là: 0,1×2−0,025×80,015 = 0 (Vô lý)
Vậy khí Y chứa 2 nguyên tố N (N2, N2O) → nNH4+ = 0,04 - 0,015 × 2 = 0,01 mol
Bảo toàn electron → số electron trao đổi của Y là: 0,1×2−0,01×80,015 = 8 → khí tạo thành là N2O
Bảo toàn khối lượng → mdd = 14,6 + 250 - 0,015 × 44 = 263,94 gam
C% Zn(NO3)2 = (0,2×189/ 263,94 )×100% = 14,32%

Bài 94: Cho 39,84 gam hỗn hợp X1 gồm Fe3O4 và Cu vào dung dịch HNO3 đun nóng, thu được 0,2/3 mol NO (sản phẩm khử duy nhất, ở đktc), dung dịch Y1 và 3,84 gam Cu. Cho từ từ đến dư dung dịch NH3 vào dung dịch Y1, không có không khí, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 27 gam B. 46,6 gam C. 40,5 gam D. 42,5 gam
Lời giải:
Hướng dẫn:
Gọi nFe3O4 =x mol; nCu (phản ứng) = y mol
3Fe 3O4 + 28HNO3 → 9Fe(NO3)3 + NO + 14H2O (1)
3Cu + 8 HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (2)
Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2 (3)
Fe(NO3)2 + 2NH3 + 2H2O→ Fe(OH)2 + 2NH4NO3 (4)
Cu(NO3)2 + 2NH3 + 2H2O → Cu(OH)2 + 2NH4NO3 (5)
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (6)
Ta có hệ: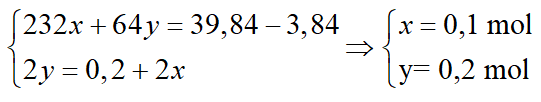
Đáp án A
Bài 95: Để 26,88 gam phôi Fe ngoài không khí một thời gian, thu được hỗn hợp rắn X gồm Fe và các oxit. Hòa tan hết X trong 288 gam dung dịch HNO3 31,5%, thu được dung dịch Y chứa các muối và hỗn hợp khí Z gồm 2 khí, trong đó oxi chiếm 61,11% về khối lượng. Cô cạn Y, rồi nung đến khối lượng không đổi thấy khối lượng chất rắn giảm 67,84 gam. Xác định nồng độ % Fe(NO3)3 trong Y?
A. 28,14% B. 26,36% C. 24,47% D. 25,19%
Lời giải:
Hướngdẫn:
2Fe(NO3)2 → Fe2O3 + 4NO2 + 1/2O2
a mol → 2a 0,25a
2Fe(NO3)3 → Fe2O3 +6NO2 + 3/2O2
b mol → 3b 0,75b
Ta có hệ:
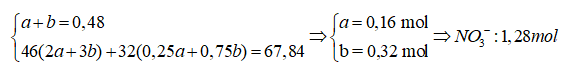
nN(trong Z)=1,44-1,28=0,16 mol→ mZ=(0,16.14.100)/(100-61,11)=5,76 gam
Sơ đồ: X + HNO3 → Muối + Z + H2O
→ mX + 1,44.63 = 0,16.180 + 0,32.242 + 0,74.18
→ mX = 34,24 gam → m(dung dịch sau)=34,24+288 – 5,76=316,48 gam
Vậy: C%(Fe(NO3)3) = (0,32.242.100)/316,48 = 24,47%
Đáp án C
Bài 96: Cho hỗn hợp X gồm FeCO3, FeS2 tác dụng vừa đủ với dung dịch HNO3 đặc, nóng thu được dung dịch Y (chứa Fe(NO3)3; H2SO4) và 22,4 lít hỗn hợp khí Z gồm hai khí (đktc). Pha loãng dung dịch Y bằng nước cất để thu được 2 lít dung dịch có pH = 1. (Biết sản phẩm khử của N+5 là NO2). Khối lượng hỗn hợp X là:
A. 20,5 gam B. 22,5 gam C. 21,5 gam D. 23,5 gam
Lời giải:
Hướng dẫn:
FeCO3 + 4HNO3→ Fe(NO3)3 + CO2 + NO2 + 2H2O (1)
0,125 0,125 0,125 0,125
FeS2 + 18HNO3 →Fe(NO3)3 + 2H2SO4 + 15NO2 + 7H2O (2)
0,05 0,05 0,1 0,75
Vì pH = 1→ [H+] = 0,1→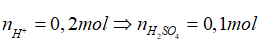
Theo (2) có: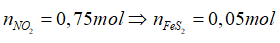
Gọi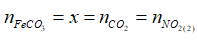
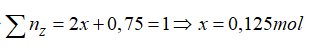
→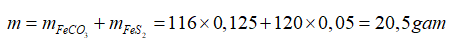
Đáp án A
Bài 97: Hòa tan hết 1 gam kim loại X trong lượng dư dung dịch HNO3 15%, thu được 446 ml (đktc) hỗn hợp Y gồm ba khí. Trong Y có chứa 117 mg N2 và 269 mg NO. Biết trong Y thì nguyên tố N chiếm 60,7% về khối lượng. Xác định kim loại X?
A. Zn B. Ca C. Ba D. Mg
Lời giải:
Hướng dẫn:
Gọi khí thứ 3 là NxOy, theo giả thiết ta có số mol các khí là
N2 = 4,1786.10-3 mol; NO = 8,967.10-3 mol; NxOy = 6,765.10-3 mol.
Suy ra %N =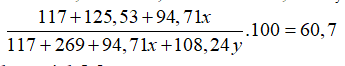
→8,2 +94,71x = 4,1.MNxOy
Xét các giá trị của x = 1, 2, 3 không có oxit nào của nitơ thõa mãn
→ x= 0 và M = 2, khí thứ 3 là H2
Dùng bảo toàn e → X = 12.n. Vậy n = 2 và X = 24, kim loại là Mg
PTHH: 9Mg + 22HNO3 → 9 Mg(NO3)2 + N2 + 2NO + H2 + 10H2O
Đáp án D
Bài 98: Cho 11,2 gam Fe vào 300 ml dung dịch chứa (HNO3 0,5M và HCl 2M) thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Cô cạn dung dịch X thu được bao nhiêu gam chất rắn khan?
A. 27,775 gam B. 27,175 gam
C. 28,125 gam D. 28,325 gam
Lời giải:
Hướng dẫn:
nFe = 0,2 mol;
nHNO3 = 0,15; nHCl = 0,6 → nH+= 0,75, nNO3- =0,15; nCL- =0,6
Fe + 4H+ + NO3- → Fe3+ + NO + 2 H2O (1)
0,15 ← 0,6 ← 0,15 → 0,15
Do sau phản ứng (1) thì Fe dư nên:
Fe + 2Fe3+ → 3Fe2+
0,05 → 0,1 → 0,15
Dung dịch X có Fe2+ (0,15 mol); Fe3+ (0,05 mol); H+ (0,15 mol); Cl- (0,6 mol)
Cô cạn dung dịch X được 2 muối: FeCl2 (0,15 mol) và FeCl3 (0,05 mol)
→ mmuối = 27,175 gam
Đáp án B
Bài 99: Hòa tan hoàn toàn 26,4 gam hỗn hợp A gồm Fe và Cu trong dung dịch HNO3, thu được 7,84 lít NO (đktc) và 800 ml dung dịch X. Cho từ từ dung dịch HCl vào X đến khi không còn khí thoát ra, thì thu được thêm 1,12 lít NO (đktc). Xác định % khối lượng của Cu trong A là:
A. 63,64% B. 36,36%
C. 45,28% D. 54,72%
Lời giải:
Hướng dẫn:
X + HCl → NO
=> trong X còn muối Fe(NO3)2
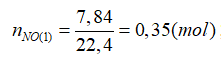
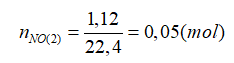
Sau khi cho HCl vào X thì thu được dung dịch trong đó chứa: Cu2+ và Fe3+
Gọi x, y lần lượt là số mol của Fe và Cu
QT cho e:
Fe→ Fe3++ 3e
Cu → Cu2++ 2e
QT nhận e:
N+5+ 3e→ NO
Theo định luật bảo toàn e: 3x+2y= 3. (0,35+0,05)
Ta có:
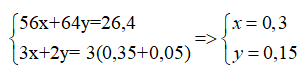
→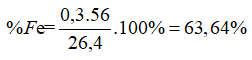
Đáp án B
Bài 100: Hòa tan 4,8 gam kim loại M hoặc hòa tan 2,4 gam muối sunfua của kim loại này, bằng dung dịch HNO3 đặc nóng dư, thì đều thu được lượng khí NO2 (sản phẩm khử duy nhất) như nhau. Xác định kim loại M?
A. Mg B. Ca C. Fe D. Cu
Lời giải:
Hướng dẫn:
(1) Phương trình phản ứng:
M + 2mH+ + mNO3- Mm+ + mNO2 + mH2O (1)
M2Sn + 4(m+n)H+ + (2m+6n)NO3- 2Mm+ + nSO42- + (2m+6n)NO2 + 2(m+n)H2O (2)
(2) Vì số mol NO2 ở hai trường hợp là bằng nhau nên ta có:
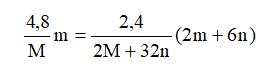
→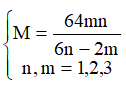
Vậy M là Cu và công thức muối là Cu2S.
Đáp án D
Bài 101: Có 4 dung dịch đựng trong 4 lọ mất nhãn là: (NH4)2SO4, NH4Cl, Na2SO4, NaOH. Nếu chỉ được phép sử dụng một thuốc thử để nhận biết 4 dung dịch trên, có thể dùng dung dịch:
A. AgNO3 B. Ba(OH)2 C. KOH D. BaCl2
Lời giải:
Đáp án B
Hướng dẫn giải :
Cho dung dịch Ba(OH)2 vào 4 dung dịch trên:
-Dung dịch làm xuất hiện kết tủa trắng và khí có mùi khai thì đó là (NH4)2SO4
(NH4)2SO4+ Ba(OH)2 → BaSO4↓+ 2NH3↑+ 2H2O
-Dung dịch nào xuất hiện chất khí mùi khai thì đó là NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2+ 2NH3↑ + 2H2O
-Dung dịch nào xuất hiện kết tủa trắng thì đó là Na2SO4
Ba(OH)2+ Na2SO4 → BaSO4 ↓ + 2NaOH
-Không có hiện tượng gì thì đó là NaOH
Bài 102: Cho các dung dịch: (NH4)2SO4, NH4Cl; Al(NO3)3; Fe(NO3)2; Cu(NO3)2. Để phân biệt các dung dịch trên chỉ có thể chỉ dùng 1 hóa chất là:
A. dung dịch NH3 B. dung dịch Ba(OH)2
C. dung dịch KOH D. dung dịch NaCl
Lời giải:
Đáp án B
Hướng dẫn giải:
Cho dung dịch Ba(OH)2 vào 5 dung dịch trên:
-Dung dịch làm xuất hiện kết tủa trắng và khí có mùi khai thì đó là (NH4)2SO4
(NH4)2SO4+ Ba(OH)2 → BaSO4↓+ 2NH3↑+ 2H2O
-Dung dịch nào xuất hiện chất khí mùi khai thì đó là NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2+ 2NH3↑ + 2H2O
-Dung dịch nào xuất hiện kết tủa keo trắng sau đó tan trong kiềm dư thì đó là Al(NO3)3
2Al(NO3)3+ 3Ba(OH)2→ 3Ba(NO3)2+ 2Al(OH)3↓
2Al(OH)3+ Ba(OH)2 → Ba(AlO2)2+ 4H2O
-Dung dịch nào làm xuất hiện kết tủa màu xanh thì đó là Cu(NO3)2
Cu(NO3)2+ Ba(OH)2→ Ba(NO3)2+ Cu(OH)2↓
-Dung dịch nào làm xuất hiện kết tủa trắng xanh sau đó hóa nâu ngoài không khí thì đó là Fe(NO3)2
Fe(NO3)2+ Ba(OH)2→ Ba(NO3)2+ Fe(OH)2↓
Bài 103: Dùng hóa chất nào sau đây để nhận biết các dung dịch: (NH4)2SO4, AlCl3, FeCl3, CuCl2, ZnCl2?
A. dung dịch NH3 B. dung dịch NaOH
C. dung dịch Ba(OH)2 D. dung dịch Ca(OH)2
Lời giải:
Đáp án A
Hướng dẫn giải:
Cho dung dịch NH3 dư lần lượt vào các dung dịch trên ta có:
-Dung dịch nào làm xuất hiện kết tủa trắng thì đó là AlCl3
AlCl3+ 3NH 3+ 3H2O → Al(OH)3 ↓ + 3NH4Cl
-Dung dịch nào làm xuất hiện kết tủa nâu đỏ thì đó là FeCl3
FeCl3+ 3NH 3+ 3H2O → Fe(OH)3 ↓ + 3NH4Cl
-Dung dịch nào làm xuất hiện kết tủa xanh lam sau đó tan trong NH3 dư tạo dung dịch xanh thẫm thì đó là CuCl2
CuCl2+ 2NH3+ 2H2O → Cu(OH)2 ↓ + 2NH4Cl
Cu(OH)2+ 4NH3 → [Cu(NH3)4](OH)2
-Dung dịch nào làm xuất hiện kết tủa trắng sau đó tan trong NH3 dư tạo dung dịch trong suốt thì đó là ZnCl2
ZnCl2+ 2NH3+ 2H2O → Zn(OH)2 ↓ + 2NH4Cl
Zn(OH)2+ 4NH3 → [Zn(NH3)4](OH)2
Bài 104: Để phân biệt các dung dịch riêng biệt đựng trong các lọ mất nhãn: NH4 NO3, (NH4)2CO3, ZnCl2, BaCl2, FeCl2 chỉ cần dùng 1 thuốc thử là:
A. dung dịch NaOH B. dung dịch HCl
C. dung dịch CaCl2 D. quỳ tím
Lời giải:
Đáp án A
Hướng dẫn giải:
Cho dung dịch NaOH vào các dung dịch trên:
-Dung dịch nào làm xuất hiện chất khí có mùi khai thì đó là NH4NO3 và (NH4)2CO3
NaOH + NH4NO3 → NaNO3+ NH3+ H2O
2NaOH + (NH4)2CO3 → Na2CO3+ 2NH3+ 2H2O
-Dung dịch nào làm xuất hiện kết tủa trắng sau đó tan trong kiềm dư thì đó là ZnCl2
ZnCl2+ 2NaOH → Zn(OH)2 ↓ + 2NaCl
Zn(OH)2 + 2NaOH → Na2ZnO2+ 2H2O
-Dung dịch nào xuất hiện kết tủa trắng xanh sau đó hóa nâu ngoài không khí thì đó là FeCl2
FeCl2+ 2NaOH → Fe(OH)2 ↓ + 2NaCl
-Dung dịch nào không có hiện tượng gì thì đó là BaCl2
Lấy dung dịch BaCl2 vừa nhận được ở trên vào NH4NO3 và (NH4)2CO3:
-Dung dịch nào làm xuất hiện kết tủa trắng thì đó là (NH4)2CO3
(NH4)2CO3+ BaCl2 → BaCO3 ↓ + 2NH4Cl
-Dung dịch nào không có hiện tượng gì thì đó là NH4NO3
Bài 105: Cho 6 lọ mất nhãn chứa 6 dung dịch sau: NH4Cl, NaNO3, (NH4)2SO4, CuSO4, MgCl2, ZnCl2. Chỉ dùng hóa chất nào sau đây có thể nhận ra cả 6 chất trên?
A. quỳ tím B. dung dịch NaOH
C. dung dịch Ba(OH)2 D. NH3
Lời giải:
Đáp án C
Hướng dẫn giải:
Cho dung dịch Ba(OH)2 vào 6 dung dịch trên:
-Dung dịch làm xuất hiện kết tủa trắng và khí có mùi khai thì đó là (NH4)2SO4
(NH4)2SO4+ Ba(OH)2 → BaSO4↓+ 2NH3↑+ 2H2O
-Dung dịch nào xuất hiện chất khí mùi khai thì đó là NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2+ 2NH3↑ + 2H2O
-Dung dịch nào xuất hiện kết tủa keo trắng sau đó tan trong kiềm dư thì đó là ZnCl2
ZnCl2+ Ba(OH)2 → Zn(OH)2 ↓ + BaCl2
Zn(OH)2 + Ba(OH)2→ BaZnO2+ 2H2O
-Dung dịch nào làm xuất hiện kết tủa màu xanh thì đó là CuSO4
CuSO4+ Ba(OH)2→ BaSO4+ Cu(OH)2↓
-Dung dịch nào làm xuất hiện kết tủa trắng thì đó là MgCl2
MgCl2+ Ba(OH)2→ BaCl2+ Mg(OH)2↓
-Không có hiện tượng gì thì đó là NaNO3
Bài 106: Cho cácmẫuphânbónsau: KCl , Ca(H2PO4)2 , NH4H2PO4và NH4NO3 . Dùng 1 hóa chất nào sau đây có thể phân biệt được các mẫu phân bón trên?
A. dung dịch NaOH B. dung dịch Ca(OH)2 C. dung dịch BaCl2 D. dung dịch AgNO3
Lời giải:
Đáp án B
Hướng dẫn giải:
Cho dung dịch Ca(OH)2 vào các dung dịch trên:
-Nếu xuất hiện kết tủa trắng thì đó là Ca(H2PO4)2:
Ca(H2PO4)2+ 2Ca(OH)2 → Ca3(PO4)2+ 4H2O
-Nếu vừa xuất hiện chất khí có mùi khai và kết tủa trắng thì đó là NH4H2PO4
2NH4H2PO4 + 3Ca(OH)2 → Ca3(PO4)2+ 2NH3+ 6H2O
-Nếu xuất hiện chất khí có mùi khai thì đó là NH4NO3:
2NH4NO3+ Ca(OH)2 → Ca(NO3)2+ 2NH3+ 2H2O
Bài 107: Cho 37,8 gam hỗn hợp X gồm NH4NO3 và (NH4)3PO4 tác dụng hết với dung dịch Ba(OH)2 dư thu được 15,68 lít khí (đktc). Tính % khối lượng (NH4)3PO4 có trong hỗn hợp X?
A. 21,16% B. 78,84% C. 25,56% D. 74,44%
Lời giải:
Đáp án B
Hướng dẫn giải:
2NH4NO3 + Ba(OH)2 → Ba(NO3)2+ 2NH3↑+ 2H2O
2(NH4)3PO4 + 3Ba(OH)2 → Ba3(PO4)2+ 6NH3↑+6 H2O
Đặt nNH4NO3= x mol; n(NH4)3PO4= y mol → 80x + 149 y= 37,8 gam
Ta có nNH3= x + 3y = 15,68/ 22,4 mol
Giải hệ trên ta có x= 0,1 và y= 0,2 mol
→%m(NH4)3PO4= 0,2.149.100%/37,8= 78,84%
Bài 108: Có m gam hỗn hợp X gồm 2 muối NH4Cl và (NH4)3PO4 được chia thành 2 phần bằng nhau:
Phần 1: cho tác dụng với dung dịch KOH dư thu được 10,08 lít khí (đktc)
Phần 2: cho tác dụng với dung dịch AgNO3 dư thu được 63,1375 gam kết tủa
Giá trị của m là?
A. 22,6375 gam B. 45,275 gam C. 20,35 gam D. 40,7 gam
Lời giải:
Đáp án B Hướng dẫn giải: -Phần 1 : NH4Cl + KOH →KCl + NH3↑ + H2O (NH4)3PO4+ 3KOH → K3PO4+ 3NH3 ↑ + 3H2O -Phần 2 : NH4Cl + AgNO3→AgCl ↓ + NH4NO3 (NH4)3PO4+ 3AgNO3 → Ag3PO4 ↓ + 3NH4NO3 Đặt số mol NH4Cl và (NH4)3PO4 có trong mỗi phần lần lượt là x, y mol Ta có : nkhí= nNH3= x + 3y = 10,08/22,4= 0,45 mol Ta có : mkết tủa= mAgCl+ mAg3PO4= 143,5x+ 419 y= 63,1375 gam Giải hệ trên ta có : x= 0,075 mol và y= 0,125 mol → m= 2. (53,5.0,075+149.0,125)=45,275 gam
Bài 109: Nhiệt phân 40 gam NH4NO3 (rắn khan). Sau một thời gian thấy khối lượng chất rắn còn lại là 10 gam. Tính thể tích khí và hơi thu được ở đktc?
A. 22,4 lít B. 23,52 lít C. 25,2lít D. 33,6 lít
Lời giải:
Đáp án C
Hướng dẫn giải:
NHNO3 → N2O + 2H2O
x x 2x mol
Khối lượng chất rắn giảm chính là do N2O và H2O bay hơi
→mN2O+ mH2O= 44x + 2x.18= 80x = 40-10=30 gam → x= 0,375 mol
→Vkhí và hơi= 3x.22,4=25,2 lít
Bài 110: Cho 1,605 gam NH4Cl tác dụng với dung dịch Ba(OH)2 dư, đun nóng thu được một sản phẩm khí. Hấp thụ hoàn toàn lượng khí trên vào dung dịch chứa 3,92 gam H3PO4. Muối thu được là:
A. NH4H2PO4 B. (NH4)2HPO4
C. (NH4)3PO4 D. NH4H2PO4 và (NH4)2HPO4
Lời giải:
Đáp án A
Hướng dẫn giải:
2NH4Cl + Ba(OH)2 → BaCl2+ 2NH3+ 2H2O
Ta có: nNH3= nNH4Cl= 0,03 mol; nH3PO4= 0,04 mol
Ta thấy T= nNH3/ nH3PO4= 0,03/ 0,04= 0,75 ⟨1
→Muối thu được là NH4H2PO4
NH3+ H3PO4 → NH4H2PO4
Bài 111: Thổi từ từ khí NH3 đến dư vào 250 gam dung dịch CuSO4 8%. Khi thổi V1 (lít, đktc) khí NH3 thì lượng kết tủa thu được là cực đại. Tiếp tục thổi thêm V2 (lít, đktc) khí NH3 thì kết tủa vừa tan hết thu được dung dịch có màu xanh thẫm. Giá trị của V1, V2 lần lượt là:
A. 5,6 lít; 11,2 lít B. 5,6 lít; 5,6 lít
C. 2,8 lít ; 11,2 lít D. 2,8 lít ; 5,6 lít
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có : mCuSO4= 250.8%=20 gam → nCuSO4= 0,125 mol
CuSO4+ 2NH3+ 2H2O → Cu(OH)2 ↓ + (NH4)2SO4
Ta có: nNH3= 2.nCuSO4= 2.0,125= 0,25 mol → V1= 0,25.22,4= 5,6 lít
Cu(OH)2+ 4NH3 → [Cu(NH3)4](OH)2
Ta có nNH3= 4nCu(OH)2= 4.nCuSO4= 4.0,125=0,5 mol → V2= 0,5.22,4 = 11,2 lít
Bài 112: Dẫn khí NH3 dư vào 500 ml dung dịch AlCl3 0,3M; CuCl2 0,2M; FeCl2 0,3 M. Sau phản ứng thu được kết tủa A. Lọc lấy kết tủa A đem nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là?
A. 27,65 gam B. 19,65 gam C. 18,45 gam D. 21,25 gam
Lời giải:
Đáp án B
Hướng dẫn giải:
Ta có : nAlCl3= 0,15 mol ; nCuCl2= 0,1 mol ; nFeCl2= 0,15 mol
AlCl3+ 3NH3+ 3H2O → Al(OH)3+ 3NH4Cl
FeCl2+ 2NH3+ 2H2O → Fe(OH)2+ 2NH4Cl
CuCl2+ 4NH3 → [Cu(NH3)4]Cl2
Kết tủa A có Al(OH)3: 0,15 mol và Fe(OH)2: 0,15 mol
2Al(OH)3 → Al2O3+ 3H2O
2Fe(OH)2 +1/2 O2 → Fe2O3+2 H2O
Ta có m gam chất rắn chứa 0,075 mol Al2O3 và 0,075 mol Fe2O3
→ m= 0,075.102+ 0,075.160= 19,65 (gam)
Bài 113: Dẫn khí NH3 dư vào 100 ml dung dịch chứa Al(NO3)3 0,1M; Zn(NO3)2 0,2M và AgNO3 0,15M. Sau phản ứng thu được m gam kết tủa. Giá trị của m là?
A. 0,78 g B. 1,65 g C. 1,02 g D. 0,98 g
Lời giải:
Đáp án A
Hướng dẫn giải:
Al(NO3)3+ 3NH3+ 3H2O → Al(OH)3+ 3NH4NO3
Zn(NO3)2+ 4NH3 → [Zn(NH3)4] (NO3)2
AgNO3+ 2NH3 → [Ag(NH3)2] NO3
Sau phản ứng m gam kết tủa có Al(OH)3
Ta có nAl(OH)3= nAl(NO3)3= 0,1.0,1= 0,01 mol → mAl(OH)3= 0,01.78= 0,78 gam
Bài 114: Hòa tan 54,44 gam hỗn hợp X gồm PCl3 và PBr3 vào nước được dung dịch Y. Để trung hòa hoàn toàn Y cần dùng 500 ml dung dịch KOH 2,6M. Tính % khối lượng của PCl3 trong X là:
A. 26,96% B. 12,125% C. 8,08% D. 30,31%
Lời giải:
Đáp án D
Hướng dẫn giải:
Gọi số mol PCl3 là x mol; số mol PBr3 là y mol
Phương trình phản ứng :
PCl3 + 3H2O → H3PO3+ 3HCl
x x 3x mol
PBr3+ 3H2O → H3PO3+ 3HBr
y y 3y mol
Dung dịch Y phản ứng với KOH
HX + KOH → KX + H2O
(3x+3y)
H3PO3 + 2KOH → K2HPO3 + 2H2O
(x+y) 2(x+y) mol
Ta có 137,5x + 271 y= 54,44; nKOH= 5x + 5y= 1,3 mol
Giải hệ trên ta có x= 0,12 và y= 0,14
%mPCl3= 30,31%
Bài 115: Thủy phân hoàn toàn 13,75 gam PCl3 thu được dung dịch X gồm hai axit. Trung hòa dung dịch X cần thể tích dung dịch NaOH 0,1M là:
A. 4 lít B. 5 lít C. 3 lít D. 6 lít
Lời giải:
Đáp án B
Hướng dẫn giải:
PCl3+ 3H2O → H3PO3 + 3HCl
0,1 0,3 0,1 0,3 mol
Trung hòa dung dịch X vào NaOH:
HCl + NaOH → NaCl + H2O
0,3 0,3 mol
H3PO3+ 2NaOH → Na2HPO3+ 2H2O
0,1 0,2 mol
Ta có nNaOH= 0,5 mol → VddNaOH = 0,5/0,1= 5 (lít)
Bài 116: Cho 2,13 gam P2O5 tác dụng với 80 ml dung dịch NaOH 1M. Sauk hi các phản ứng xảy ra hoàn toàn thu được dung dịch X chứa m gam muối. Bỏ qua sự thủy phân của các ion, giá trị của m là:
A. 4,70 B. 4,48 C. 2,46 D. 4,37
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có: nP2O5= 0,015 mol → nH3PO4= 0,03 mol
nNaOH= 0,08 mol ⟨ 0,09 mol
Áp dụng định luật bảo toàn khối lượng ta có 0,03.98 + 0,08.40= m + 0,08.18 → m= 4,7 gam

Bài 117: Cho m gam P2O5 vào 1 lít dung dịch hỗn hợp NaOH 0,2M và KOH 0,3M đến phản ứng hoàn toàn thu được dung dịch X. Cô cạn cẩn thận X thu được 35,4 gam hỗn hợp muối khan. Giá trị của m là :
A. 21,3 gam B. 28,4 gam C. 7,1 gam D. 14,2 gam
Lời giải:
Đáp án D
Hướng dẫn giải:
Ta có: nOH-= 0,2 + 0,3= 0,5 mol →nH2O= 0,5 mol
Theo định luật bảo toàn khối lượng ta có: mH3PO4+ 0,2.40 + 0,3.56= 35,4+ 0,5.18 → mH3PO4= 19,6 gam
→ nH3PO4= 0,2 mol→ nP2O5= 0,1 mol (bảo toàn nguyên tố P)→ m= mP2O5= 0,1.142= 14,2 gam
Bài 118: Đốt cháy hoàn toàn 6,2 gam P trong khí O2 dư thu được chất rắn X. Cho X vào 200 ml dung dịch NaOH 1,25M. Khối lượng muối tạo thành trong dung dịch là:
A. 18,0 gam NaH2PO4 và 7,1 gam Na2HPO4
B. 14,2 gam Na2HPO4 và 16,4 gam Na3PO4
C. 7,1 gam Na2HPO4 và 8,2 gam Na3PO4
D. 6,0 gam NaH2PO4 và 21,3 gam Na2HPO4
Lời giải:
Đáp án A
Hướng dẫn giải:
4P + 5O2 → 2P2O5
Ta có: nP2O5= 0,5. nP= 0,1 mol; nNaOH= 0,2. 1,25= 0,25 mol
Ta có: 2⟨ T= →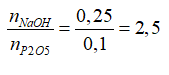
P2O4 + 2NaOH + H2O → 2NaH2PO4
x 2 x 2x mol
P2O5 + 4 NaOH → 2Na2HPO4+ H2O
y 4y 2y mol
Ta có: nP2O5= x + y = 0,1 mol; nNaOH= 2x + 4y= 0,25 mol
→ x= 0,075 mol; y = 0,025 mol
→ mNaH2PO4= 2x. 120= 18 gam; mNa2HPO4= 2y. 142= 7,1 gam
Bài 119: Hòa tan hết 0,15 mol P2O5 vào 200 gam dung dịch H3PO4 9,8% thu được dung dịch X. Cho X tác dụng hết với 750 ml dung dịch NaOH 1M thu được dung dịch Y. Hỏi trong Y có chứa những hợp chất nào của P và khối lượng tương ứng là bao nhiêu (bỏ qua sự thủy phân của các muối)?
A. 45,0 gam NaH2PO4 ; 17,5 gam Na2HPO4
B. 30,0 gam NaH2PO4; 35,5 gam Na2HPO4
C. 21,3 gam NaH2PO4; 24,6 gam Na3PO4
D. 42,6 gam Na2HPO4; 8,2 gam Na3PO4
Lời giải:
Đáp án B
Hướng dẫn giải:
nH3PO4= 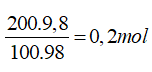
P2O5+ 3H2O → 2 H3PO4
0,15 0,3 mol
→ Tổng số mol H3PO4 là 0,3 + 0,2 = 0,5 mol; nNaOH= 0,75 mol
→Tỉ lệ T=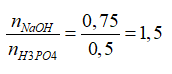
→ NaOH phản ứng với H3PO4 theo phương trình sau:
NaOH + H3PO4 → NaH2PO4 + H2O
x x x mol
2NaOH + H3PO4 → Na2HPO4 + 2H2O
2y y y mol
Ta có: nNaOH= x + 2y= 0,75 mol và nH3PO4= x + y= 0,5 mol
→ x= 0,25; y= 0,25 → mNaH2PO4= 30 gam; mNa2HPO4= 35,5 gam
Bài 120:Cho 21,30 gam P2O5 vào V lít dung dịch NaOH 1M, thu được dung dịch trong đó có chứa 38,20 gam hỗn hợp muối photphat. Giá trị của V là:
A. 0,40 lít B. 1,00 lít C. 0,60 lít D. 0,44 lít
Lời giải:
Đáp án A
Hướng dẫn giải:
P2O5+ 3H2O → 2 H3PO4
0,15 0,3 mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Theo các PT ta có: nH2O= nNaOH= V (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O →40. V + 0,3.98= 38,20 + 18.V → V= 0,4 lít
Bài 121: Cho 15,62 gam P2O5 vào 400 ml dung dịch NaOH nồng độ a M thu được dung dịch có tổng khối lượng các chất tan bằng 24,2 gam. Giá trị của a là:
A. 0,2 B.0,3 C. 0,4 D. 0,5
Lời giải:
Đáp án B
Hướng dẫn giải:
P2O5+ 3H2O → 2H3PO4
0,11 0,22mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Nếu chất tan trong dung dịch chỉ chứa các muối thì:
Theo các PT ta có: nH2O= nNaOH= 0,4a (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O →0,4a. 40 + 0,22.98= 24,2 + 0,4a.18 → a= 0,3 M
Bài 122: Hòa tan hoàn toàn m gam P2O5 vào dung dịch chứa 0,7 mol NaOH, sau phản ứng thu được dung dịch chỉ chứa 2,1033m gam muối. Tỉ lệ mol của P2O5 và NaOH gần nhất với:
A. 0,214 B. 0,286 C. 0,429 D. 0,143
Lời giải:
Đáp án A
Hướng dẫn giải:
P2O5+ 3H2O → 2 H3PO4
m/142 2m/142 mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Vì dung dịch sau phản ứng chỉ chứa muối nên ta có: nH2O= nNaOH= 0,7 (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O → 0,7.40 + (2m/142).98=2,1033m + 0,7.18 →m = 21,3 gam
→nP2O5= 0,15 mol → 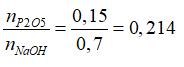
Bài 123: Đun nóng hỗn hợp Ca và P đỏ. Hoà tan sản phẩm thu được vào dd HCl dư thu được 28lít khí ở đktc. Đốt cháy khí này thành P2O5. Lượng oxit thu được tác dụng với dung dịch kiềm tạo thành 142g Na2HPO4. Xác định thành phần % về khối lượng mỗi chất trong hỗn hợp đầu.
A. 69,31%; 30,69% B. 35,57%; 64,43%
C. 30%; 70% D. 40%; 60%
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có nkhí= 1,25 mol; nNa2HPO4= 1 mol
3Ca + 2P → Ca3P2 (1)
Sản phẩm thu được có chứa Ca3P2, có thể có Ca dư hoặc P dư
Ca3P2+ 6HCl→ 3CaCl2+ 2PH3↑ (2)
Ca + 2HCl → CaCl2+ H2 ↑ (3)
2PH3+ 4O2 → P2O5+ 3H2O (4)
1 ← 0,5 mol
P2O5+ 4NaOH → 2Na2HPO4+ H2O (5)
0,5 ← 1 mol
Theo PT (2), (4), (5) ta thấy nPH3= nNa2HPO4= 1 mol ⟨1,25 mol → Sản phẩm khí phải có H2
→ nH2= 1,25- 1 = 0,25 mol→ nCa dư= nH2= 0,25 mol
Theo PT (2): nCa3P2= 0,5. nPH3= 0,5 mol
Theo PT (1): nCa pứ= 3.nCa3P2= 1,5 mol; nP pứ= 2.nCa3P2= 2.0,5= 1 mol
nCa banđầu= nCa pứ + nCa dư= 0,25 + 1,5= 1,75 mol
→Trong hỗn hợp đầu có: mCa= 1,75.40= 70 gam; mP= 1.31= 31 gam
→%mCa= 69,31%; %mP= 30,69%
Bài 124: Tiến hành nung một loại quặng chứa Ca3(PO4)2 hàm lượng 70% với C và SiO2 đều lấy dư ở 10000C. Tính lượng quặng cần lấy để có thể thu được 62 g P. Biết hiệu suất phản ứng đạt 80%.
A. 484,375 gam B. 553,6 gam C. 310 gam D. 198,4 gam
Lời giải:
Đáp án B
Hướng dẫn giải:
Ca3(PO4)2+ 3SiO2+ 5C → 3 CaSiO3+ 2P + 5 CO
Ta có nCa3(PO4)2= 0,5. nP= 0,5. 2= 1,0 mol → mCa3(PO4)2= 1. 310= 310 (gam)
→ Khối lượng quặng cần lấy là:
mquặng=
Bài 125: Tính lượng P cần dùng để có thể điều chế được 100 ml dung dịch H3PO4 31,36% (d = 1,25 gam/ml). Biết hiệu suất phản ứng đạt 100%.
A. 3,1 gam B. 6,2 gam C. 9,3 gam D. 12,4 gam
Lời giải:
Đáp án D
Hướng dẫn giải:
Khối lượng dung dịch H3PO4 là mdung dịch= V. D=100. 1,25= 125 gam
→ mH3PO4= 125.31,36/100= 39,2 gam → nH3PO4= 0,4 mol
Bảo toàn nguyên tố P ta có: nP= nH3PO4= 0,4 mol → mP= 12,4 gam
Bài 126: Lấy V(ml) dung dịch H3PO4 35% ( d = 1,25gam/ml ) đem trộn với 100 ml dung dịch KOH 2M thu được dung dịch X có chứa 14,95 gam hỗn hợp 2 muối K3PO4 và K2HPO4. Tính V?
A. 15,12 ml B. 16,8 ml C. 18,48 ml D. 18,6 ml.
Lời giải:
Đáp án B
Hướng dẫn giải:
H3 PO4 + 2KOH → K2HPO4+ 2H2O
x 2x x mol
H3PO4 + 3KOH → K3PO4 + 3H2O
y 3y y mol
Ta có: nKOH= 2x + 3y= 0,1.2= 0,2 mol
mhỗn hợp muối= 174x + 212 y= 14,95 gam
Giải hệ trên ta có: x= 0,025 mol; y = 0,05 mol → nH3PO4= x+y= 0,075 mol
→ mH3PO4= 0,075. 98= 7,35 gam →mdung dịch H3PO4 35%= 7,35.100/35= 21 (gam)
→Vdd = m/D= 21/1,25= 16,8 ml
Bài 127: Trộn lẫn 200 gam dung dịch K2HPO4 17,4% với 100 gam dung dịch H3PO4 9,8%. Tính nồng độ % của 2 muối photphat trong dung dịch thu được ?
A. 9,07%; 5,8% B. 9,07%; 6,2%
C. 8,07%; 5,8% D. 8,07%; 6,2%
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có: nK2HPO4= 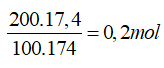
K2HPO4+ H3PO4 → 2KH2PO4
0,2 0,1 0,2 mol
Ta có: 0,2 >0,1 nên K2HPO4 dư
Ta có dung dịch thu được có chứa 0,2 mol KH2PO4 và 0,1 mol K2HPO4 dư
Ta có: mdung dịch= 200 + 100= 300 gam
C%KH2PO4 = 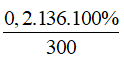
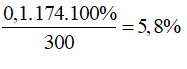
Bài 128: Khối lượng quặng photphorit chứa 65% Ca3(PO4)2 cần lấy để điều chế 150 kg photpho là (có 3% P hao hụt trong quá trình sản xuất).
A. 1,189 tấn B. 0,2 tấn C. 0,5 tấn D. 2,27 tấn
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có sơ đồ: Ca3(PO4)2 → 2P
Ta có: nCa3(PO4)2= 0,5.nP= 0,5.150/31= 75/31 (kmol) → mCa3(PO4)2= (75/31).310= 750 (kg)
→ Khối lượng Ca3(PO4)2 thực tế cần có: 750.100/97=773,2 kg
→Khối lượng quặng photphoric cần lấy là: 773,2.100/65= 1189 kg= 1,189 tấn
Bài 129: Cho m gam P2O5 vào 700 ml dung dịch KOH 1M, sau khi kết thúc phản ứng, cô cạn dung dịch thu được (3m+5,4) gam chất rắn. Giá trị của m là:
A. 14,2 B. 28,4 C. 21,3 D. 7,1
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có: nP2O5=m/142 mol
-TH1: Chất rắn khan chỉ chứa các muối
P2O5+ 3H2O → 2 H3PO4
m/142 2m/142 mol
KOH + H3PO4 → KH2PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
3KOH + H3PO4 → K3PO4 + 3H2O
Vì dung dịch sau phản ứng chỉ chứa muối nên ta có: nH2O= nKOH= 0,7 (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mKOH + mH3PO4= mmuối + mH2O → 0,7.56+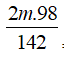
→ nH3PO4= 2m/142= 0,184 mol → T= 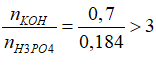
-TH2: Chất rắn khan chứa muối và KOH dư
P2O5+ 3H2O → 2 H3PO4
m/142 2m/142 mol
3KOH + H3PO4 → K3PO4 + 3H2O
6m/142 2m/142 2m/142 mol
Chất rắn khan chứa 2m/142 mol K2PO4 và (0,7- 6m/142 ) mol KOH
→ 212. 2m/142 + 56. (0,7- 2m/142 ) =3m+5,4 → m= 14,2 gam
Bài 130: Đốt cháy hoàn toàn m gam P bằng oxi rồi hòa tan hoàn toàn sản phẩm cháy vào dung dịch chứa 0,1 mol H2SO4 thu được dung dịch X. Cho 0,5 mol KOH vào X, sau khi các phản ứng xảy ra hoàn toàn cô cạn dung dịch thu được 943m/62 gam chất rắn. Giá trị của m là:
A. 2,17 B. 2,48 C. 3,1 D. 3,72
Lời giải:
Đáp án B
Hướng dẫn giải:
Ta có: 4P + 5O2 → 2P2O5 (1)
Cho sản phẩm cháy vào dung dịch chứa 0,1 mol H2SO4 thì:
P2O5+ 3H2O → 2H3PO4 (2)
Ta có: nH3PO4= nP= m/31 mol
Dung dịch X chứa H3PO4 và H2SO4
Cho 0,5 mol KOH phản ứng với dung dịch X:
2KOH + H2SO4 → K2SO4+ 2H2O (3)
0,2 ← 0,1 → 0,1 mol
→ Số mol KOH phản ứng với H3PO4 là 0,5- 0,2= 0,3 mol
KOH + H3PO4 → KH2PO4 + H2O (4)
2KOH + H3PO4 → K2HPO4 + 2H2O (5)
3KOH + H3PO4 → K3PO4 + 3H2O (6)
-TH1: Chất rắn sau phản ứng chỉ chứa các muối
→ nH2O= nKOH= 0,5 mol
Theo định luật bảo toàn khối lượng ta có:
mKOH+ maxit= mmuối + mH2O → 0,5.56+ 0,1.98+ 98.m/31 =943m/62+ 0,5.18 → m=2,39 gam
→nH3PO4= nP=0,077 mol →T= 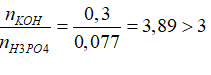
TH2: Chất rắn sau phản ứng có KOH dư
3KOH + H3PO4 → K3PO4 + 3H2O (6)
3m/31 m/31 m/31 mol
Chất rắn sau phản ứng có chứa 0,1 mol K2SO4;m/31 mol K3PO4 và (0,3- 3m/31 mol)KOH dư
→ 0,1.174+ m/31. 212+ (0,3- 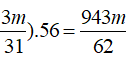
Bài 131: Cho 2,13 gam P2O5 tác dụng hết với V ml dung dịch NaOH 1M, sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chỉ chứa 4,48 gam muối. Giá trị của V là:
A. 15 ml B. 70 ml C. 45 ml D. 60 ml
Lời giải:
Đáp án B
Hướng dẫn giải:
Ta có: nP2O5= 2,13/142= 0,015 mol
P2O5+ 3H2O → 2 H3PO4
0,015 0,03 mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Do trong dung dịch chỉ chứa các muối nên:
Theo các PT ta có: nH2O= nNaOH= V.1/1000= 0,001V (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O →0,001V. 40 + 0,03.98= 4,48 + 0,001V.18 →V= 70 ml
Bài 132: Hòa tan 3,82 gam hỗn hợp X gồm NaH2PO4, Na2HPO4 và Na3PO4 vào nước dư thu được dung dịch Y. Trung hòa hoàn toàn Y cần 50 ml dung dịch KOH 1M thu được dung dịch Z. Khối lượng kết tủa thu được khi cho Z tác dụng hết với dung dịch AgNO3 dư là:
A. 20,95 gam B. 16,76 gam C. 12,57 gam D. 8,38 gam
Lời giải:
Đáp án C
Hướng dẫn giải:
Gọi số mol NaH2PO4, Na2HPO4 và Na3PO4 lần lượt là x, y, z mol
→ 120x+ 142y + 164z= 3,82 (*1)
Trung hòa Y bằng dung dịch KOH:
H2PO4-+ 2OH- → PO43-+ 2H2O (1)
x 2x x mol
HPO42-+ OH- → PO43-+ H2O (2)
y y y mol
Theo PT (1) và (2) ta có nOH-= 2x+ y= 0,05 mol (*2)
Nhân cả 2 vế của (*2) với 22 ta có 44x + 22y= 1,1 gam (*3)
Công theo vế của (*1) với (*3|) ta có: 164x +164y + 164 z= 1,1+ 3,82=4,92
→ x + y +z= 0,03 mol
Tổng số mol PO43- có trong dung dịch Z là x+ y+z (mol)
3Ag++ PO43- → Ag3PO4 ↓ (3)
Theo PT (3) ta có nAg3PO4= nPO4(3-)= x+ y+z= 0,03 mol → mAg3PO4= 0,03.419= 12,57 gam
Bài 133: Cho 11,36 gam P2O5 vào 200 ml dung dịch NaOH 0,4M và Ba(OH)2 0,3M. Sau khi kết thúc phản ứng, thu được dung dịch X. Cô cạn dung dịch X thu được lượng rắn khan là:
A. 16,22 B. 13,52 C. 25,54 D. 20,54
Lời giải:
Đáp án C
Hướng dẫn giải:
Ta có : nP2O5= 0,08 mol ; nNaOH= 0,08 mol ; nBa(OH)2= 0,06 mol ; nOH-= 0,08 + 2.0,06= 0,2 mol
P2O5+ 3H2O → 2 H3PO4
0,08 0,16mol
Ta có T= nOH-/nH3PO4= 1,25 → 1 ⟨ T ⟨ 2 → OH- tác dụng với H3PO4 theo phương trình :
OH-+ H3PO4 → H2PO4- + H2O
x x x mol
2OH-+ H3PO4 → HPO42-+ 2H2O
2y y y mol
Ta có: nOH-= x + 2y= 0,2 mol ; nH3PO4= x + y= 0,16 mol →x= 0,12 và y= 0,04
Cô cạn dung dịch X thu được chất rắn khan chứa 0,12 mol H2PO4- và 0,04 mol HPO42- ; 0,08 mol N+ và 0,06 mol Ba2+ → mchất rắn khan= 0,12. 97+ 0,04.96+ 0,08.23 + 0,06.137=25,54 gam
Bài 134: Cho 200 ml dd H3PO4 1,5M tác dụng với 250ml dd NaOH 2M. Sau phản ứng thu được muối gì và có khối lượng là bao nhiêu?
A. 24 gam NaH2PO4 và 28,4 gam Na2HPO4 B. 12 gam NaH2PO4 và 28,4 gam Na2HPO4
C. 24 gam NaH2PO4 và 14,2 gam Na2HPO4 D. 12 gam NaH2PO4 và 14,2 gam Na2HPO4
Lời giải:
Đáp án B
Hướng dẫn giải:
Ta có: nH3PO4= 0,3 mol; nNaOH= 0,5 mol
Ta có 1⟨ T= nNaOH/ nH3PO4=1,67⟨2
→ NaOH tác dụng với H3PO4 theo 2PTHH:
NaOH + H3PO4 → NaH2PO4+ H2O
2NaOH + H3PO4 → Na2HPO4+ 2H2O
Đặt nNaH2PO4= x mol; nNa2HPO4= y mol
Ta có nH3PO4= x+ y= 0,3 mol; nNaOH= x + 2y= 0,5 mol → x=0,1; y= 0,2
→ mNaH2PO4= 12gam; mNa2HPO4=28,4 gam

Bài 135: Cho 20g dung dịch H3PO4 37,11% tác dụng vừa đủ với NH3 thì thu được 10g muối photphat amoni A. Công thức của muối A là:
A. (NH4)2HPO4 B. NH4H2PO4
C. (NH4)3PO4 D. Không xác định
Lời giải:
Đáp án A
Hướng dẫn giải:
Ta có nH3PO4= 0,07573 mol
Đặt công thức của muối amoni là (NH4)nH3-nPO4
H3PO4+ n NH3 →(NH4)nH3-nPO4
Ta có nmuối= nH3PO4= 0,07573 mol→ Mmuối A= 10/ 0,07573= 132 g/mol
→ 18n + 3-n+ 95= 132 → n= 2 → Công thức của muối A là (NH4)2HPO4
Bài 136: Một mẫu supephotphat đơn khối lượng 15,55 gam chứa 35,43% Ca(HPO4)2 còn lại CaSO4. Độ dinh dưỡng của loại phân bón trên là:
A. 21,46% B. 61,20% C. 16% D. 45,81%
Lời giải:
Đáp án A
Hướng dẫn giải:
Khối lượng Ca(H2PO4)2 có trong 15,55 gam supephotphat đơn là :
mCa(H2PO4)2= 15,55. 35,43%= 5,5 gam → nCa(H2PO4)2= 5,5/234= 0,0235 mol
Bảo toàn nguyên tố P ta có: nCa(H2PO4)2= nP2O5= 0,0235 mol → mP2O5= 0,0235. 142= 3,337 (gam)
Độ dinh dưỡng của phân lân được tính bằng %P2O5có trong phân
→Độ dinh dưỡng của phân bón trên là:
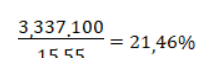
Bài 137: Phân kali (KCl) được sản xuất từ quặng sinvinit thường chỉ có 50% K2O. Hàm lượng % của KCl trong phân bón đó là:
A. 39,6 B. 69,3 C. 72,9 D. 79,3
Lời giải:
Đáp án D
Hướng dẫn giải:
Giả sử khối lượng quặng sinvinit là 100 gam
mK2O= 50 gam → nK2O = 0,532 mol
Bảo toàn nguyên tố K ta có nKCl= 1,064 mol→ mKCl= 1,064. 74,5=79,268 gam
Bài 138: Một loại phân kali chứa 59,6% KCl; 34,5% K2CO3 về khối lượng, còn lại là SiO2. Độ dinh dưỡng của loại phân bón trên là:
A. 61,10 B. 49,35 C. 50,70 D. 60,20
Lời giải:
Đáp án A
Hướng dẫn giải:
Giả sử có 100 gam phân → nKCl= 0,8 mol; nK2CO3= 0,25 mol
Bảo toàn nguyên tố K ta có nK2O= 0,65 mol
Vậy độ dinh dưỡng của phân là: 0,65. 94= 61,1%
Bài 139: Quá trình tổng hợp supephotphat kép diễn ra theo sơ đồ sau:
Ca3(PO4)2 →H3PO4 →Ca(H2PO4)2
Tính khối lượng dung dịch H2SO4 70% đã dùng để điều chế được 351 kg Ca(H2PO4)2 theo sơ đồ biến hóa trên. Biết hiệu suất của quá trình là 70%.
A. 800 kg B. 600 kg C. 500 kg D. 420 kg
Lời giải:
Đáp án B
Hướng dẫn giải:
Ta áp dụng bảo toàn nguyên tố hiđro:
nCa(H2PO4)2= 1,5 kmol → nH= 1,5.4= 6 kmol → nH2SO4= 3 kmol
→mH2SO4= 3.98= 294 (kg)→ mddH2SO4 70% = 294. 100/70= 420 (kg)
Biết hiệu suất của quá trình là 70% →mddH2SO4 70% thực tế =420.100/70= 600 (kg)
Bài 140: Người ta điều chế supephotphat đơn từ một loại bột quặng có chứa 73% Ca3(PO4)2 , 26% CaCO3, và 1% SiO2. Khối lượng dung dịch H2SO4 65% đủ để tác dụng với 100 kg bột quặng là:
A. 100 kg B. 110,1 kg C. 120 kg D. 150 kg
Lời giải:
Đáp án B
Hướng dẫn giải:
Trong 100 kg bột quặng ta có: mCa3(PO4)2= 100. 73%= 73 kg; mCaCO3= 100.26%= 26 kg
→ nCa3(PO4)2= 73/ 310 (kmol)=0,235 kmol; nCaCO3= 26/100= 0,26kmol
Ca3(PO4)2+ 2H2SO4 → Ca(H2PO4)2+ 2CaSO4
0,235 → 0,47 kmol
CaCO3+ H2SO4 → CaSO4+ CO2+ H2O
0,26 → 0,26 kmol
→ Tổng số mol H2SO4 là 0,47 + 0,26= 0,73 kmol → mH2SO4= 0,73.98= 71,54 (kg)
→ mddH2SO4 = 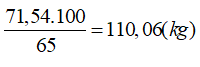
Bài 141: Một loại phân supephotphat kép có chứa 69,62% muối canxi đihiđrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là
A. 48,52%. B. 42,25%. C. 39,76%. D. 45,75%.
Lời giải:
Đáp án B
Hướng dẫn giải:
Trong 100 gam phân supephotphat kép có: mCa(H2PO4)2= 69,62 gam
→ nCa(H2PO4)2= 69,62/243= 0,2975 mol
→ nP2O5= nCa(H2PO4)2= 0,2975 mol → mP2O5= 0,2975.142= 42,25 (gam)
Độ dinh dưỡng của phân lân được tính bằng % khối lượng của P2o5 tương ứng có trong phân.
→Độ dinh dưỡng của loại phân bón này là 42,25%
Bài 142: Một loại phân kali có thành phần chính là KCl (còn lại là các tạp chất không chứa kali) được sản xuất từ quặng sinvinit có độ dinh dưỡng 55%. Phần trăm khối lượng của KCl có trong loại phân kali đó là:
A. 95,51% B. 65,75% C. 87,18% D. 88,52%
Lời giải:
Đáp án C
Hướng dẫn giải:
Độ dinh dưỡng của phân kali được tính bằng %mK2O
Xét 100 gam phân có 55 gam KO → nK2O= 55/ 94 (mol)
Bảo toàn nguyên tố K ta có: n KCl=2.n>K2O= 2.55/94= 55/47 mol → mKCl= 87,18 gam
→%mKCl= 87,18%
Bài 143:Phân lân supephotphat kép thực tế sản xuất được thường chỉ có 40% P2o5. Hàm lượng % của canxi đihiđrophotphat trong phân bón đó là:
A. 65,9 B. 56,9 C. 32,95 D. 69,5
Lời giải:
Đáp án A
Hướng dẫn giải:
Xét 100g phân bón có 40g P2O5 →nP2O5= 40/142 = 20/71 mol
Bảo toàn P: nCa(H2PO4)2=nP2O5= 20/71 (mol)
→mCa(H2PO4)2=65,92 g →%mCa(H2PO4)2=65,92%
Bài 144: Khối lượng dung dịch H2SO4 65% cần dùng để điều chế được 500 kg supephotphat kép là:
A. 677 kg B. 700 kg C. 644 kg D. 720 kg
Lời giải:
Đáp án C
Hướng dẫn giải:
Ca3(PO4)2+3H2SO4→3CaSO4+2H3PO4(1)
Ca3(PO4)2+4H3PO4→3Ca(H2PO4)2 (2)
Theo PTHH (1): nH2SO4= 1,5. nH3PO4
Theo PTHH (2): nH3PO4= 4/3. nCa(H2PO4)2 → nH2SO4= 2.nCa(H2PO4)2= 2. 500/234=500/117 (mol)
→ mH2SO4= 500/117. 98= 418,803 kg → mddH2SO4 65% = 644 kg
Bài 145: Khi cho khí NH3 tác dụng vừa đủ với 1,96 tấn axit photphoric khan theo tỉ lệ mol tương ứng là 3:2. Khối lượng phân amophot thu được là:
A. 24,7 tấn B. 2,47 tấn C. 1,15 tấn D. 1,32 tấn
Lời giải:
Đáp án B
Hướng dẫn giải:
NH3 + H3PO4 → NH4H2PO4
2NH3 + H3PO4→ (NH4)2HPO4
Phân amophot là hỗn hợp NH4 H2PO4 ; (NH4)2HPO4
Ta có: nH3PO4= 2.104 mol → nNH3= 1,5. nH3PO4= 3.104 mol
Theo bảo toàn khối lượng ta có:
mphân amophot= mNH3+ mH3PO4= 3.104.17+ 2.104.98=247.107 (g)= 2,47 tấn
Bài 146: Một loại phân bón amophot là hỗn hợp muối có thành phần số mol NH4H2PO4 và (NH4)2HPO4 là 1:1. Để điều chế loại phân bón này từ 6000 mol H3PO4 người ta cần dùng lượng NH3 có thể tích đo ở đkc là:
A. 201,6 m3 B. 153 m3 C. 20,6 m3 D. 32,5 m3
Lời giải:
Đáp án A
Hướng dẫn giải:
NH3 + H3PO4→ NH4 H2PO4
2NH3 + H3PO4 → (NH4)2HPO4
Đặt số mol NH4 H2PO4 là x mol → Số mol(NH4)2HPO4 là x mol
Theo 2 PT: nH3PO4= x+ x = 6000 mol → x= 3000 mol→ nNH3= x + 2x = 9000 mol
→ VNH3= 9000.22,4=201 600 lít= 201,6 m3
Bài 147: Phân đạm ure thường chỉ có 46% N. Khối lượng (kg) phân ure đủ cung cấp 70 kg N là:
A. 152,2 B. 145,5 C. 160,9 D. 200,0
Lời giải:
Đáp án A
Hướng dẫn giải:
Trong 1 phân tử (NH2)2CO, N chiếm 46% về khối lượng
→m(NH2)2CO=70.100/46=152,17 kg