Phản ứng oxi hóa ankan - Hoá học lớp 11
Phản ứng oxi hóa ankan
Với Phản ứng oxi hóa ankan Hoá học lớp 11 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Phản ứng oxi hóa ankan từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

A. Phương pháp giải & Ví dụ minh họa
Phản ứng đốt cháy ankan:
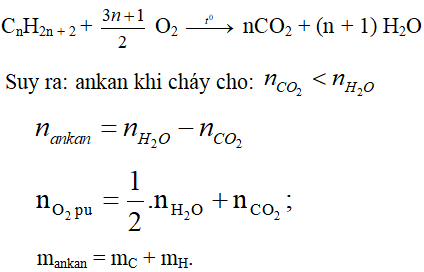
* Nếu có hỗn hợp gồm gồm hai ankan:
CnH2n + 2 : x mol
CmH2m + 2 : y mol
Gọi công thức trung bình của hai ankan là:

Ví dụ minh họa
Bài 1: Đốt cháy hoàn toàn 2,24 lít hỗn hợp X (đktc) gồm CH4, C2H6 và C3H8 thu được 4,48 lit khí CO2 (đktc) và m gam H2O. Giá trị của V là
Hướng dẫn:
nX = 2,24/22,4 = 0,1 mol; nCO2 = 4,48/22,4 = 0,2 mol
nX = nH2O - nCO2 ⇒ nH2O = nCO2 + nX = 0,2 + 0,1 = 0,3 mol
⇒ m = 0,3.18 = 5,4 (gam)
Bài 2: Đốt cháy hoàn toàn 6 gam hỗn hợp X gồm hai ankan cần hết 15,68 lít O2 (đktc). Hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong dư, thu được m gam kết tủa. Giá trị của m là
Hướng dẫn:


Bài 3: Đốt cháy hoàn toàn 1 hiđrocacbon A ( là chất khí, đkc) rồi dẫn sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 chứa NaOH dư người ta thấy khối lượng bình 1 tăng 1,8g và khối lượng bình 2 tăng 3,52 gam. Xác định CTPT của A.
Hướng dẫn:
Khối lượng bình 1 tăng là khối lượng của H2O ⇒ nH2O = 1,8/18 = 0,1 mol
Khối lượng bình 2 tăng là khối lượng của CO2 ⇒ nCO2 = 3,52/44 = 0,08 mol
Nhận thấy: nCO2 < nH2O ⇒ hidrocacbon là ankan;
Số mol ankan là nankan = 0,1 – 0,08 = 0,02 mol
Phương trình phản ứng:
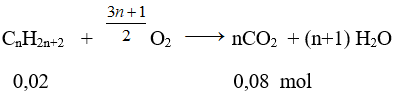
⇒ n = 0,08/0,02 = 4
CTPT của A là C4H10
Bài 4: Đốt cháy hoàn toàn 6,8g hỗn hợp khí X gồm: ankan A và CH4, sản phẩm cháy dẫn vào bình 1 đựng P2O5 và bình 2 đựng 1000 ml Ba(OH)2 0,5M. Sau thí nghiệm khối lượng bình 1 tăng 12,6g.
a. Tìm công thức phân tử của A, biết VA : VCH4 = 2 : 3.
b. Tính khối lượng các chất trong X.
c. Tính khối lượng muối tạo thành.
Hướng dẫn:
VA : VCH4 = 2 : 3 ⇒ nA : nCH4 = 2x : 3x
Khối lượng bình 1 tăng là khối lượng của H2O: nH2O = 12,6/18 = 0,7 mol
a. Gọi CTPT của ankan là CnH2n+2
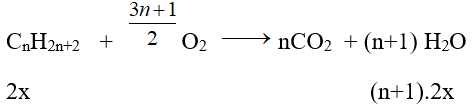
CH4 + 2O2 → CO2 + 2H2O
3x 6x
Ta có: (14n + 2).2x + 16.3x = 6,8 (1) ; (n + 1).2x + 6x = 0,7(2)
Từ 1, 2 ⇒ x = 0,05 và nx = 0,15 ⇒ n = 3
Vậy CTPT của A là C3H8
b. Khối lượng của mỗi an kan trong hỗn hợp X là
mC3H8 = 2.0,05.44 = 4,4 gam ⇒ mCH4 = 6,8 – 4,4 = 2,4 gam
c. Số mol CO2 tạo thành là nCO2 = 2.0,15 + 3.0,05 = 0,45 mol
Số mol Ba(OH)2 là: nBa(OH)2 = 1.0,5 = 0,5 mol
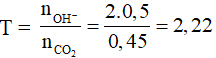
Khối lượng muối tạo thành: mBaCO3 = 0,45.197 = 88,65 gam
Bài 5: Đốt cháy hoàn toàn một lượng hi đrocacbon X. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ba(OH)2 (dư) tạo ra 29,55 gam kết tủa, dung dịch sau phản ứng có khối lượng giảm 19,35 gam so với dung dịch Ba(OH)2 ban đầu. Công thức phân tử X là
Hướng dẫn:
nC = nCO2 = nBaCO3 = 29,55/197 = 0,15 mol
mgiảm = mBaCO3 - (mCO2 + mH2O) = 19,35 mol ⇒ mCO2 + mH2O = 10,2g
mH2O = 10,2 – 0,15.44 = 3,6 (gam) ⇒ nH2O = 3,6/18 = 0,2 mol ⇒ nH = 0,4 mol
nC : nH = 0,15 : 0,4 = 3 : 8 ⇒ CTPT: C3H8
B. Bài tập trắc nghiệm
Bài 1: Đốt cháy hiđrocacbon X, rồi hấp thụ hoàn toàn sản phẩm cháy vào dd Ba(OH)2 dư, thấy có 49,25 gam kết tủa xuất hiện và khối lượng dd sau phản ứng giảm đi 32,85 gam. CTPT của X là:
A. C5H12 B. C2H6 C. C3H8 D. C4H10
Lời giải:
Đáp án: A
nCO2 = nBaCO3 = 49,25/197 = 0,25 mol ; mCO2 + mH2O = 49,25 – 32,85 = 16,4
mH2O = 16,4 – 0,25.44 = 5,4 ; nH2O = 5,4/18 = 0,3 mol ; nH2O > nCO2 ⇒ X là ankan ;
CTPT của X là : CnH2n+2 ; n = 0,25/0,05 = 5⇒ X : C5H12

Bài 2: Khi đốt cháy hoàn toàn 7,84 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được 16,8 lít khí CO2 (đktc) và x gam H2O. Giá trị của x là
A. 6,3. B. 13,5. C. 18,0. D. 19,8.
Lời giải:
Đáp án: D
nH2O = nCO2 + nhh = 16,8/22,4+ 7,84/22,4 = 1,1 mol ⇒ x = 1,1.18 = 19,8 gam
Bài 3: Đốt cháy hoàn toàn 4,48 lít hỗn hợp gồm C2H6 và C3H8 (đkc) rồi cho sản phẩm cháy đi qua bình 1 đựng H2SO4 đặc, bình 2 đựng dd nước vôi trong có dư thì thấy khối lượng bình 1 tăng m gam, bình 2 tăng 2,2 gam. Tính m.
A. 3,5 B. 4,5 C. 5,4 D. 7,2
Lời giải:
Đáp án: B
m = (4,48/22,4+ 2,2/44).18= 4,5 gam
Bài 4: Đốt cháy hết 2,24 lít ankan X (đktc), dẫn toàn bộ sản phẩm cháy vào dd nước vôi trong dư thấy có 40g kết tủa. CTPT X
A. C2H6 B. C4H10 C. C3H6 D. C3H8
Lời giải:
Đáp án: B
CTPT của X là CnH2n+2 ; n = nCO2 /nX = 4
Bài 5: Đốt cháy hoàn toàn 0,56 lit butan ( đktc) và cho sản phẩm cháy hấp thụ hoàn toàn vào 400ml dd Ba(OH)2 0,2M. Số gam kết tủa tạo thành:
A. 9,85g B. 9,98g C. 10,4g D.11,82g
Lời giải:
Đáp án: D
nC4H10 = 0,56/22,4 = 0,025 mol ⇒ nCO2 = 4.0,025 = 0,1 mol; nH2O = 5.0,025 = 0,125 mol; T = nOH-/nCO2 = 0,16/0,1 = 1,6 ⇒ tạo ra 2 muối; nCO32- = 0,06 ⇒ mCaCO3 = 0,06.197 = 11,82 gam
Bài 6: Đốt cháy hết 2,24 lít ankan X (đktc), dẫn toàn bộ sản phẩm cháy vào dd nước vôi trong dư thấy có 40g kết tủa. CTPT X
A. C2H6 B. C4H10 C. C3H6 D. C3H8
Lời giải:
Đáp án: B
CTPT của X là CnH2n+2 ; n = nCO2 /nX = 4

Bài 7: Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí Clo (theo tỉ lệ số mol 1 : 1) thu được một sản phẩm hữu cơ duy nhất . Tên gọi của X là
A. 2,2-đimetylpropan B. etan
C. 2-metylpropan D. 2- metylbutan
Lời giải:
Đáp án: A
nH2O > nCO2 ⇒ X là ankan
Có CTPT là CnH2n+2
nX = nH2O - nCO2 = 0,132 – 0,11 = 0,022 (mol)
⇒ 0,022n = 0,11 ⇒ n = 5 ⇒ CTPT: C5H12
C5H12 tác dụng với khí Clo thu được sản phẩm hữu cơ duy nhất nên CTCT của X là:
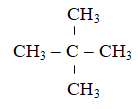
Bài 8: Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. thể tích không khí (dktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên niên trên là
A. 70,0 lít B. 78,4 lít C. 84,0 lít D. 56,0 lít.
Lời giải:
Đáp án: A
nCO2 = 7,84/22,4 - 0,35 mol; nH2O = 9,9/18 = 0,55 mol
Bảo toàn nguyên tố O:
2nO2 = 2nCO2 + nH2O ⇒ nO2 = 0,625 mol ⇒ VO2 = 0,625.22,4 = 14 lit
Vì oxi chiếm 1/5 Vkk ⇒ Vkk = 5.14 = 70 (lít)

