70 câu trắc nghiệm Cacbon, Silic có lời giải chi tiết (nâng cao) - Hoá học lớp 11
70 câu trắc nghiệm Cacbon, Silic có lời giải chi tiết (nâng cao)
Với 70 câu trắc nghiệm Cacbon, Silic có lời giải chi tiết (nâng cao) Hoá học lớp 11 tổng hợp 70 bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Cacbon, Silic từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

Bài 1:Có 5 lọ mất nhãn đựng 5 chất bột màu trắng: NaCl, Na2CO3, Na2SO4, BaCO3, BaSO4. Chỉ dùng nước và khí CO2 thì có thể nhận được mấy chất?
A. 2
B. 3
C. 4
D. 5
Lời giải:
Đáp án: D
*Hòa tan 5 chất rắn trên vào nước.
-Chất nào tan trong nước là NaCl, Na2CO3, Na2SO4 (nhóm I)
-Chất không tan trong nước là BaCO3, BaSO4 (nhóm II)
*Sục khí CO2 vào 2 chất ở nhóm II
-Chất nào tan thu được dung dịch trong suốt thì đó là BaCO3
BaCO3 + CO2 + H2O → Ba(HCO3)2
-Chất không tan là BaSO4
*Lấy dung dịch Ba(HCO3)2 thu được ở trên cho vào 3 chất ở nhóm I
-Chất nào xuất hiện làm xuất hiện kết tủa trắng thì đó là Na2CO3 và Na2SO4
Na2CO3 + Ba(HCO3)2 → BaCO3↓ + 2NaHCO3
Na2SO4 + Ba(HCO3)2 → BaSO4↓ + 2NaHCO3
-Chất nào không có hiện tượng gì là NaCl
*Sục khí CO2 vào 2 kết tủa trên:
-Chất nào tan thu được dung dịch trong suốt thì đó là BaCO3 → Chất ban đầu là Na2CO3
BaCO3 + CO2 + H2O → Ba(HCO3)2
-Chất không tan là BaSO4 → Chất ban đầu là Na2SO4
Bài 2:Hỗn hợp X gồm CuO và Fe2O3, Hòa tan hoàn toàn 44 gam X bằng dung dịch HCl dư, sau phản ứng thu được dung dịch chứa 85,25 gam muối. Mặt khác, nếu khử hoàn toàn 22 gam X bằng CO dư, cho hỗn hợp khí thu được sau phản ứng lội từ từ qua dung dịch Ba(OH)2 (dư) thì thu được m gam kết tủa. Giá trị của m là:
A. 76,755
B. 73,875
C.147,750
D. 78,875
Lời giải:
Đáp án B
Trong 22 gam hỗn hợp X ta đặt nCuO= x mol; nFe2O3= y mol
→ 80x + 160y= 22 gam (1)
- Hòa tan hoàn toàn 44 gam X bằng dung dịch HCl dư thu 85,25 gam muối.
→ Hòa tan hoàn toàn 22 gam X thu được 85,25/ 2= 42,625 gam
CuO + 2HCl → CuCl2 + H2O
x x mol
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
y 2y
Ta có: mmuối= mCuCl2 + mFeCl3=135x+ 162,5.2y= 42,625 gam (2)
Giải hệ gồm PT (1) và (2) ta có x=0,075 mol; y= 0,1 mol
CuO + CO
Fe2O3 + 3CO
Ta có: nCO2= nCuO + 3.nFe2O3= x + 3y= 0,375 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
→ nBaCO3= nCO2= 0,375 mol → mBaCO3= 0,375.197=73,875 gam
Bài 3:Cho 4,48 lít khí CO (ở đktc) từ từ qua ống sứ nung nóng đựng 8 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Khí thu được sau phản ứng có tỉ khối so với hiđro bằng 20. Công thức của oxit sắt và phần trăm thể tích của khí CO2 trong hỗn hợp khí sau phản ứng?
A. Fe3O4 ; 75%
B. Fe2O3; 75%
C. Fe2O3; 65%
D. FeO; 75%
Lời giải:
Đáp án B
Đặt công thức oxit sắt là FexOy có số mol là a mol
Ta có: nCO= 0,2 mol
FexOy + yCO
a ay ax ay mol
Sau phản ứng thu được ay mol CO2, (0,2-ay) mol CO dư
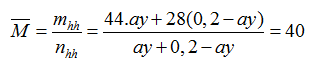
Ta có: mFexOy= a. (56x+16y)= 56ax + 16ay= 8 gam → ax=0,1 mol
→ Công thức oxit là Fe2O3
Sau phản ứng thu được 0,15 mol CO2 và 0,05 mol CO dư
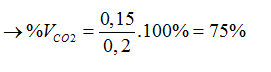
Bài 4:Khử hoàn toàn m gam oxit MxOy cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hòa tan hết a gam M bằng dung dịch H2SO4 đặc nóng dư thu được 20,16 lít SO2 (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là:
A. Cr2O3
B. FeO
C. Fe3O4
D. CrO
Lời giải:
Đáp án C
Ta có: nCO= 0,8 mol; nSO2= 0,9 mol
MxOy + yCO → xM + yCO2 (1)
Ta thấy đáp án M là Fe hoặc Cr nên M có số oxi hóa cao nhất là +3
2M + 6H2SO4 → M2(SO4)3 + 3SO2 + 6H2O (2)
Theo PT (2): nM= 2/3.nSO2= 0,6 mol
Theo PT (1):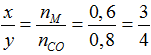
Bài 5:Dẫn luồng khí CO đi qua hỗn hợp gồm CuO và Fe2O3 nung nóng, sau một thời gian thu được chất rắn X và khí Y. Cho Y hấp thụ hoàn toàn vào dung dịch Ba(OH)2 dư thu được 29,55 gam kết tủa. Chất rắn X phản ứng với dung dịch HNO3 dư thu được V lít khí NO (sản phẩm khử duy nhất ở đktc). Giá trị của V là:
A. 2,24
B. 4,48
C. 6,72
D. 3,36
Lời giải:
Đáp án A
Ta có sơ đồ phản ứng:
CO + CuO, Fe2O3 → Chất rắn X chứa Cu, Fe, CuO dư, Fe2O3 dư, FeO, Fe3O4
Khí Y là CO2
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
Ta có: nCO2= nBaCO3= 29,55/197= 0,15 mol
Chất rắn X + HNO3 → Cu(NO3)2 + Fe(NO3)3
Áp dụng bảo toàn electron cho cả quá trình:
-QT cho electron:
C+2 → C+4+ 2e
0,15 0,15 0,3 mol
-QT nhận electron:
N+5+ 3e → NO
0,3 → 0,1 mol
→ VNO= 22,4. 0,1= 2,24 lít
Bài 6:Cho dòng khí CO đi qua ống sứ đựng 0,12 mol hỗn hợp X gồm FeO và Fe2O3 nung nóng, thu được 14,352 gam hỗn hợp rắn Y và 0,138 mol CO2. Hòa tan hết Y vào dung dịch HNO3 dư thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là:
A. 0,224
B. 0,672
C. 2,285
D. 6,857
Lời giải:
Đáp án C
Đặt nFeO= x mol; nFe2O3= y mol → x+y = 0,12 mol (1)
Bản chất phản ứng:
CO + Ooxit → CO2
ta có: nO (oxit)= nCO2= 0,138 mol
→ mX= mY + mO (oxit)= 14,352+ 0,138.16=16,56 gam → 72x + 160y= 16,56 (2)
Giải hệ (1) và (2) ta có: x= 0,03 mol; y= 0,09 mol
-QT cho electron:
FeO → Fe3++ 1e
0,03 0,03
C+2 → C+4+ 2e
0,138 0,276 mol
-QT nhận electron:
N+5+ 3e → NO
Theo định luật bảo toàn electron: ne cho= ne nhận → 0,03 + 0,276= 3.nNO
→ nNO=0,102 mol → VNO= 2,2848 lít= 2,285 lít
Bài 7:Thổi hơi nước qua than nóng đỏ thu được hỗn hợp khí X khô (H2, CO, CO2). Cho X qua dung dịch Ca(OH)2 thì còn lại hỗn hợp khí Y khô (H2, CO). Một lượng khí Y tác dụng vừa hết 8,96 gam CuO thấy tạo thành 1,26 gam nước. Thành phần % thể tích khí CO2 trong X là:
A. 20%
B. 11,11%
C. 30,12%
D. 29,16%
Lời giải:
Đáp án B
C + H2O
0,042 → 0,042
C + 2H2O
0,014 ← (0,07-0,042)
CO2 + Ca(OH)2 → CaCO3 + H2O (3)
CO + CuO
0,042 ← (0,112-0,07)
H2 + CuO
0,07 0,07 ← 0,07 mol
Ta có: nCuO= 0,112 mol; nH2O= 0,07 mol
Tính toán theo phương trình ta có: 0,042 mol CO; 0,014 mol CO2; 0,07 mol H2
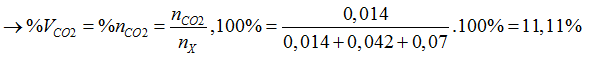
Bài 8:Cho hơi nước đi qua than nóng đỏ, thu được 15,68 lít hỗn hợp khí X (đktc) gồm CO, CO2 và H2. Cho toàn bộ X tác dụng hết với CuO dư nung nóng thu được hỗn hợp chất rắn Y. Hòa tan hết toàn bộ Y bằng dung dịch HNO3 loãng dư thu được 8,96 lít khí NO (sản phẩm khử duy nhất, ở đktc). Phần trăm thể tích khí CO trong X là:
A. 18,42%
B. 28,57%
C. 14,28%
D. 57,15%
Lời giải:
Đáp án B
Đặt nCO PT1= x mol; nCO 2 PT2= y mol
C + H2O
x x mol
C + 2H2O
y 2y mol
CO + CuO
x x
H2 + CuO 
(x+2y) (x+2y) mol
Hỗn hợp khí X có x mol CO, y mol CO2; (x+2y) mol H2
→ x + y + x+ 2y= 15,68/22,4= 0,7 mol hay 2x +3y= 0,7 mol (1)
Tổng số mol Cu là x+x+2y= 2x+ 2y mol
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO+ 4H2O (5)
Theo PT (5): nNO= 2/3. nCu= 2/3 (2x+2y)= 0,4 (2)
Giải hệ (1,2) ta có: x= 0,2; y= 0,1
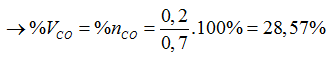
Bài 9:Hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 .Cho khí CO qua m gam X nung nóng, sau một thời gian thu được hỗn hợp chất rắn Y và hỗn hợp khí Z. Cho toàn bộ Z vào dung dịch Ca(OH)2 dư, đến khi phản ứng hoàn toàn, thu được 4 gam kết tủa. Mặt khác, hòa tan hoàn toàn Y trong dung dịch H2SO4 đặc nóng dư thu được 1,008 lít khí SO2 (đktc, sản phẩm khử duy nhất) và dung dịch chứa 18 gam muối. Giá trị của m là:
A. 7,12
B. 13,52
C. 6,8
D. 5,68
Lời giải:
Đáp án A
Quy hỗn hợp X chứa hai chất: FeO xmol và Fe2O3 y mol
Cho X+ khí CO → Chất rắn Y + khí Z chứa CO, CO2
CO2 + Ca(OH)2 → CaCO3 + H2O
Có: nCO2= nCaCO3= 0,04 mol
Cho Y + H2SO4 đặc nóng dư thu được nSO2=0,045 mol
-QT cho e:
FeO → Fe3++ 1e
x x mol
C+2 → C+4+ 2e
0,04 0,08 mol
-QT nhận electron:
S+6+ 2e → SO2
0,09 ← 0,045 mol
Theo định luật bảo toàn electron: ne cho= ne nhận → x+0,08 = 0,09 → x= 0,01mol
Muối thu được sau phản ứng là Fe2(SO4)3 → nFe2(SO4)3= 18/400= 0,045 mol
Bảo toàn nguyên tố Fe ta có: x+ 2y= 0,045.2 → y= 0,04 mol
→ m= mFeO + mFe2O3=72x + 160y= 72.0,01+ 160.0,04= 7,12 gam
Bài 10:Khi cho 3,36 lít (đo ở đktc) hỗn hợp khí X gồm N2, CO và CO2 đi qua CuO dư đốt nóng, rồi sục vào dung dịch nước vôi trong dư, thì thu được 10 gam kết tủa và 4,8 gam đồng. Thành phần % về thể tích của N2 trong hỗn hợp X là giá trị nào dưới đây?
A. 16,67%
B. 33,33%
C. 50,00%
D. 66,67%
Lời giải:
Đáp án B
Đặt nN2=x mol; nCO= y mol; nCO2= z mol → x+y+z=3,36/22,4= 0,15 mol
CO + CuO
y y y
ta có: y=nCu= 4,8/64= 0,075 mol; nCO2=y + z mol
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
Ta có: nCaCO3= nCO2= y+z= 10/100= 0,1 mol → z= 0,025 mol
→ x=0,05 mol → %VN2= %nN2=33,33%
Bài 11:Hòa tan hoàn toàn 12 gam hỗn hợp X gồm CuO, Fe2O3, MgO cần dùng vừa đủ 225 ml dung dịch HCl 2M. Mặt khác, nếu đốt nóng 12 gam X trong khí CO dư để phản ứng xảy ra hoàn toàn thì thu được 10 gam chất rắn Y. Phần trăm khối lượng Fe2O3 trong hỗn hợp X bằng:
A. 33,33%
B. 40,00%
C. 66,67%
D. 50,00%
Lời giải:
Đáp án A
Khi cho X tác dụng với HCl: nHCl= 0,225.2= 0,45 mol
CuO + 2HCl → CuCl2 + H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Đặt nCuO= x mol; nFe2O3= y mol; nMgO= z mol → 80x+ 160y +40z= 12 gam (1)
nHCl= 2x+6y+2z= 0,45 mol (2)
CO + CuO
x x mol
Fe2O3 + 3CO
y 2 y mol
Chất rắn Y chứa x mol Cu; 2y mol Fe và z mol MgO
→ 64x + 56.2y + 40z= 10 gam (3)
Từ các PT(1,2,3) ta có x= 0,05; y=0,025; z=0,1
→ %mFe2O3=33,33%
Bài 12:Thổi hơi nước qua than nóng đỏ thu được hỗn hợp khí X khô (H2, CO, CO2). Cho X qua dung dịch Ca(OH)2 thì còn lại hỗn hợp khí Y khô (H2, CO). Một lượng khí Y tác dụng vừa hết 20,8 gam Fe2O3 thấy tạo thành 4,86 gam nước. Thành phần % thể tích khí CO2 trong X là:
A. 20%
B. 11,11%
C. 16,13%
D. 29,16%
Lời giải:
Đáp án C
C + H2O
0,12 → 0,12
C + 2H2O
0,075 ← (0,27-0,12)
CO2 + Ca(OH)2 → CaCO3 + H2O (3)
3CO + Fe2O3
0,12 ← (0,13-0,09)
3H2 + Fe2O3
0,27 0,09 ← 0,27 mol
Ta có: nFe2O3= 0,13 mol; nH2O= 0,27 mol
Tính toán theo phương trình ta có: 0,12 mol CO; 0,075 mol CO2; 0,27 mol H2
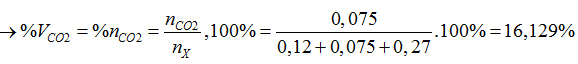
Bài 13:Cho 22,4 lít hỗn hợp X gồm hai khí CO, CO2 đi qua than nóng đỏ (không có mặt không khí) thu được khí Y có thể tích hơn thể tích X là 7,84 lít (thể tích khí đo được ở đktc). Dẫn Y đi qua dung dịch Ca(OH)2 vừa đủ thì thu được dung dịch chỉ chứa 20,25 gam Ca(HCO3)2. Thành phần phần trăm về thể tích của khí CO trong hỗn hợp X là:
A. 25%
B. 37,5%
C. 40%
D. 50%
Lời giải:
Đáp án C
Đặt nCO= x mol; nCO2= y mol trong hỗn hợp X → x+ y= 22,4/22,4= 1mol (1)
CO2 + C
z z 2z mol
Khí Y chứa 2z+x mol khí CO và y-z mol khí CO2
nY- nX= 7,84/22,4=0,35 mol → nY= 0,35+ 1= 1,35 mol
→ 2z +x + y-z= 1,35 → x+ y + z= 1,35 mol (2)
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ta có: nCO2= 2.nCa(HCO3)2= 2.20,25/162= 0,25 mol → y-z= 0,25 (3)
Từ (1,2,3) ta có x= 0,4; y= 0,6; z=0,35 mol
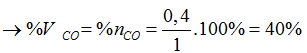
Bài 14:Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp khí X gồm CO2, CO, H2. Toàn bộ lượng khí X vừa đủ khử hết 48 gam Fe2O3 thành Fe và thu được 10,8 gam H2O. Phần trăm thể tích CO2 trong hỗn hợp khí X là:
A. 14,29
B. 28,57
C. 13,24
D. 16,14
Lời giải:
Đáp án A
C + H2O
0,3 → 0,3
C + 2H2O 
0,15 ← (0,6-0,3)
CO2 + Ca(OH)2 → CaCO3 + H2O (3)
3CO + Fe2O3
0,3 ← (0,3-0,2)
3H2 + Fe2O3
0,60 0,2 ← 0,6 mol
Ta có: nFe2O3= 0,3 mol; nH2O= 0,6 mol
Tính toán theo phương trình ta có: 0,3 mol CO; 0,15 mol CO2; 0,6 mol H2
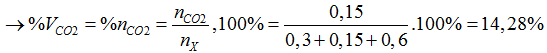
Bài 15:Cho hơi nước đi qua than nung nóng đỏ sau khi loại bỏ hơi nước thu được 17,92 lít (đktc) hỗn hợp khí X gồm CO2, CO và H2. Hấp thụ X vào dung dịch Ba(OH)2 dư thu được 35,46 gam kết tủa và có V lít khí Y thoát ra. Cho Y tác dụng với CuO dư nung nóng sau phản ứng thấy khối lượng chất rắn giảm m gam. Giá trị của m là:
A. 12,8
B. 2,88
C. 9,92
D. 2,08
Lời giải:
Đáp án C
Đặt nCO PT1= x mol; nCO2 PT2= y mol
C + H2O
x x mol
C + 2H2O
y 2y mol
→ nhỗn hợp X= nCO + nCO2 + nH2= 2x+ 3y= 17,92/22,4= 0,8 mol (*)
CO2 + Ba(OH)2 → BaCO3 + H2O (3)
nCO2= nBaCO3= 35,46/197=0,18 mol → y= 0,18 mol
Thay vào (*) ta có x=0,13 mol
Khí thoát ra là CO (0,13 mol); H2 (x+2y=0,49 mol)
CO + CuO
x x
H2 + CuO
(x+2y) (x+2y) mol
Khối lượng chất rắn giảm chính là khối lượng oxi trong oxit tách ra
Theo PT (4,5) ta có: nO (Oxit tách ra)= nCO + nH2= x+x+2y= 0,62 mol
→ m= 0,62.16= 9,92 gam
Bài 16:Trong bình kín chứa 0,5 mol CO và m gam hỗn hợp X gồm FeO, Fe3O4 , Fe2O3 (trong đó số mol FeO bằng số mol Fe2O3). Đun nóng bình cho tới khi phản ứng xảy ra hoàn toàn thì khí trong bình có tỉ khối so với khí CO ban đầu là 1,457. Giá trị của m là:
A. 16,8
B. 21,5
C. 22,8
D. 23,2
Lời giải:
Đáp án D
Do số mol FeO bằng số mol Fe2O3 nên ta có thể quy đổi hỗn hợp X thành Fe3O4
CO + Fe3O4 → CO2 + Chất rắn
Bản chất phản ứng:
CO + Ooxit → CO2
x x x mol
Khí trong bình có chứa x mol CO2 và 0,5-x mol CO dư
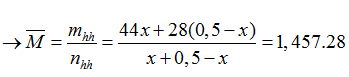
4CO + Fe3O4 
Theo PT: nFe3O4 phản ứng= 1/4. nCO= 0,1 mol → m= mFe3O4 = 0,1.232= 23,2 gam
Bài 17:Cho luồng khí CO đi qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 đốt nóng. Sau khi kết thúc thí nghiệm thu được B gồm 4 chất nặng 4,784 gam. Khí đi ra khỏi ống sứ cho hấp thụ vào dung dịch Ba(OH)2 dư thì thu được 9,062 gam kết tủa. Phần trăm khối lượng Fe2O3 trong hỗn hợp A bằng:
A. 86,96%
B. 76,01%
C. 73,04%
D. 66,01%
Lời giải:
Đáp án A
Đặt số mol FeO là x mol; Số mol Fe2O3 là y mol → x+ y = 0,04 mol (1)
Bản chất phản ứng: CO + Ooxit → CO2
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
Theo PT: nO (oxit)= nCO2= nBaCO3= 9,062/197= 0,046 mol
Khi cho CO qua hỗn hợp A thì khối lượng chất rắn giảm. Lượng giảm chính là lượng O trong oxit tách ra
→ mhỗn hợp A= mB + mO (oxit tách ra)= 4,784+ 0,046.16=5,52 gam
→ 72x+ 160y= 5,52 gam (2)
Giải hệ gồm (1), (2) ta có x= 0,01; y= 0,03
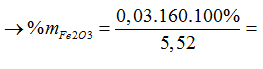
Bài 18:Cho khí CO đi qua ống sứ đựng 37,12 gam Fe3O4 nung nóng thu được hỗn hợp rắn X. Khí đi ra khỏi ống sứ được hấp thụ hết vào dung dịch Ba(OH)2 dư thu được 43,34 gam kết tủa. Hòa tan hết lượng hỗn hợp X trong dung dịch H2SO4 đặc nóng dư thấy bay ra V lít khí SO2 (đktc). Giá trị của V là:
A. 4,48
B. 3,584
C. 3,36
D. 6,72
Lời giải:
Đáp án D
Ta có: nFe3O4 = 0,16 mol; nBaCO3= 0,22 mol
CO + Fe3O4 → Hỗn hợp rắn X có chứa Fe, FeO, Fe3O4 + H2SO4 đặc nóng → SO2
Bản chất phản ứng:
CO + O oxit → CO2
CO2 + Ba(OH)2 → BaCO3 + H2O
nCO= nCO2= nBaCO3= 0,22 mol
-QT cho electron:
Fe3O4 → 3Fe+3+ 1e
C+2 → C+4+ 2e
Tổng số mol e cho là: ne cho= nFe3O4 + 2.nCO= 0,16+ 2.0,22=0,6 mol
-QT nhận electron:
S+6+ 2e → SO2
Theo bảo toàn electron: ne cho= ne nhận= 0,6 mol → nSO2= 0,3 mol → V= 6,72 lít
Bài 19:Hòa tan hoàn toàn 16 gam hỗn hợp X gồm CuSO4, FeSO4 và Fe2(SO4)3 trong đó S chiếm 22,5% về khối lượng) trong nước được dung dịch X. Thêm NaOH dư vào X, lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được chất rắn Y, thổi CO dư đi qua Y thu được hỗn hợp rắn Z. Biết các phản ứng xảy ra hoàn toàn. Khối lượng của Z là:
A. 12,4 gam
B. 8 gam
C. 5,2 gam
D. 7,2 gam
Lời giải:
Đáp án C
mS= 16.22,5%=3,6 gam → nS= 0,1125 mol= nSO4(2-)
→ mCu, Fe trongX= mX- mSO4(2-)= 16- 0,1125.96=5,2 gam
Cu2++ 2OH- → Cu(OH)2
Fe2++ 2OH- → Fe(OH)2
Fe3++ 3OH- → Fe(OH)3
Cu(OH)2
2Fe(OH)2 + 1/2 O2
2Fe(OH)3
CuO + CO
Fe2O3 + 3CO
Sau khi các phản ứng xảy ra hoàn toàn ta có Z chứa Cu và Fe → mZ= 5,2 gam
Bài 20:Hỗn hợp X gồm Al, Fe2O3, Fe3O4 , CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít khí CO (đktc) sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít khí NO (đktc, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m là:
A. 41,13
B. 35,19
C. 38,45
D. 40,03
Lời giải:
Đáp án C
Z gồm CO và CO2
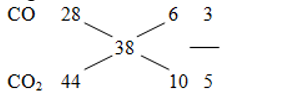
⇒nCO=0,15 mol ; nCO2=0,25 mol
⇒ nO bị chiếm = 0,25 mol
⇒ nO còn lại = 0,2539m/16−0,25 mol
nNO=7,168/22,4=0,32 mol
Coi hỗn hợp Y gồm kim loại: 0,7461m (gam) và O: 0,2539m/16−0,25 (mol)
Ta có:
O0 + 2e → O-2
0,2539m/16−0,25 0,2539m/8−0,5
N+5 + 3e → N+2
0,96 0,32
⇒ m muối = m KL + mNO3-trong muối = 0,7461m + 62. (0,2539m/8−0,5+0,96)
⇒ 3,456m = 2,714m + 28,52
⇔ m = 38,45 gam
Bài 21:Thổi luồng khí CO qua ống đựng m gam Fe2O3. Sau một thời gian thu được m1 gam hỗn hợp Y gồm 4 chất rắn khác nhau. Hòa tan hết chất rắn Y bằng dung dịch HNO3 dư thu được 0,448 lít khí NO là sản phẩm khử duy nhất và dung dịch Z. Cô cạn dung dịch Z thu được (m1+ 16,68) gam muối khan. Giá trị của m, m1 và thể tích khí CO lần lượt:
A. 4,0; 3,76; 0,672 lít
B. 8,0; 7,52; 0,672 lít
C. 8,0; 7,52; 0, 336 lít
D. 4,0; 3,76; 0,336 lít
Lời giải:
Đáp án B
Sơ đồ phản ứng: CO + Fe2O3 → m1 gam Y+ HNO3 dư → Fe(NO3)3 + NO
Ta có: nNO= 0,448/22,4= 0,02 mol
-Quá trình cho e:
C+2 → C+4+ 2e
0,03 ← 0,06
-Quá trình nhận e:
NO3-+5 + 3e + 4H+ → NO + 2H2O
0,06 ← 0,02 mol
Áp dụng định luật bảo toàn e: ne cho= ne nhận= 0,06 mol → nCO= 0,03 mol
→ VCO= 0,672 lít
Ta có: nO (oxit tách ra)= nCO phản ứng= 0,03 mol
→ m1=m – mO (oxit tách ra)= m- 0,03.16= m- 0,48 (gam)
Ta có: nFe(NO3)3 = 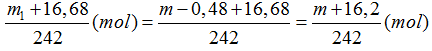
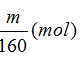
Theo bảo toàn nguyên tố Fe ta có: nFe(NO3)3= 2.nFe2O3
→ 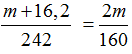
Bài 22:Hỗn hợp rắn X gồm FeO và Fe3O4 có tỉ lệ mol 2:1. Dẫn khí CO đi qua m gam X nung nóng thu được 20 gam hỗn hợp rắn Y. Hòa tan hết Y vào dung dịch H2SO4 đặc nóng dư thu được 5,6 lít khí SO2 (đktc, sản phẩm khử duy nhất). Giá trị của m gần nhất với:
A. 22,5
B. 24,0
C. 20,5
D. 24,5
Lời giải:
Đáp án A
Đặt nFeO= 2x mol; nFe3O4 = x mol
→ nFe= 2x+3x= 5x mol; nO= 2x+ 4x= 6x mol
20 gam hỗn hợp rắn Y có chứa Fe và O
→ mO (trong Y)= mY- mFe= 20-5x.56 gam
→ mO (đã phản ứng)= mO (X)- mO (Y)= 6x.16- (20-5x.56)= 376x-20 (gam)
→ nO (đã phản ứng)= 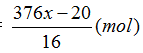
CO+ m gam X → 20 gam Y + H2SO4 đặc nóng dư → Fe2(SO4)3 + SO2
Ta có: nSO2= 5,6/22,4= 0,25 mol
-Quá trình cho e:
C+2 → C+4+ 2e
Fe → Fe3++ 3e
5x → 15x mol
-Quá trình nhận e:
S+6+ 2e → SO2
0,5 ← 0,25 mol
O + 2e → O-2
Bản chất phản ứng khử oxit sắt: CO + O(oxit) → CO2
Áp dụng định luật bảo toàn e: ne cho= ne nhận
→ 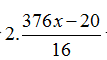
→ m= 72.2x+ 232x=22,56 gam
Bài 23:Dẫn khí than ướt qua m gam hỗn hợp X gồm các chất Fe2O3, CuO, Fe3O4 (có số mol bằng nhau) đun nóng được 36 gam hỗn hợp chất rắn Y. Cho Y phản ứng hết với dung dịch HNO3 loãng dư thu được 11,2 lít khí NO (sản phẩm khử duy nhất, đktc). m có giá trị gần nhất với giá trị nào?
A. 46,5
B. 47,0
C. 47,5
D. 48,0
Lời giải:
Đáp án B
Thành phần chủ yếu của khí than ướt là CO; H2, CO2, N2
Giả sử trong X có các oxit có cùng số mol là x.
Qui hỗn hợp về thành Fe; Cu; O:
⇒ sau khi cho khí than ướt qua thì:
CO + O → CO2.
H2 + O → H2O.
⇒ Y gồm: 5x mol Fe; x mol Cu và y mol O.
Khi phản ứng với HNO3 xảy ra: nNO= 11,2/22,4= 0,5 mol
+Quá trình cho e: Fe → Fe+3 + 3e Cu → Cu+2 + 2e
+ Quá trình nhận e: O + 2e → O-2 N+5 + 3e → N+2
Ta có: Áp dụng định luật bảo toàn electron đối với quá trình Y tác dụng với HNO3
3.5x + 2.x = 2.y + 3.0,5
Mặt khác: mY = 56.5x + 64.x + 16.y = 36
⇒ x = 0,1 mol; y= 0,1 mol
⇒ m = 0,1.160 + 0,1.80 + 0,1.232 = 47,2g.
Bài 24:Dẫn từ từ đến hết V lít khí CO2 (đktc) vào 200 ml dung dịch Ca(OH)2 1,5M thu được 20 gam kết tủa. Giá trị của V là:
A. 4,48 lít hoặc 6,72 lít
B. 4,48 lít hoặc 8,96 lít
C. 2,24 lít hoặc 6,72 lít
D. 2,24 lít hoặc 8,96 lít
Lời giải:
Đáp án B
Ta có: nCa(OH)2= 0,2.1,5= 0,3 mol; nCaCO3= 20/100= 0,2 mol
Ta có : nCa(OH)2 > nCaCO3 nên có 2 trường hợp xảy ra :
-TH1 : Ca(OH)2 dư :
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có: nCO2= nCaCO3= 0,2 mol → V= VCO2= 0,2.22,4= 4,48 lít
-TH2 : Ca(OH)2 phản ứng hết :
CO2 + Ca(OH)2 → CaCO3 + H2O
0,2 0,2 0,2
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,2 ← (0,3-0,2)
Ta có: nCO2= 0,2 + 0,2= 0,4 mol → V= VCO2= 0,4.22,4= 8,96 lít
Bài 25:Dẫn từ từ đến hết 4,48 lít khí CO2 (đktc) vào 100 ml dung dịch chứa NaOH 1M và Ca(OH)2 1M. Tính khối lượng kết tủa tạo thành sau khi các phản ứng xảy ra hoàn toàn.
A. 5 gam
B. 15 gam
C. 20 gam
D. 10 gam
Lời giải:
Đáp án D
nCO2= 0,2 mol; nCa(OH)2= 0,1 mol; nNaOH= 0,1 mol
nOH-= 0,3 mol → 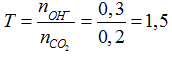
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có x+ y= 0,2; x+ 2y= 0,3 suy ra x= 0,1; y=0,1
Ca2+ + CO32- → CaCO3↓
0,1 0,1 mol 0,1 mol
mCaCO3= 0,1. 100= 10 gam
Bài 26:Dẫn 4,48 lít khí CO2 (đktc) vào 100 ml dung dịch chứa Ba(OH)2 1,2 M và KOH 1,0 M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là:
A. 19,70 gam
B. 29,55 gam
C. 23,64 gam
D. 31,52 gam
Lời giải:
Đáp án C
nCO2= 0,2 mol; nBa(OH)2= 0,12 mol; nKOH= 0,1 mol
nOH-= 0,34 mol → 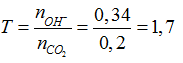
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có x+ y= 0,2; x+ 2y= 0,34 suy ra x= 0,06; y=0,14
Ba2+ + CO32- → BaCO3↓
0,12 0,14 mol 0,12 mol
mBaCO3= 0,12. 197= 23,64 (gam)
Bài 27:Hấp thụ hoàn toàn 3,36 lít (đktc) khí CO2 vào 100 ml dung dịch X chứa NaOH 1M và Ca(OH)2 0,5M. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y. Khối lượng dung dịch Y thay đổi như thế nào so với dung dịch X?
A. tăng 1,6 gam
B. giảm 1,6 gam
C. tăng 5,0 gam
D. giảm 5,0 gam
Lời giải:
Đáp án A
nCO2= 0,15 mol; nCa(OH)2= 0,05 mol; nNaOH= 0,1 mol
nOH-= 0,05.2+ 0,1= 0,2 mol → 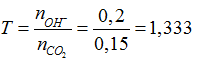
→ Tạo 2 loại muối : HCO3- và CO32-
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có x+ y= 0,15; x+ 2y= 0,2 suy ra x= 0,1; y=0,05
Ca2+ + CO32- → CaCO3↓
0,05 0,05 mol 0,05 mol
mCaCO3= 0,05. 100= 5 gam
mCO2= 0,15.44= 6,6 gam
Do mCO2> mCaCO3 nên khối lượng dung dịch tăng một lượng là:
∆mtăng= mCO2- mCaCO3= 6,6-5= 1,6 gam

Bài 28:Hấp thụ hoàn toàn 7,84 lít (đktc) khí CO2 vào 200 ml dung dịch X chứa KOH 0,75M và Ba(OH)2 0,75M. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y. Khối lượng dung dịch Y thay đổi như thế nào so với dung dịch X?
A. tăng 19,7 gam
B. giảm 19,7 gam
C. tăng 4,3 gam
D. giảm 4,3 gam
Lời giải:
Đáp án D
nCO2= 0,35 mol; nBa(OH)2= 0,15 mol; nKOH= 0,15 mol
nOH-= 0,45 mol → 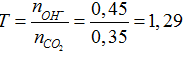
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có nCO2= x+ y= 0,35;
nOH-= x+ 2y= 0,45 suy ra x= 0,25; y=0,1
Ba2+ + CO32- → BaCO3↓
0,15 0,1 mol 0,1 mol
mBaCO3= 0,1. 197= 19,7 (gam)
mCO2= 0,35.44=15,4 gam
Do mCO2< mBaCO3 nên khối lượng dung dịch giảm một lượng là:
∆mgiảm= mBaCO3- mCO2= 19,7- 15,4= 4,3 gam
Bài 29:Hấp thụ hoàn toàn 2,688 lít khí CO2 (ở đktc) vào 2,5 lít dung dịch Ba(OH)2 nồng độ a mol/l thu được 15,76 gam kết tủa. Giá trị của a là:
A. 0,032
B. 0,048
C. 0,06
D. 0,04
Lời giải:
Đáp án D
Ta có: nCO2= 0,12 mol; nBa(OH)2= 2,5 a mol ; nBaCO3= 0,08 mol
Ta có nCO2 > nBaCO3 nên xảy ra các PTHH sau :
CO2 + Ba(OH)2 → BaCO3↓+ H2O (1)
0,08 0,08 ← 0,08 mol
2CO2 + Ba(OH)2 → Ba(HCO3)2
(0,12-0,08) → 0,02 mol
Tổng số mol Ba(OH)2 là nBa(OH)2= 0,08 + 0,02= 0,1 mol= 2,5a
→ a=0,04M
Bài 30:Khi cho 0,02 mol hoặc 0,04 mol CO2 hấp thụ hết vào dung dịch Ba(OH)2 thì lượng kết tủa thu được đều bằng nhau. Số mol Ba(OH)2 có trong dung dịch là:
A. 0,01
B. 0,02
C. 0,03
D. 0,04
Lời giải:
Đáp án C
Do cho 0,02 mol hoặc 0,04 mol CO2 hấp thụ hết vào dung dịch Ba(OH)2 thì lượng kết tủa thu được đều bằng nhau nên chứng tỏ khi nCO2= 0,02 mol thì kết tủa chưa bị hòa tan, còn khi nCO2= 0,04 mol thì kết tủa bị hòa tan một phần
-Khi nCO2= 0,02 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
Ta có: nCO2= nBaCO3= 0,02 mol
-Khi nCO2= 0,04 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
0,02 0,02 0,02
2CO2 + Ba(OH)2 → Ba(HCO3)2
(0,04-0,02) → 0,01
Ta có: nBa(OH)2= 0,02+ 0,01= 0,03 mol
Bài 31:Sục V lít khí CO2 (đktc) vào 1 lít dung dịch Ba(OH)2 0,12M. Khi V biến thiên từ 2,24 lít đến 4,48 lít thì khối lượng kết tủa cũng biến đổi theo, trong đó lượng kết tủa thu được ít nhất là:
A. 19,7
B. 7,88
C. 15,26
D. 9,85
Lời giải:
Đáp án B
Ta có: nBa(OH)2= 0,12 mol; nCO2= 0,1 mol ; nCO2= 0,2 mol
-Tại điểm cực đại:
CO2 + Ba(OH)2 → BaCO3 + H2O
0,12 0,12 0,12
Vậy khi nCO2= 0,12 mol thì lượng kết tủa đạt cực đại
Vậy khi đi từ nCO2 = 0,1 mol đến 0,12 mol thì lượng kết tủa sẽ dần tăng lên. Khi đi từ nCO2= 0,12mol đến 0,2 mol thì lượng kết tủa sẽ dần giảm xuống
→ Lượng kết tủa nhỏ nhất khi nCO2= 0,1 mol hoặc 0,2 mol.
-Khi nCO2= 0,1 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
0,10 0,10 0,10 mol
Ta có: nBaCO3= 0,1 mol
-Khi nCO2= 0,2 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
x x x mol
2CO2 + Ba(OH)2 → Ba(HCO3)2
2y y mol
Ta có: nBa(OH)2= x + y= 0,12 mol ; nCO2= x+ 2y= 0,2 mol
→ x= 0,04 mol ; y = 0,08 mol
Ta có: nBaCO3= 0,04 mol
So sánh 2 trường hợp trên ta thấy nBaCO3 min= 0,04 mol → mBaCO3 min= 7,88 gam
Bài 32:Cho 17,15 gam hỗn hợp X gồm Ba và Na vào nước thu được dung dịch Y và 3,92 lít khí H2 (đktc). Cho khí CO2 vào dung dịch Y. Cho V lít khí CO2 (đktc) vào dung dịch Y thấy lượng kết tủa thu được là lớn nhất. Giá trị của V là:
A. 2,24 ≤V≤ 5,6
B. 2,24 ≤V≤ 4,48
C. 3,92 ≤V≤ 5,6
D. 2,24 ≤V≤ 3,92 hoặc V= 5,6
Lời giải:
Đáp án A
Ba+ 2H2O → Ba(OH)2 + H2
Na + H2O → NaOH + ½ H2
Đặt nBa= x mol; nNa= y mol → mhỗn hợp= 137x + 23y= 17,15 gam
nH2= x+ ½ y=3,92/22,4=0,175 mol ; nOH-= 2.nH2= 0,35 mol
Giải hệ trên ta có: x= 0,1 mol ; y=0,15 mol
Để giải bài này ta nên sử dụng phương trình phân tử :
Sục khí CO2 vào dung dịch Y chứa NaOH, Ba(OH)2 thì xảy ra các PTHH sau:
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O (1)
CO2 + 2NaOH → Na2CO3 + H2O (2)
CO2 + Na2CO3 + H2O → 2NaHCO3 (3)
CO2 + BaCO3 + H2O → Ba(HCO3)2 (4)
Để lượng kết tủa thu được lớn nhất thì BaCO3 không bị hòa tan
→ Lượng CO2 nhỏ nhất khi xảy ra phản ứng (1), còn lượng CO2 lớn nhất khi xảy ra phản ứng (1), (2), (3)
-KHi xảy ra phản ứng (1): nCO2= nBa(OH)2= x= 0,1 mol
-Khi xảy ra cả phản ứng (1,2,3): nCO2= nBa(OH)2 + 1/2nNaOH + nNa2CO3 =0,1+0,5 .0,15+ 0,5.0,15= 0,25 mol
→ 0,1 ≤ nCO2 ≤ 0,25 mol → 2,24 ≤ VCO2 ≤ 5,6
Bài 33:Hấp thụ hoàn toàn 0,16 mol CO2 vào 2 lít dung dịch Ca(OH)2 0,05M được kết tủa X và dung dịch Y. Khối lượng dung dịch Y thay đổi như thế nào so với ban đầu?
A. tăng 3,04 gam
B. giảm 3,04 gam
C. tăng 7,04 gam
D. giảm 7,04 gam
Lời giải:
Đáp án A
Ta có nCa(OH)2= 2.0,05= 0,1 mol
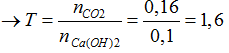
CO2 + Ca(OH)2 → CaCO3 + H2O
x x x mol
2CO2 + Ca(OH)2 → Ca(HCO3)2
2y y mol
Ta có: nCa(OH)2= x + y= 0,1 mol ; nCO2= x+ 2y= 0,16 mol → x= 0,04 mol ; y = 0,06 mol
Ta có: nCaCO3= 0,04.100= 4 gam ; mCO2= 0,16. 44= 7,04 gam
→ Khối lượng dung dịch Y tăng một lượng là :
∆mtăng= mCO2- mCaCO3= 7,04- 4= 3,04 gam
Bài 34:Hòa tan một mẫu hợp kim K-Ba có số mol bằng nhau vào nước được dung dịch X và 6,72 lít khí (đktc). Sục 0,025 mol khí CO2 vào dung dịch X thu được m gam kết tủa. Giá trị của m là:
A. 2,955
B. 4,334
C. 3,940
D. 4,925
Lời giải:
Đáp án D
Ba+ 2H2O → Ba(OH)2 + H2
K + H2O → KOH + ½ H2
Đặt nBa= x mol; nK= x mol
nH2= x+ ½ x=6,72/22,4=0,3 mol → x= 0,2 mol ; nOH-= 2.nH2= 0,6 mol
ta thấy :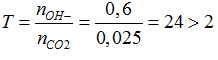
CO2 + 2OH- → CO32-+ H2O
0,025 0,6 0,025 mol
Ba2+ + CO32- → BaCO3↓
0,2 0,025 mol 0,025 mol
mBaCO3= 0,025. 197= 4,925 (gam)
Bài 35:Dẫn một lượng khí CO2 thu được khi đốt cháy một hợp chất hữu cơ vào bình đựng nước vôi trong dư thu được 5 gam kết tủa. Lọc bỏ kết tủa và đun nóng nước lọc thu được thì tạo được thêm 2,5 gam kết tủa nữa. Tính thể tích khí CO2 ban đầu (đktc)?
A. 1,68 lít
B. 2,24 lít
C. 1,12 lít
D. 1,792 lít
Lời giải:
Đáp án B
Ta có: nCaCO3 lần 1= 5/100= 0,05 mol; nCaCO3 lần 2 = 2,5/100= 0,025 mol
Do khi lọc kết tủa rồi đem đun nóng nước lọc thấy xuất hiện kết tủa nên CO2 phản ứng với nước vôi trong theo 2 PTHH sau:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,05 ← 0,05 mol
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 ← 0,025 mol
Ca(HCO3)2
0,025 → 0,025 mol
→ Tổng số mol CO2 ban đầu là nCO2= 0,05= 0,05= 0,1 mol → VCO2= 2,24 lít
Bài 36:Hỗn hợp X gồm CO và NO có tỉ khối so với hiđro bằng 14,5. V lít hỗn hợp X tác dụng vừa đủ với 1,6 gam oxi thu được hỗn hợp mới Y. Cho Y sục vào 200 ml dung dịch NaOH 2M ta được 200 ml dung dịch mới. Số lượng chất tan có trong dung dịch mới là:
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án D
Ta có nO2= 0,05 mol; nNaOH= 0,2. 2= 0,4 mol
Đặt nCO= x mol; nNO= y mol
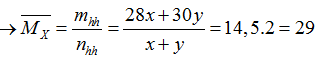
2CO + O2 → 2CO2
2NO+ O2 → 2 NO2
Theo 2 PTHH trên ta có: nO2= 0,5. (nCO + nNO)= 0,5 (x+y)= 0,05 mol (2)
Từ (1) và (2) ta có x= y = 0,05 mol
→ Hỗn hợp khí Y có 0,05 mol CO2 và 0,05 mol NO2
Cho Y vào dung dịch NaOH ta có:
CO2 + 2NaOH → Na2CO3 + H2O
0,05 → 0,1
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
0,05 0,05
Tổng số mol NaOH phản ứng là 0,1+ 0,05= 0,15 mol → nNaOH dư= 0,25 mol
Vậy trong dung dịch mới có chứa Na2CO3, NaNO2, NaNO3, NaOH (4 chất tan)
Bài 37:Hỗn hợp khí X (NO2, CO2) có tỉ khối hơi so với H2 bằng 22,5. Hấp thụ hết 4,48 lít khí X vào 200 ml dung dịch NaOH 1,225M, sau phản ứng hoàn toàn khối lượng muối trong dung dịch là:
A. 17,09
B. 14,065
C. 18,8
D. 15,2
Lời giải:
Đáp án A
Đặt nCO2= x mol; nNO2= y mol
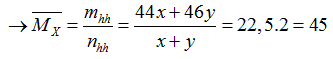
Mà nX= x+ y= 0,2 mol → x=y= 0,1 mol
Ta có : nNaOH= 0,2.1,225= 0,245 mol
Cho X vào dung dịch NaOH ta có:
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
0,1 0,1 0,05 0,05 mol
Số mol NaOH còn dư là 0,245- 0,1= 0,145 mol
Ta có: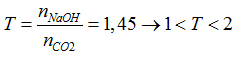
CO2 + NaOH → NaHCO3
a a a mol
CO2 + 2NaOH → Na2CO3 + H2O
b 2b b mol
Có nCO2= a+ b= 0,1;
nOH-= a+ 2b= 0,145 suy ra a= 0,055 mol; b= 0,045 mol
Vậy trong dung dịch có 0,05 mol NaNO2; 0,05 mol NaNO3; 0,055 mol NaHCO3 và 0,045 mol Na2CO3 → mmuối= 17,09 gam
Bài 38:Trộn 50 gam dung dịch KOH 11,2% với 150 gam dung dịch Ba(OH)2 22,8% được dung dịch A. Dẫn 7,84 lít khí CO2 (đktc) vào dung dịch A, sau khi phản ứng hoàn toàn thu được dung dịch B. Khối lượng của dung dịch B so với dung dịch A?
A. giảm 24 gam
B. giảm 29,55 gam
C. giảm 14,15 gam
D. tăng 15,4 gam
Lời giải:
Đáp án C
Ta có:
nOH-= 0,1+ 2.0,2= 0,5 mol → 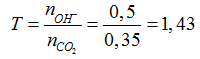
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có nCO2= x+ y= 0,35;
nOH-= x+ 2y= 0, 5 suy ra x=0,2; y= 0,15 mol
Ba2+ + CO32- → BaCO3↓
0,2 0,15 mol 0,15 mol
mBaCO3= 0,15. 197= 29,55 (gam)
mCO2= 0,35.44=15,4 gam
Do mCO2< mBaCO3 nên khối lượng dung dịch giảm một lượng là:
∆mgiảm= mBaCO3- mCO2= 29,55- 15,4= 14,15 gam
Bài 39:Hấp thụ hết V lít khí CO2 vào 400 ml dung dịch Ba(OH)2 0,6M thu được a gam kết tủa và dung dịch X. Dẫn 0,7V lít khí CO2 vào dung dịch X thu được thêm 0,3a gam kết tủa nữa. Thể tích các khí đều đo ở đktc. Giá trị của V là:
A. 3,136
B. 3,36
C. 3,584
D. 3,84
Lời giải:
Đáp án C
Ta có: nBa(OH)2= 0,4. 0,6= 0,24 mol
Khi sục thêm 0,7V lít khí CO2 vào dung dịch X thu thêm 0,3a gam kết tủa nên chứng tỏ trong dung dịch X chứa Ba(OH)2 dư
- Hấp thụ V lít CO2 vào dung dịch Ba(OH)2 thu được a gam kết tủa:
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
a/100 a /100 ← a/100 mol
Ta có: nCO2= nBaCO3 → V/22,4= a/100 (1)
-Hấp thụ 1,7V lít CO2 vào dung dịch Ba(OH)2 thu được tổng cộng a+0,3a= 1,3 a gam kết tủa.
*TH1: Kết tủa chưa bị hòa tan:
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
1,3a/100 1,3 a /100 ← 1,3a/100 mol
Ta có: nCO2= nBaCO3 → 1,7V/22,4= 1,3a/100 (2)
Từ (1) và (2) ta có V=0 ; a= 0 nên trường hợp này loại
*TH2 : Kết tủa bị hòa tan một phần
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
1,3a/100 1,3a/100 1,3a/100 mol
2CO2 + Ba(OH)2 → Ba(HCO3)2
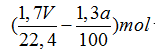
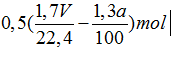
Ta có nBa(OH)2=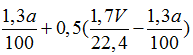
Giải hệ (1) và (3) ta có a=16 ; V= 3,584 lít

Bài 40:Hỗn hợp X gồm Na và Ba trong đó Na chiếm 14,375% về khối lượng. Hòa tan hoàn toàn m gam X vào nước thu được 1,344 lít khí H2 (đktc) và dung dịch Y. Hấp thụ hoàn toàn 2,016 lít khí CO2 (đktc) vào dung dịch Y. Các phản ứng xảy ra hoàn toàn. Khối lượng kết tủa thu được là:
A. 7,88 gam
B. 2,14 gam
C. 5,91 gam
D. 3,94 gam
Lời giải:
Đáp án C
Ba+ 2H2O → Ba(OH)2 + H2
Na + H2O → NaOH + ½ H2
Đặt nBa= x mol; nNa= y mol → mhỗn hợp= 137x + 23y
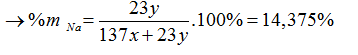
nH2= x+ ½ y=1,344/22,4=0,06mol ; nOH-= 2.nH2= 0,12 mol; nCO2=0,09 mol
Giải hệ trên ta có: x= 0,04 mol; y= 0,04 mol
ta thấy :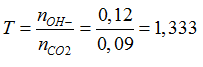
CO2 + OH- → HCO3-
a a a mol
CO2 + 2OH- → CO32- + H2O
b 2b b mol
Có nCO2= a+ b= 0,09 mol;
nOH-= a+ 2b= 0,12 suy ra a=0,06 mol; b= 0,03 mol
Ba2+ + CO32- → BaCO3↓
0,04 0,03 mol 0,03 mol
mBaCO3= 0,03. 197= 5,91(gam)
Bài 41:Hấp thụ hết V lít khí CO2 (đktc) bởi dung dịch có chứa 0,08 mol Ca(OH)2 ta thu được 2 gam kết tủa, lọc kết tủa, thu lấy phần nước lọc, khối lượng của phần nước lọc tăng so với khối lượng dung dịch Ca(OH)2 ban đầu 4,16 gam. Giá trị của V là:
A. 3,136
B. 4,480
C. 3,360
D. 0,448
Lời giải:
Đáp án A
Ta có: nCaCO3= 2/100= 0,02 mol
mdung dịch tăng= mCO2- mCaCO3 → mCO2= 4,16 + 2= 6,16 gam → nCO2= 0,14 mol → VCO2= 0,14.22,4= 3,136 lít
Bài 42:Sục V lít khí CO2 (đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1M và NaOH 1M. Sau phản ứng thu được 19,7 gam kết tủa. Giá trị của V là:
A. 2,24 hoặc 11,2
B. 5,6 hoặc 1,2
C. 2,24 hoặc 4,48
D. 6,72 hoặc 4,48
Lời giải:
Đáp án A
nBa(OH)2 0,2 mol; nNaOH= 0,2 mol
nOH-= 0,6 mol; nBaCO3=19,7/197= 0,1 mol
Ta có 2 trường hợp:
-TH1: CO2 tác dụng với OH- chỉ tạo CO32-
CO2 + 2OH- → CO32- + H2O
0,1 0,2 ← 0,1 mol
Ba2+ + CO32- → BaCO3↓
0,2 0,1 ← 0,1 mol
→ VCO2= 2,24 lít
-TH2: CO2 tác dụng với OH- tạo CO32- và HCO3-
CO2 + OH- → HCO3-
0,4 ← (0,6-0,2) mol
CO2 + 2OH- → CO32- + H2O
0,1 0,2 ← 0,1
Ba2+ + CO32- → BaCO3↓
0,2 0,1 ← 0,1 mol
Ta có: nCO2= 0,1+ 0,4= 0,5 mol → VCO2= 11,2 lít
Bài 43:Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại 24,2%. Thêm vào X một lượng bột MgCO3, khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ dung dịch HCl bằng 21,10%. Nồng độ % của dung dịch CaCl2 và MgCl2 lần lượt là:
A. 11,35% và 3,54%
B. 11,35% và 4,54%
C. 10,35% và 3,04%
D. 10,35% và 3,54%
Lời giải:
Đáp án D
Giả sử có 100 gam dung dịch HCl 32,85% thì khối lượng HCl là 32,85 gam.
nHCl=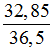
- Gọi số mol của CaCO3 là x (mol). Phản ứng:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 (1)
x 2x x x
Từ (1) và đề ra: nHCldư = (0,90 - 2x) mol
Khối lượng dung dịch X sau phản ứng (1): 100 + 100x – 44x = (100 + 56x) gam
Theo đề ra: C%HCl =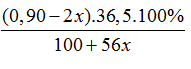
Vậy sau p/ư (1) nHCl còn lại = 0,7mol
- Cho MgCO3 vào dung dịch X, có p/ư: MgCO3 + 2HCl → MgCl2 + H2O + CO2 (2)
y 2y y y
Sau p/ư (2) nHCl dư = 0,7-2y
Khối lượng dung dịch Y là: (105,6 + 84y - 44y) gam hay (105,6 + 40y) gam
Từ (2) và đề ra: C%HCl trong Y=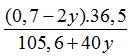
Dung dịch Y chứa 2 muối CaCl2, MgCl2 và HCl dư:
C%(CaCl2) = 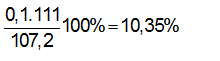
C%(MgCl2) = 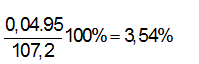
Bài 44:Cho m gam NaOH vào 2 lít dung dịch NaHCO3 nồng độ a mol/l thu được 2 lít dung dịch X. Lấy 1 lít dung dịch X tác dụng với dung dịch BaCl2 dư thu được 11,82 gam kết tủa. Mặt khác, cho 1 lít dung dịch X vào dung dịch CaCl2 dư rồi đun nóng, sau khi kết thúc các phản ứng thu được 7,0 gam kết tủa. Giá trị của a, m tương ứng là:
A. 0,08 và 4,8
B. 0,04 và 4,8
C. 0,14 và 2,4
D. 0,07 và 3,2
Lời giải:
Đáp án
Ta có: nBaCO3= 11,82/197= 0,06 mol; nCaCO3= 7/100= 0,07 mol
NaOH + NaHCO3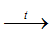
0,06 0,06 mol
BaCl2 + Na2CO3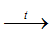
0,06 0,06 mol
m = 0,06.2.40 = 4,8g
2NaHCO3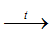
CaCl2 + Na2CO3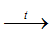
0,07 0,07 mol
nNa2CO3 (4) = nNa2CO3 (1) + nNa2CO3 (3)
→ nNa2CO3 (3) = 0,07 – 0,06 = 0,01 mol
nNaHCO3 trong một lít dd = nNaHCO3 (1) + nNaHCO3 (3) = 0,06 + 0,01.2 = 0,08 mol
a = 0,08/1 = 0,08 mol/l

Bài 45:Cho 9,125 gam muối hiđrocacbonat hóa trị II phản ứng hết với dung dịch H2SO4 dư thu được dung dịch chứa 7,5 gam muối sunfat trung hòa. Công thức của muối hiđrocacbonat là:
A. Zn(HCO3)2
B. Mg(HCO3)2
C. Ba(HCO3)2
D. Ca(HCO3)2
Lời giải:
Đáp án B
Đặt công thức muối hiđrocacbonat là R(HCO3)2
R(HCO3)2 +H2SO4 → RSO4 + 2CO2 + 2H2O
Theo PT ta thấy: nR(HCO3)2= nRSO4
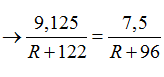
Bài 46:Cho 1,9 gam hỗn hợp muối cacbonat và hi đrocacbonat của kim loại kiềm M tác dụng hết với dung dịch HCl dư sinh ra 0,448 lít khí (ở đktc). Kim loại M là:
A. Na
B. Li
C. K
D. Rb
Lời giải:
Đáp án A
Đặt công thức muối cacbonat là M2CO3 có số mol x , muối hiđrocacbonat là MHCO3 có số mol y mol
M2CO3 + 2HCl → 2MCl + CO2 + H2O
x x mol
MHCO3 + HCl → MCl + CO2 + H2O
y y mol
Ta có
nCO2= x+y= 0,448/22,4= 0,02 mol= nhỗn hợp 2 muối
→ 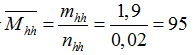
→ M+61 < 95 < 2M + 60 → 17,5 < M<34 → Chỉ có Na thỏa mãn
Bài 47:Hòa tan hoàn toàn muối MCO3 bằng lượng vừa đủ dung dịch H2SO4 12,25% thu được dung dịch MSO4 14,29%. Kim loại M là:
A. Mg
B. Fe
C. Zn
D. Ca
Lời giải:
Đáp án A
Giả sử nMCO3= 1 mol → nH2SO4= nMSO4= nCO2= 1mol
→ mH2SO4= 98 gam; mMSO4= M+96 gam; mCO2= 44 gam; mdd H2SO4 12,25%=800 g
MCO3 + H2SO4 → MSO4 + CO2↑ + H2O
Ta có: mdd sau pứ= mMCO3 + mdd H2SO4- mCO2= M+60+800-44= M+816 (gam)
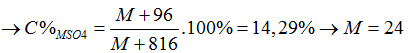
Bài 48:Trong một cái cốc đựng muối cacbonat của kim loại hóa trị I. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hóa trị I là:
A. Li
B. Na
C. K
D. Ag
Lời giải:
Đáp án B
Đặt công thức muối cacbonat kim loại là M2CO3
M2CO3 + H2SO4 → M2SO4 + CO2 + H2O
Giả sử nM2CO3= 1 mol → nH2SO4= nM2SO4= nCO2= 1mol
→ mH2SO4= 98 gam; mM2SO4= 2M+96 gam; mCO2= 44 gam; mdd H2SO4 10%=980 g
Ta có: mdd sau pứ= mM2CO3 + mdd H2SO4- mCO2=2M + 60+980-44= 2M+996 (gam)
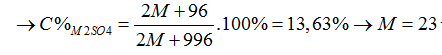
Bài 49:Hai cốc đựng dung dịch HCl đặt trên hai đĩa cân X, Y cân ở trạng thái cân bằng. Cho 5 gam CaCO3 vào cốc X và 4,784 gam M2CO3 (M là kim loại kiềm) vào cốc Y. Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí thăng bằng. Kim loại M là:
A. K
B. Cs
C. Li
D. Na
Lời giải:
Đáp án D
HCl+CaCO3 → CaCl2 +H2O+CO2(1)
0,05 0,05 mol
HCl+M2CO3 → MCl2 +H2O+CO2(2)
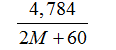
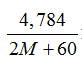
Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí cân bằng nên ta có
mCaCO3−mCO2PT1=mM2CO3−mCO2PT2
→ 5- 0,05.44= 4,784-44. 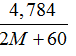
⇒ M = 23 vậy M là Na
Bài 50:Cho 33,8 gam hỗn hợp gồm một muối cacbonat axit và một muối cacbonat trung hòa của cùng một kim loại kiềm X phản ứng với dung dịch HCl dư thu được 6,72 lít khí CO2 (đktc). Xác định X?
A. Li
B. Na
C. K
D. Rb
Lời giải:
Đáp án C
Đặt công thức muối cacbonat là M2CO3 có số mol x , muối hiđrocacbonat là MHCO3 có số mol y mol
M2CO3 + 2HCl → 2MCl + CO2 + H2O
x x mol
MHCO3 + HCl → MCl + CO2 + H2O
y y mol
Ta có
nCO2= x+y= 6,72/22,4= 0,3 mol= nhỗn hợp 2 muối
→ 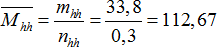
→ M+61< 112,67< 2M + 60 → 26,33< M< 51,67 → Chỉ có K thỏa mãn
Bài 51:Thêm từ từ dung dịch chứa 0,06 mol HCl vào dung dịch chứa 0,05 mol Na2CO3. Thể tích khí CO2 (đktc) thu được là:
A. 0,224 lít
B. 0,56 lít
C. 0,672 lít
D. 2,24 lít
Lời giải:
Đáp án A
Thứ tự phản ứng :
Na2CO3 + HCl → NaCl+ NaHCO3
0,05 → 0,05 0,05 mol
NaHCO3 + HCl → NaCl+ CO2 + H2O
0,05 (0,06-0,05) → 0,01 mol
→ VCO2= 0,01.22,4= 0,224 lít
Bài 52:Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ từng giọt cho đến hết 200 ml dung dịch HCl 1M vào 100 ml dung dịch X. Giá trị của V là:
A. 2,24
B. 4,48
C. 3,36
D. 1,12
Lời giải:
Đáp án D
Ta có : nHCl= 0,2 mol ; nNa2CO3= 0,15 mol ; nKHCO3= 0,1 mol
Cho từ từ HCl vào dung dịch X ta có:
CO32-+ H+ → HCO3-
0,15 0,15 0,15 mol
HCO3- + H+ → CO2 + H2O
(0,15+0,1) (0,2-0,15) → 0,05 mol
→ VCO2=1,12 lít
Bài 53:Dung dịch X chứa 0,6 mol NaHCO3 và 0,3 mol Na2CO3. Thêm rất từ từ dung dịch chứa 0,8 mol HCl vào dung dịch X thu được dung dịch Y và V lít khí CO2 (đktc). Thêm nước vôi trong vào dung dịch Y thấy tạo thành m gam kết tủa. Giá trị của V và m lần lượt là:
A. 11,2 và 40
B. 16,8 và 60
C. 11,2 và 60
D. 11,2 và 90
Lời giải:
Đáp án A
Thêm rất từ từ HCl vào dung dịch X:
CO32-+ H+ → HCO3- (1)
0,3 0,3 0,3 mol
Sau phản ứng (1): nHCO3-= 0,3+ 0,6= 0,9 mol; nH+ còn lại= 0,8- 0,3= 0,5 mol
HCO3- + H+ → CO2 + H2O
0,9 0,5 → 0,5 mol
→ V=VCO2= 0,5.22,4= 11,2 lít
Dung dịch Y chứa HCO3-: 0,9- 0,5= 0,4 mol
HCO3-+ OH- → CO32-+ H2O
0,4 0,4 mol
Ca2+ + CO32- → CaCO3
0,4 0,4 mol
→ mCaCO3= 0,4.100= 40 gam
Bài 54: Trộn 100 ml dung dịch chứa KHCO3 1M và K2CO3 1M với 100 ml dung dịch chứa NaHCO3 1M và Na2CO3 1M được 200 ml dung dịch X. Nhỏ từ từ 100 ml dung dịch Y chứa H¬2SO4 1M và HCl 1M vào dung dịch X được V lít khí CO2 (đktc). Giá trị của V là:
A. 5,6
B. 1,12
C. 2,24
D. 4,48
Lời giải:
Đáp án C
Ta có : nKHCO3= 0,1 mol ; nK2CO3= 0,1 mol ; nNaHCO3= 0,1mol; nNa2CO3= 0,1 mol
Dung dịch X có: nCO3(2-)= 0,2 mol; nHCO3-= 0,2 mol
nH2SO4= 0,1 mol; nHCl= 0,1 mol → nH+= 0,1.2+0,1= 0,3 mol; nSO4(2-) = 0,1 mol
Nhỏ từ từ dung dịch Y vào dung dịch X ta có:
CO32-+ H+ → HCO3- (1)
0,2 0,2 0,2 mol
Sau phản ứng (1) ta thấy: nHCO3-= 0,2+ 0,2= 0,4 mol; nH+= 0,3- 0,2= 0,1 mol
HCO3- + H+ → CO2 + H2O
0,4 0,1 → 0,1 mol
→ V= VCO2= 0,1.22,4= 2,24 lít
Bài 55:Nung m gam hỗn hợp X gồm hai muối cacbonat trung tính của 2 kim loại A và B đều có hóa trị 2. Sau một thời gian thu được 3,36 lít CO2 đktc và còn lại hỗn hợp rắn Y. Cho Y tác dụng hết với dung dịch HCl dư rồi cho khí thoát ra hấp thụ hết bởi dung dịch Ca(OH)2 dư thu được 15 gam kết tủa, phần dung dịch đem cô cạn thu được 32,5 gam hỗn hợp muối khan. Giá trị của m là:
A. 30,8 gam
B. 29,2 gam
C. 29,8 gam
D. 30,2 gam
Lời giải:
Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3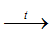
nCO2 = 3,36 /22,4 = 0,15 mol → nMCO3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
nCaCO3 = 15/100 = 0,15 mol → nMCO3 dư = 0,15 mol
nMCO3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có nMCO3 = nMCl2 = 0,3 (mol)
Bảo toàn khối lượng có: mMCO3 = mMCl2 - 0,3.(71- 60) = 29,2 (gam)
Bài 56:Cho hỗn hợp K2CO3 và NaHCO3 (tỉ lệ mol 1:1) vào bình đựng dung dịch Ba(HCO3)2 thu được kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 0,5M vào bình đến khi không còn khí thoát ra thì hết 560 ml. Biết toàn bộ Y phản ứng vừa đủ với 200 ml dung dịch NaOH 1M. Khối lượng kết tủa X là:
A. 3,94 gam
B. 7,88 gam
C. 11,28 gam
D. 9,85 gam
Lời giải:
Đáp án B
Đặt nK2CO3= nNaHCO3= a mol; nBa(HCO3)2= b mol
Ta có phản ứng:
Ba2++ CO32- → BaCO3↓(∗)
b a mol
Khi cho HCl vào bình đến hết thoát khí, HCl sẽ phản ứng với BaCO3, NaHCO3, Ba(HCO3)2, K2CO3 có trong bình.
Ta có: 2H+ + CO32- → H2O + CO2
H+ + HCO3- → H2O + CO2
Ta có: ∑nCO3(2-)=a mol
∑nHCO3-=a+2b mol
nHCl = nH+ = 0,56 × 0,5 = 0,28 mol ⇒ 2a + a + 2b = 0,28 (1)
Khi cho dung dịch Y tác dụng vừa đủ dung dịch NaOH, chỉ có HCO3- phản ứng.
HCO3- + OH- → H2O + CO32-
⇒nHCO3−=nOH− ⇔ a + 2b = 0,2 (2)
Từ (1), (2) ⇒ a = 0,04; b = 0,08
Thế a, b vào phương trình (*)
⇒mBaCO3=197×a=197×0,04=7,88 g

Bài 57:Cho từ từ 450 ml dung dịch HCl 1M vào 500 ml dung dịch X gồm Na2CO3 và NaHCO3 thì thu được 5,6 lít khí (đktc) và dung dịch Y. Cho dung dịch Y tác dụng với dung dịch Ba(OH)2 dư thì thu được 19,7 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch X lần lượt là:
A. 0,2M và 0,15M
B. 0,2M và 0,5M
C. 0,3M và 0,4M
D. 0,4M và 0,3M
Lời giải:
Đáp án D
Ta có: nHCl= 0,45 mol; nCO2= 5,6/22,4= 0,25 mol. Giả sử ban đầu có x mol NaHCO3
CO32- + H+ → HCO3- (1)
HCO3-+ H+ → CO2 + H2O (2)
0,25 0,25 ← 0,25
Theo PT (2): nHCO3-= nH+= nCO2= 0,25 mol
→ nH+ PT1= 0,45- 0,25= 0,2 mol → nCO3(2-) PT1= nH+= nHCO3- PT1= 0,2 mol
→ nNa2CO3= nCO3(2-) PT1= 0,2 mol → CM Na2CO3= 0,2/ 0,5= 0,4M
Dung dịch Y chứa Na+, HCO3- dư: x+0,2- 0,25= x- 0,05 mol
HCO3-+ OH- → CO32-+ H2O
Ba2++ CO32- → BaCO3
Ta thấy: nHCO3-= nCO3(2-)= nBaCO3= 19,7/197= 0,1 mol → x- 0,05= 0,1 → x= 0,15 mol → CM NaHCO3= 0,15/ 0,5= 0,3M
Bài 58:Cho từ từ 150 ml dung dịch HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1,008 lít khí (điều kiện chuẩn) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là:
A. 0,18M và 0,26M
B. 0,21M và 0,18M
C. 0,21M và 0,32M
D. 0,2M và 0,4M
Lời giải:
Đáp án B
Ta có: nHCl= 0,15 mol; nCO2= 1,008/22,4= 0,045 mol. Giả sử ban đầu có x mol NaHCO3
CO32- + H+ → HCO3- (1)
HCO3-+ H+ → CO2 + H2O (2)
0,045 0,045 ← 0,045
Theo PT (2): nHCO3-= nH+= nCO2= 0,045 mol
→ nH+ PT1= 0,15- 0,045= 0,105 mol → nCO3(2-) PT1= nH+= nHCO3- PT1= 0,105 mol
→ nNa2CO3= nCO3(2-) PT1= 0,105 mol → CM Na2CO3= 0,105/ 0,5= 0,21M
Dung dịch Y chứa Na+, HCO3- dư: x+0,105- 0,045= x+0,06 mol
HCO3-+ OH- → CO32-+ H2O
Ba2++ CO32- → BaCO3
Ta thấy: nHCO3-= nCO3(2-)= nBaCO3= 29,55/197= 0,15 mol → x+0,06= 0,15
→ x= 0,09 mol → CM NaHCO3= 0,09/ 0,5= 0,18M
Bài 59:Nung 34,6 gam hỗn hợp gồm Ca(HCO3)2, NaHCO3 và KHCO3 thu được 3,6 gam H2O và m gam hỗn hợp các muối cacbonat. Giá trị của m là:
A. 43,8
B. 22,2
C. 17,8
D. 21,8
Lời giải:
Đáp án B
Ca(HCO3)2 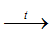
2NaHCO3 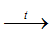
2KHCO3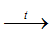
Theo các PTHH ta có: nCO2= nH2O= 3,6/18= 0,2 mol
Áp dụng định luật bảo toàn khối lượng ta có:
mmuối hidrocacbonat= mmuối cacbonat + mCO2 + mH2O
→ 34,6= m+ 0,2.44+ 3,6 → m=22,2 gam
Bài 60:Cho 300 ml dung dịch chứa NaHCO3 x mol/l và Na2CO3 y mol/l. Thêm từ từ dung dịch HCl z mol/l vào dung dịch trên đến khi bắt đầu có khí bay ra thì dừng lại, thấy hết t ml. Mối quan hệ giữa x, y, z, t là:
A. t.z=300xy
B. t.z= 150xy
C. t.z= 100xy
D. t.z= 300y
Lời giải:
Đáp án D
Ta có : nNaHCO3= 0,3x mol ; nNa2CO3= 0,3y mol
Thứ tự phản ứng :
Na2CO3 + HCl → NaCl + NaHCO3 (1)
NaHCO3 + HCl → NaCl + CO2 + H2O (2)
Thêm HCl đến khi bắt đầu có khí thì dừng lại
→ Phản ứng (1) xảy ra vừa đủ → nHCl= nNa2CO3
→ z.t/1000= 0,3y → t.z= 300 y
Bài 61:Nhỏ từ từ 62,5 ml dung dịch hỗn hợp Na2CO3 0,08M và KHCO3 0,12M vào 125 ml dung dịch HCl 0,1M và khuấy đều. Sau khi các phản ứng kết thúc, thu được V ml khí CO2 (đktc). Tính giá trị của V.
Lời giải:
Đáp án
Ta có: nH+= 0,125. 0,1= 0,0125 mol
CO32- + 2H+ → CO2 + H2O
0,005 0,01 0,005
HCO3- + H+ → CO2 + H2O
0,0075 0,0075 0,0075
Nếu phản ứng xảy ra vừa đủ thì : 0,0175 mol H+ 0,0125 mol CO2
Theo bài ra axit thiếu 0,0125 mol H+ 1/112 mol CO2 V=0,2 lít = 200 ml
Bài 62:Thêm từ từ từng giọt của 100 ml dung dịch chứa Na2CO3 1,2M và NaHCO3 0,6M vào 200 ml dung dịch HCl 1M, sau phản ứng hoàn toàn thu được dung dịch X. Cho dung dịch nước vôi trong dư vào dung dịch X thì thu được bao nhiêu gam kết tủa?
A. 10 gam
B. 8 gam
C. 6 gam
D. 12 gam
Lời giải:
Đáp án C
Ta có: nNa2CO3= 1,2.0,1= 0,12 mol; nNaHCO3= 0,1.0,6= 0,06 mol; nHCl= 0,2 mol
Thêm từ từ hỗn hợp Na2CO3 và NaHCO3 vào HCl
CO32- + 2H+ → CO2 + H2O
0,12 0,24
HCO3- + H+ → CO2 + H2O
0,06 0,06
Nếu phản ứng xảy ra vừa đủ thì cần 0,24 + 0,06= 0,3 mol H+ > 0,2 mol → H+ bị thiếu
Đặt nCO3(2-) pứ= x mol; nHCO3- pứ= y mol
CO32- + 2H+ → CO2 + H2O
x 2x
HCO3- + H+ → CO2 + H2O
y y
Ta có: nH+= 2x+ y= 0,2 mol
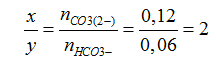
Giải hệ trên ta có : x= 0,08 mol ; y= 0,04 mol
Dung dịch X chứa 0,12-x= 0,04 mol CO32- và 0,06-y= 0,02 mol HCO3-
HCO3-+ OH- → CO32-+ H2O
0,02 0,02
Tổng số mol CO32- là 0,02+ 0,04= 0,06 mol
CO32-+ Ca2+ → CaCO3
0,06 0,06 mol → mCaCO3= 0,06.100= 6 gam
Bài 63:Sục 4,48 lít khí CO (đktc) phản ứng với 8 gam một oxit kim loại, sau khi phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 là 20. Giá trị của m là:
A. 7,2
B. 3,2
C. 6,4
D. 5,6
Lời giải:
Đáp án D
Đặt công thức oxit kim loại là MxOy: a mol. Ta có: nCO= 0,2 mol
MxOy + yCO → x M + y CO2
a ay ax ay mol
Sau phản ứng thu được (0,2-ay) mol CO và ay mol CO2
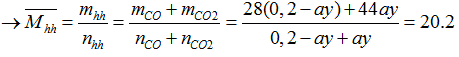
→ ay= 0,15 mol
Ta có: moxit kim loại= a(Mx+16y)= Max+ 16ay= 8 gam
→ Max= 8-16.0,15=5,6 gam=m
Bài 64:Sục 7,84 lít khí CO2 (đktc) vào 200 ml dung dịch NaOH 2M thu được 200 ml dung dịch X. Dung dịch Y chứa HCl 1M và H2SO4 x M. Cho từ từ đến hết 100 ml dung dịch Y vào 200 ml dung dịch X thu được 5,6 lít khí CO2 (đktc) và dung dịch Z. Cho BaCl2 dư vào dung dịch Z thu được m gam kết tủa. Giá trị của m là:
A. 23,30 gam
B. 43,00 gam
C. 46,60 gam
D. 34,95 gam
Lời giải:
Đáp án A
Ta có: nCO2= 0,35 mol; nNaOH= 0,2.2= 0,4 mol
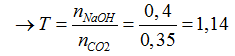
CO2 + NaOH → NaHCO3
x x x mol
CO2 + 2NaOH → Na2CO3 + H2O
y 2y ymol
Ta có: nCO2= x+y= 0,35 mol; nNaOH= x+2y= 0,4 mol
→ x=0,3 và y=0,05
Dung dịch X chứa 0,3 mol NaHCO3 và 0,05 mol Na2CO3
Trong 100 ml dung dịch Y có: nHCl= 0,1 mol; nH2SO4= 0,1x mol
→ nH+= 0,1+ 0,2x mol; nSO4(2-)= 0,1x mol
Cho từ từ 100 ml dung dịch Y vào 200 ml dung dịch X thu được nCO2= 0,25 mol
H++ CO32- → HCO3-
0,05 ← 0,05 → 0,05
H+ + HCO3- → CO2 + H2O
0,25 0,25 ← 0,25 mol
Ta có: nH+= 0,05+ 0,25= 0,1+ 0,2x → x=1 mol/l
Dung dịch Z có chứa Na+ ; HCO3- ; SO42-: 0,1x= 0,1 mol
Ba2+ + SO42- → BaSO4 ↓
nBaSO4= nSO4(2-)= 0,1 mol → mBaSO4= 0,1.233= 23,3 gam
Bài 65:Nung 9,28 gam hỗn hợp A gồm FeCO3 và một oxit sắt trong không khí đến khối lượng không đổi. Sau khi phản ứng xảy ra hoàn toàn, thu được 8 gam một oxit sắt duy nhất và khí CO2. Hấp thụ hết lượng khí CO2 vào 300 ml dung dịch Ba(OH)2 0,1M, kết thúc phản ứng thu được 3,94 gam kết tủa. Tìm công thức hoá học của oxit sắt.
A. FeO
B. Fe2O3
C. Fe3O4
D. FeO hoặc Fe2O3
Lời giải:
Đáp án C
Gọi công thức tổng quát của oxit sắt là FxOy ( x, y N*)
PTHH: 4FeCO3 + O2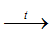
2FxOy +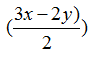
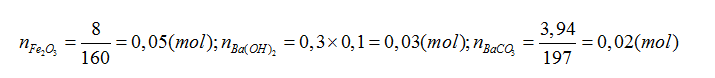
Cho CO2 vào dung dịch Ba(OH)2
PTHH: CO2 + Ba(OH)2 BaCO3 (3)
Có thể: 2CO2 + Ba(OH)2 Ba(HCO3)2 (4)
Trường hợp 1: Xảy ra các phản ứng 1, 2, 3
Theo PT(1), (3): 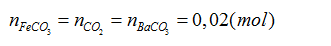
Theo (1): 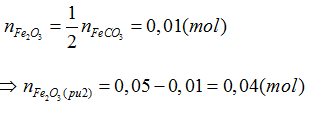
Theo PT(2): 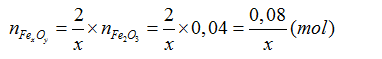
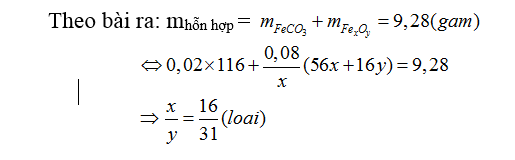
Trường hợp 2: Xảy ra các phản ứng 1, 2, 3, 4
Theo PT (3): 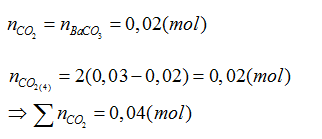
Theo PT(1), (3): 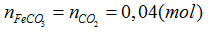
Theo (1): 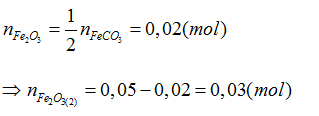
Theo PT(2): 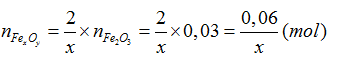
Theo bài ra: mhỗn hợp 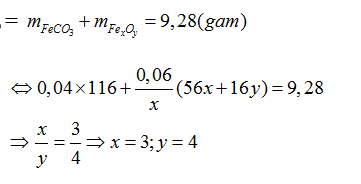
Vậy công thức oxit sắt là Fe3O4 ( sắt từ oxit)
Bài 66:Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào dung dịch chứa a mol NaOH và b mol Na2CO3 thu được dung dịch X. Chia X thành hai phần bằng nhau. Cho từ từ phần 1 vào 120 ml dung dịch HCl 1M thu được 2,016 lít khí CO2 (đktc). Cho phần 2 phản ứng hết với dung dịch Ba(OH)2 dư thu được 29,55 gam kết tủa. Tỉ lệ a: b tương ứng là:
A. 2 : 5
B. 2:3
C. 2:1
D. 1 :2
Lời giải:
Đáp án B
Ta có: nCO2= 0,15 mol; nCO2(phần 1)= 0,09 mol ; nBaCO3= 0,15 mol
Giả sử xảy ra các phản ứng:
CO2 + NaOH → Na2CO3 + H2O
CO2 + Na2CO3 +H2O → 2 NaHCO3
Dung dịch X chứa z mol NaHCO3 và t mol Na2CO3
Xét phần 1 ta có: giả sử có x mol NaHCO3 và y mol Na2CO3 phản ứng
NaHCO3 + HCl → NaCl + CO2 + H2O
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Ta có: nHCl= x+2y= 0,12 mol; nCO2=x+y= 0,09 mol
→ x= 0,06 và y= 0,03 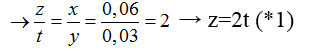
Xét phần 2 :
HCO3- + OH- → CO32-+ H2O
0,5z 0,5z
CO32- + Ba2+ → BaCO3 ↓
(0,5z+0,5t) → (0,5z+0,5t)
→ nBaCO3= 0,5z+ 0,5t= 0,15 (*2)
Từ (*1) và (*2) ta có: z= 0,2 mol; t= 0,1 mol
→ Dung dịch X chứa 0,2 mol NaHCO3 và 0,1 mol Na2CO3
Quay lại 2 phản ứng đầu :
CO2 + 2NaOH → Na2CO3 + H2O (1)
0,05 → 0,1 0,05
CO2 + Na2CO3 +H2O → 2 NaHCO3 (2)
0,1 0,1 ← 0,2 mol
Ta có: nCO2 PT 1= nCO2-nCO2 PT 2= 0,15- 0,1= 0,05 mol
Theo PT (1) : nNaOH=a= 0,1 mol
Số mol Na2CO3 còn sau phản ứng (2) là b+ 0,05- 0,1= 0,1 → b= 0,15
Do đó: 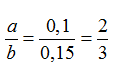
Bài 67:Thổi dòng khí CO đi qua ống sứ chứa 6,1 gam hỗn hợp A gồm CuO, Al2O3 và một oxit của kim loại R đốt nóng, tới khi phản ứng hoàn toàn thì chất rắn còn lại trong ống có khối lượng 4,82 gam. Toàn bộ lượng chất rắn này phản ứng vừa đủ với 150 ml dung dịch HCl 1M. Sau phản ứng thấy thoát ra 1,008 lít khí H2 (ở đktc) và còn lại 1,28 gam chất rắn không tan. Xác định công thức oxit của R trong hỗn hợp A.
A. Fe3O4
B. FeO
C. Fe2O3
D. ZnO
Lời giải:
Đáp án A
Vì khi cho chất rắn thu được sau phản ứng với CO tác dụng với dung dịch HCl tạo ra khí H2 nên R phải là kim loại đứng sau Al và đứng trước hidro trong dãy hoạt động hóa học. Đặt công thức oxit của R là RxOy.
CuO + CO → Cu + CO2
a a
RxOy + y CO → x R + y CO2
c xc
Al2O3 + 6 HCl → 2 AlCl3 + 3 H2O
b 6b
R + n HCl → RCln + n/2 H2
xc nxc xc nxc/2
Đặt số mol của CuO, Al2O3, RxOy trong 6,1 gam hỗn hợp A lần lượt là a, b và c. Có:
80a + 102b + (xMR + 16y)c = 6,1 (1)
1,28 + 102b + MRxc = 4,82 (2)
64a = 1,28 (3)
6b + nxc = 0,15 (4)
nxc/2 = 0,045 (5)
(3) => a = 0,02 ;
(5) => ncx = 0,09 (6)
(4) => b = 0,01 ;
(2) => MR = 28n;
=> n = 2; MR = 56, R là Fe
(6) => xc = 0,045 ; (1) => yc = 0,06
=> 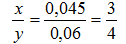
=> x = 3; y = 4, công thức oxit là Fe3O4 .
Bài 68:Hòa tan hoàn toàn 11,2 gam CaO vào nước ta thu được dung dịch A. Nếu hòa tan hoàn toàn 28,1 gam hỗn hợp MgCO3 và BaCO3 (trong đó chứa a% MgCO3 về khối lượng) bằng dung dịch HCl và cho tất cả khí thoát ra hấp thụ hết vào dung dịch A thì thu được kết tủa D. Hỏi a có giá trị bao nhiêu để kết tủa D lớn nhất?
A. 18,73
B. 43,93
C. 56,19
D. 29,89
Lời giải:
Đáp án D
CaO + H2O → Ca(OH)2
Ta có : nCa(OH)2= nCaO= 0,2 mol
PTHH: MgCO3 + 2HCl → MgCl2 + H2O + CO2↑ (4)
BaCO3 + 2HCl → BaCl2 + H2O + CO2↑ (5)
CO2 + Ca(OH)2 → CaCO3↓ + H2O (6)
CO2 + CaCO3 + H2O → Ca(HCO3)2 (7)
mMgCO3 = 28,1 . a% = 0,281a
mBaCO3 = 28,1 – 0,281a
Theo PTHH (4): nCO2(4) = n MgCO3 = 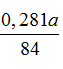
Theo PTHH (5): nCO2(5) = n BaCO3 = 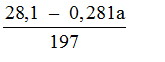
Tổng số mol CO2 = 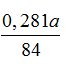
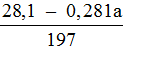
Khối lượng kết tủa D lớn nhất khi CO2 phản ứng vừa đủ với Ca(OH)2 ở (6). Có nghĩa là:
Số mol CO2 =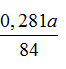
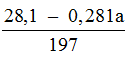
Giải ra ta được a = 29,89%
Bài 69:Khử hoàn toàn 32,20 gam hỗn hợp gồm CuO, Fe2O3 và ZnO bằng CO ở nhiệt độ cao thu được 25,00 gam hỗn hợp X gồm 3 kim loại. Cho X tác dụng vừa đủ với dung dịch HNO3 thì thu được V lít khí NO duy nhất (đktc) và dung dịch chứa m gam muối (không chứa NH4NO3). Giá trị V là
A. 20,16.
B. 60,48.
C. 6,72.
D. 4,48.
Lời giải:
Đáp án C
Bản chất: CO + Ooxit → CO2
Ta có: mchất rắn ban đầu= mX + mO (oxit) → mO (oxit)= 32,2- 25,0= 7,2 gam
→ nO (oxit)= 0,45 mol= nCO phản ứng
-QT cho electron:
C+2 → C+4+ 2e
0,45 → 0,9 mol
-QT nhận electron:
N+5+ 3e → NO
Theo định luật bảo toàn electron: ne cho= ne nhận → 0,9= 3.nNO
→ nNO= 0,3 mol → V= 6,72 lít
Bài 70:Hấp thụ hoàn toàn 0,672 lít khí CO2 (đktc) vào 1 lít dung dịch gồm NaOH 0,025M và Ca(OH)2 0,0125M thu được x gam kết tủa. Giá trị của x là:
A. 2,00
B. 0,75
C. 1,00
D. 1,25
Lời giải:
Đáp án C
nCO2= 0,03 mol; nCa(OH)2= 0,0125 mol; nNaOH= 0,025 mol
nOH-= 0,05 mol → 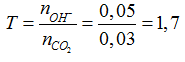
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có x+ y= 0,03; x+ 2y= 0,05 suy ra x= 0,01; y=0,02
Ca2+ + CO32- → CaCO3↓
0,0125 0,01 mol 0,01 mol
mCaCO3= 0,01.100= 1,00 gam
Bài 71:Hỗn hợp X gồm RCO3 và R’CO3. Nung m gam hỗn hợp X một thời gian thu được 3,36 lít khí CO2 (đktc) và còn lại chất rắn Y. Cho Y tác dụng với dung dịch HCl dư thu được dung dịch B và V lít khí CO2. Cho V lít khí CO2 hấp thụ hoàn toàn vào dung dịch Ba(OH)2 thu được 9,85 gam gam kết tủa và dung dịch D. Đun nóng dung dịch D thu được tối đa 9,85 gam kết tủa nữa. Phần dung dịch B đem cô cạn thu được 38,15 gam muối khan. Tính m.
A. 34,85
B. 31,75
C. 32,25
D. 33,15
Lời giải:
Đáp án A
Gọi công thức TB của hai muối cacbonat là:
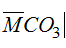
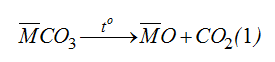
Chất rắn Y (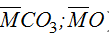
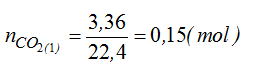
Y tác dụng với dung dịch HCl dư
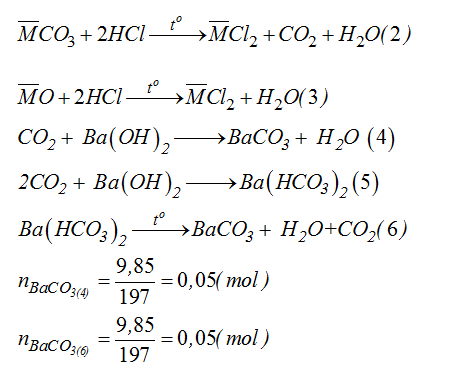
Theo PT (4,5,6):
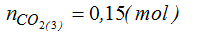
Theo PT (1,2): 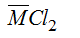
Muối khan là:
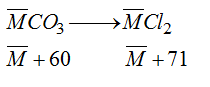
1 mol muối cacbonat phản ứng tạo 1 mol muối clorua tăng 11(g)
0,3 mol muối cacbonat phản ứng tạo 0,3 mol muối clorua tăng 3,3(g).
Khối lượng muối cacbonat ban đầu là: 38.15-3,3= 34,85(g)
Giá trị của m = 34,85(g)

