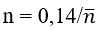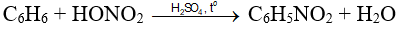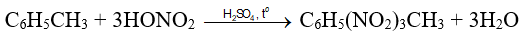Phản ứng thế của Benzen - Hoá học lớp 11
Phản ứng thế của Benzen
Với Phản ứng thế của Benzen Hoá học lớp 11 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Phản ứng thế của Benzen từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

A. Phương pháp giải & Ví dụ minh họa
Lưu ý:
- Phản ứng clo hóa, brom hóa (tº, Fe) hoặc phản ứng nitro hóa (tº, H2SO4 đặc) đối với hiđrocacbon thơm phải tuân theo quy tắc thế trên vòng benzen:
+ Nếu trong vòng benzen đã có sẵn một nhóm thế loại I – nhóm đẩy electron (nhóm ankyl –OH, NH2, -F, -Cl, -OCH3, -Br, -I, …) phản ứng thế xảy ra dễ hơn và định hướng cho nhóm thế mới vào vị trí ortho và para.
+ Nếu vòng benzen đã có sẵn nhóm thế loại II –nhóm hút electron (nhóm –NO2; -COOH, -CHO, -SO3H, …) sẽ định hướng cho nhóm thế mới vào vị trí meta.
- Phản ứng clo hóa, brom hóa có thể xảy ra ở phần mạch nhánh no của vòng benzen khi điều kiện phản ứng là ánh sáng khuếch tán và đun nóng (đối với brom).
Ví dụ minh họa
Bài 1: Cho 15,6 g C6H6 tác dụng hết với Cl2 (xúc tác bột sắt). Nếu hiệu suất của phản ứng là 80% thì khối lượng clobenzen thu được là bao nhiêu?
Hướng dẫn:
nC6H6 = 15,6 / 78 = 0,2 mol; mclobenzen = 0,2.0,8. 112,5 = 18 gam

Bài 2: Nitro hóa benzen được 14,1 gam hỗn hợp hai chất nitro có khối lượng phân tử hơn kém nhau 45 đvC. Đốt cháy hoàn toàn hỗn hợp hai chất nitro này được 0,07 mol N2. Tìm hai chất nitro?
Hướng dẫn:
Phương trình phản ứng:
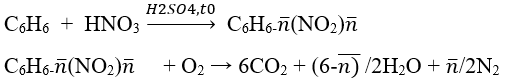
Số mol hỗn hợp:
Phân tử khối của hỗn hợp:
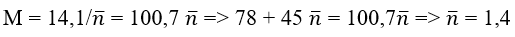
Vì hai chất nitro có khối lượng phân tử hơn kém nhau 45 đvC nên CT của 2 hợp chất nitro là: C6H5NO2 và C6H4(NO2)2.
Bài 3: Nitro hóa benzen được 14,1 gam hỗn hợp hai chất nitro có khối lượng phân tử hơn kém nhau 45 đvC. Đốt cháy hoàn toàn hỗn hợp hai chất nitro này được 0,07 mol N2. Hai chất nitro đó là:
Hướng dẫn:
Đặt CTPT chung của 2 hợp chất là C6H6-n(NO2)n
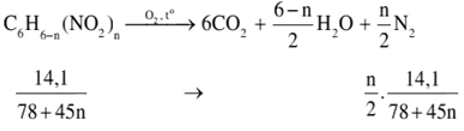
Ta có
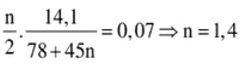
Hỗn hợp 2 chất nitro có khối lượng phân tử hơn kém nhau 45dvc nên phân tử của chúng hơn kém nhau 1 nhóm –NO2.
⇒ C6H5NO2 và C6H4(NO2)2.
B. Bài tập trắc nghiệm
Bài 1: Nitro hoá bezen thu được hỗn hợp 2 chất hữu cơ X và Y, trong đó Y nhiều hơn X một nhóm –NO2. Đốt cháy hoàn toàn 12,75 gam hỗn hợp X, Y thu được CO2, H2O và 1,232 lít N2 (đktc). Công thức phân tử và số mol X trong hỗn hợp là :
A. C6H5NO2 và 0,9. B. C6H5NO2 và 0,09.
C. C6H4(NO4)2 và 0,1. D. C6H5NO2 và 0,19.
Lời giải:
Đáp án: B
nN2 = 0,055 mol ⇒ nhh = 0,11/ntb ⇒ M = 116 ⇒ ntb = 1,1 = CTPT của X: C6H5NO2. Ta có: nX: nY = 9:1 ⇒ nX = 0,09 mol
Bài 2: Một hợp chất hữu cơ X có vòng benzen có CTĐGN là C3H2Br và M=236. Gọi tên hợp chất này biết rằng hợp chất này là sản phẩm chính trong phản ứng giữa C6H6 và Br2 (xúc tác Fe).
A. o- hoặc p-đibrombenzen
B. o- hoặc p-đibromuabenzen.
C. m-đibromuabenzen.
D. m-đibromben
Lời giải:
Đáp án: B
Đặt CTPT của hợp chất X là (C3H2Br)n suy ra (12.3+2+80).n = 236
⇒ n = 2. ⇒ C6H4Br2.
Vì X là sản phẩm chính trong phản ứng giữa C6H6 và Br2 (xúc tác Fe) nên theo quy tắc thế trên vòng benzen ta thấy X có thể là o- đibrombenzen hoặc p-đibrombenzen.
Bài 3: Khi cho clo tác dụng với 78 gam benzen (bột sắt làm xúc tác) người ta thu được 78 gam clobenzen. Hiệu suất của phản ứng là:
A. 69,33% B. 71% C. 72,33% D. 79,33%
Lời giải:
Đáp án: A
nbenzen = 1 mol; nclobenzen = 0,6933 mol ⇒ H = 69,33%
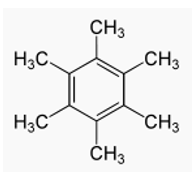
Bài 4: Đốt cháy hoàn toàn a gam hiđrocacbon X thu được a gam H2O. Trong phân tử X có vòng benzen. X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tạo thành dẫn xuất chứa 1 nguyên tử brom duy nhất. Tỉ khối hơi của X so với không khí có giá trị trong khoảng từ 5 đến 6. X là
A. Hexan. B. Hexametyl benzen.
C. Toluen. D. Hex-2-en.
Lời giải:
Đáp án: B
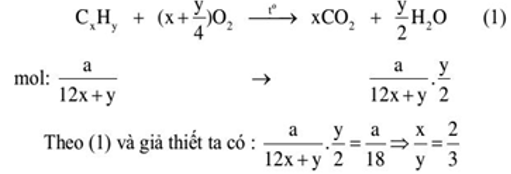
⇒CT đơn giản nhất của X là C2H3, CTPT (C2H3)n
Có 29.5 < 27n < 29.6 ⇒n=6 ⇒ C12H18
X có vòng benzen, X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tạo thành dẫn xuất chứa 1 nguyên tử brom duy nhất nên tên của X là : Hecxametyl benzen.

Bài 5: TNT (2,4,6- trinitrotoluen) được điều chế bằng phản ứng của toluen với hỗn hợp gồm HNO3 đặc và H2SO4 đặc, trong điều kiện đun nóng. Biết hiệu suất của toàn bộ quá trình tổng hợp là 80%. Tính lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluene?
A.524g B.378g C.454g D. 544g
Lời giải:
Đáp án: C
Số mol toluene tham gia phản ứng: ntoluen = 230/94 = 2,5 mol
Phương trình phản ứng:
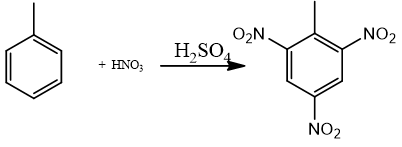
Lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluene:
mTNT = 2,5.227.80/100 = 454 gam
Bài 6: Cho benzen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế nitrobenzen. Khối lượng Nitrobenzen điều chế được từ 19,5 tấn benzen (hiệu suất phản ứng 80%) là
A. 30,75 tấn B. 38,44 tấn.
C. 15,60 tấn D. 24,60 tấn
Lời giải:
Đáp án: D
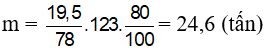
Bài 7: Cho toluen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế 2,4,6-trinitrotoluen (TNT). KHối lượng điều chế được từ 23 kg toluen (hiệu suất 80%) là
A. 45,40 kg B. 70,94 kg
C. 18,40 kg D. 56,75 kg
Lời giải:
Đáp án: A
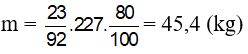
Bài 8: Toluen tác dụng với Br2 chiếu sáng (tỷ lệ mol 1 : 1), thu được sẩn phẩm hữu cơ là
A. o-bromtoluen B. m-bromtoluen.
C. phenylbromua D. benzylbromua
Lời giải:
Đáp án: D