Chuyên đề: Dẫn xuất Halogen, Ancol, Phenol - Hoá học lớp 11
Chuyên đề: Dẫn xuất Halogen, Ancol, Phenol
Với Chuyên đề: Dẫn xuất Halogen, Ancol, Phenol Hoá học lớp 11 tổng hợp các dạng bài tập, trên 350 bài tập trắc nghiệm có lời giải chi tiết với đầy đủ phương pháp giải, ví dụ minh họa sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Dẫn xuất Halogen, Ancol, Phenol từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

Tổng hợp Lý thuyết chương Dẫn xuất Halogen, Ancol, Phenol
- Lý thuyết Dẫn xuất halogen của hidrocacbon Xem chi tiết
- Lý thuyết Tính chất của Ancol Xem chi tiết
- Lý thuyết Tính chất của Phenol Xem chi tiết
- Lý thuyết Dẫn xuất halogen, ancol, phenol Xem chi tiết
Phương pháp giải các dạng bài tập chương Dẫn xuất Halogen, Ancol, Phenol
- 2 dạng bài tập Dẫn xuất halogen trong đề thi Đại học có giải chi tiết
- 6 dạng bài tập về Ancol trong đề thi Đại học có giải chi tiết
- Dạng bài tập về Phenol trong đề thi Đại học có giải chi tiết
- Dạng 1: Bài tập lý thuyết về dẫn xuất halogen, ancol, phenol
- Dạng 2: Cách viết đồng phân, gọi tên dẫn xuất halogen
- Dạng 3: Cách viết đồng phân, gọi tên Ancol, Phenol
- Dạng 4: Bài tập về dẫn xuất halogen
- Dạng 5: Ancol phản ứng với kim loại kiềm
- Dạng 6: Phenol phản ứng với kim loại kiềm và dung dịch kiềm
- Dạng 7: Phản ứng tách nước của Ancol
- Dạng 8: Phản ứng oxi hóa ancol
- Dạng 9: Độ rượu - Điều chế, nhận biết Ancol
Bài tập trắc nghiệm
- 125 câu trắc nghiệm Dẫn xuất Halogen, Ancol, Phenol có lời giải chi tiết (cơ bản)
- 125 câu trắc nghiệm Dẫn xuất Halogen, Ancol, Phenol có lời giải chi tiết (nâng cao)
Bài tập về dẫn xuất halogen
A. Bài tập tự luận
Bài 1: Đun nóng 13,875 gam một ankyl clorua Y với dung dịch NaOH, tách bỏ lớp hữu cơ, axit hóa phần còn lại bằng dung dịch HNO3, nhỏ tiếp vào dd AgNO3 thấy tạo thành 21,525 gam kết tủa. Xác định CTPT của Y?
Hướng dẫn:
Gọi CTPT của ankyl clorua Y là CnH2n+1Cl
Phương trình phản ứng: CnH2n+1Cl + NaOH → CnH2n+1OH + NaCl
NaCl + AgNO3 → AgCl ↓ + NaNO3
nAgCl = 21,525/143,5 = 0,15 mol ⇒ nankyl clorua = 0,15 mol
Mankyl clorua = 13,875/0,15 = 92,5 ⇒ n = 4.
Vậy CTPT của Y là: C4H9Cl
Bài 2: Cho 54,5 g một ankyl clorua X tác dụng với dung dịch KOH trong C2H5OH đun nóng nhẹ, thu được V lít khí Y và 7,45 g muối Z.
a. Xác định ankyl clorua
b. Tính thể tích khí thoát ra?
Hướng dẫn:

Số mol muối thu được: nKCl = 7,45/74,5 = 0,1 mol ⇒ nankyl clorua = 0,1 mol
Mankyl clorua = 5,45/0,1 = 54,5 ⇒ CT của X là C2H5Cl;
Số mol khí thu được: VC2H4 = 0,1.22,4 = 2,24 lít
Bài 3: Đun nóng 27,40 gam CH3CHBrCH2CH3 với KOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai olefin trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đktc) ? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%.
Hướng dẫn:
Khi đun nóng CH3CHBrCH2CH3 với KOH dư trong C2H5OH thì thu được hai sản phẩm hữu cơ là but-1-en và but-2-en.
Phương trình phản ứng :
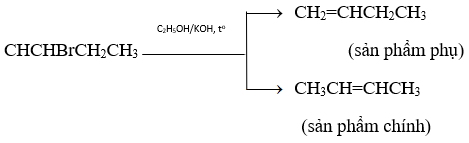
C4H8 + 6O2 −tº→ 4CO2 + 4H2O
Theo các phương trình phản ứng và giả thiết ta thấy :
nCO2 = 4nC4H8 = 4nCH3CHBrCH2CH3 = 4.27,4/137 = 4.0,2 = 0,8 mol
Vậy VCO2 = 0,8.22,4 = 17,92 lít.
B. Bài tập trắc nghiệm
Bài 1: Đun nóng 1,91 gam hỗn hợp X gồm C3H7Cl và C6H5Cl với dung dịch NaOH loãng vừa đủ, sau đó thêm tiếp dung dịch AgNO3 đến dư vào hỗn hợp sau phản ứng, thu được 1,435 gam kết tủa. Khối lượng C6H5Cl trong hỗn hợp đầu là :
A. 1,125 gam. B. 1,570 gam.
C. 0,875 gam. D. 2,250 gam.
Lời giải:
Đáp án: A
C3H7Cl + NaOH → C3H7OH + NaCl
Lưu ý: C6H5Cl không tác dụng với dung dịch NaOH ở điều kiện đun nóng
nC3H7Cl = nNaCl = nAgCl = 1,435/143,5 = 0,01 mol
⇒ mC6H5Cl = 1,91 - 0,01. 78,5 = 1,125g
Bài 2: Hỗn hợp X gồm 0,1 mol anlyl clorua ; 0,3 mol benzyl bromua ; 0,1 mol hexyl clorua ; 0,15 mol phenyl bromua. Đun sôi X với nước đến khi phản ứng xảy ra hoàn toàn, chiết lấy phần nước lọc, rồi cho tác dụng với dung dịch AgNO3 dư thu được m gam kết tủa. Giá trị của m là :
A. 28,7. B. 57,4. C. 70,75. D. 14,35.
Lời giải:
Đáp án: C
Khi đun sôi hỗn hợp X trong nước thì chỉ có anlyl clorua và benzyl bromua bị thủy phân.
C6H5CH2Br → HBr → AgBr
CH2=CH–CH2Cl → HCl → AgCl
m(tủa)= m AgBr + m AgCl =188. 0.3 + 143,5 .0,1 = 70,75g
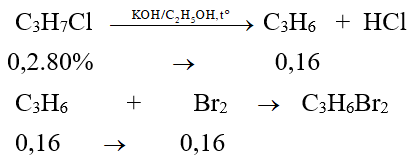
Bài 3: Đun sôi 15,7 gam C3H7Cl với hỗn hợp KOH/C2H5OH dư, sau khi loại tạp chất và dẫn khí sinh ra qua dung dịch brom dư thấy có x gam Br2 tham gia phản ứng. Tính x nếu hiệu suất phản ứng ban đầu là 80%.
A. 25,6 gam. B. 32 gam. C. 16 gam. D. 12,8 gam.
Lời giải:
Đáp án: A
Bài 4: Sản phẩm chính của phản ứng tách HBr của CH3CH(CH3)CHBrCH3 là :
A. 2-metylbut-2-en. B. 3-metylbut-2-en.
C. 3-metyl-but-1-en. D. 2-metylbut-1-en.
Lời giải:
Đáp án: A
Bài 5: Sản phẩm chính tạo thành khi cho 2-brombutan tác dụng với dung dịch KOH/ancol, đun nóng là :
A. Metylxiclopropan. B. But-2-ol.
C. But-1-en. D. But-2-en.
Lời giải:
Đáp án: D
Bài 6: Sản phẩm chính của phản ứng sau đây là chất nào ?
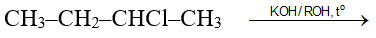
A. CH3–CH2–CH=CH2. B. CH2–CH–CH(OH)CH3.
C. CH3–CH=CH–CH3. D. Cả A và C.
Lời giải:
Đáp án: C
Bài 7: Cho sơ đồ:
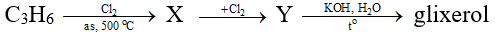
Các chất X, Y tương ứng là :
A. X: CH2=CH-CH2Cl, Y: CH2Cl-CHCl-CH2Cl.
B. X: CH2Cl-CHCl-CH3, Y: CH2Cl-CHCl-CH2Cl.
C. X: CH2Cl-CHCl-CH3, Y:CH2=CH-CH2Cl.
D. X: CHCl2-CH=CH2, Y: CH2Cl-CHCl-CHCl2.
Lời giải:
Đáp án: A
Bài 8: Cho hợp chất thơm : ClC6H4CH2Cl + dung dịch KOH (đặc, dư, to, p) ta thu được chất nào?
A. KOC6H4CH2OK. B. HOC6H4CH2OH.
C. ClC6H4CH2OH. D. KOC6H4CH2OH.
Lời giải:
Đáp án: D
Ancol phản ứng với kim loại kiềm
A. Phương pháp giải & Ví dụ minh họa
Lý thuyết và Phương pháp giải
- Cho ancol hoặc hỗn hợp ancol tác dụng với Na,K tạo thành muối ancolat + H2
R(OH)n + nNa → R(ONa)n + n/2 H2
- Dựa vào tổng số mol giữa ancol và H2 để xác định số nhóm chức
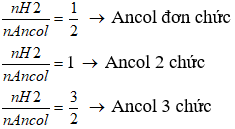
- Nếu nH2 ≥ nAncol → Ancol đa chức
Chú ý:
- nNa = 2nH2
- Nếu kim loại kiềm dư thì chúng sẽ phản ứng tiếp với nước để tạo ra khí H2
- Sử dụng các phương pháp: Tăng giảm khối lượng : 1mol Ancol → 1mol muối tăng 22 gam
+ Phương pháp bảo toàn khối lượng, Phương pháp trung bình.
Chú ý : + Khi cho dung dịch ancol (với dung môi là nước) phản ứng với kim loại kiềm thì xảy ra hai phản ứng :
2H2O + 2Na → 2NaOH + H2
2R(OH)n + 2nNa → 2R(ONa)n + nH2
Ví dụ minh họa
Bài 1: Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol đơn chức X, Y, Z thấy thoát ra 0,336 lít khí H2 (đkc). Khối lượng muối natri ancolat thu được là :
A. 2,4 gam. B. 1,9 gam. C. 2,85 gam. D. 3,8 gam.
Hướng dẫn:
Số mol khí H2 = 0,336/22,4 = 0,015 mol
Đặt công thức phân tử trung bình của ba ancol là
Phương trình phản ứng :
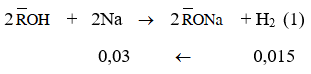
Cách 1 (sử dụng phương pháp bảo toàn khối lượng): Theo giả thiết, phương trình phản ứng (1), kết hợp với định luật bảo toàn khối lượng ta có:
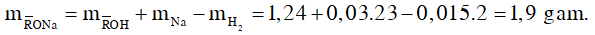
Cách 2 (Sử dụng phương pháp tăng giảm khối lượng): Theo (1) ta thấy cứ 1 mol 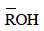
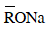
Đáp án B.
Bài 2: Hỗn hợp A chứa gixerol và một ancol đơn chức. Cho 20,30 gam A tác dụng với natri dư thu được 5,04 lít H2 ( đktc). Mặt khác 8,12 gam A hòa tan vừa hết 1,96 g Cu(OH)2. Xác định CTPT, Tính % về khối lượng của ancol đơn chức trong hỗn hợp A.
Hướng dẫn:
2C3H5 (OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Số mol gixerol trong 8,12 g A = 2 số mol Cu(OH)2 = 2.1,96/98 = 0,04 mol
Số mol gixerol trong 20,3 g A: 0,04.20,3/8,12 = 0,1 mol
Khối lượng gixerol trong 20,3 g A là : 0,1.92 = 9,2 (g)
Khối lượng ROH trong 20,3 g A là:
20,3 – 9,2 =11,1(g)
2C3H5 (OH)3 + Na → 2C3H5 (ONa)3 + 3H2
0,1.........................................................0,15
2ROH + 2Na → RONa + H2
x......................................0,5x
Số mol H2 = 0,15 + 0,5x = 5,04/22,4 = 0,225 → x = 0,15
Khối lượng 1 mol ROH: 11,1/0,15 = 74
R = 29; R là C4H9 –
CTPT: C4H10O
Phần trăm khối lượng C4H9OH = 11,1/20,3.100% = 54,68%
%C2H5OH = 32,86%
b/ C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
Khối lượng kết tủa = 0,1.331= 33,1(gam)
Bài 3: Cho 28,2 gam hỗn hợp hai rượu no đơn chức kế tiếp nhau trong dãy đồng đẳng tác dụng hết với Na (dư) sinh ra 8,4 lít H2 (đktc). Xác định CTPT và viết CTCT của hai rượu trên và tính % về khối lượng của chúng trong hỗn hợp, biết các phản ứng xảy ra hoàn toàn.
Hướng dẫn:
Gọi CTPT của hỗn hợp 2 rượu no, đơn chức là: 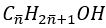
Số mol khí H2 sinh ra: nH2 = 8,4/22,4 = 0,375 mol
Phương trình phản ứng:
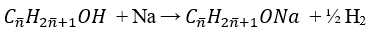
nhh ancol = 0,375.2 = 0,75 mol
Mhh = 28,2/0,75 = 37,6 g/mol
⇒ 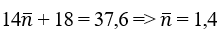
Vậy CTPT của 2 ancol: CH3OH và CH3CH2OH
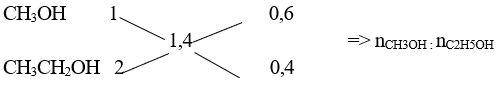
nCH3OH = 0,45 mol ; nC2H5OH = 0,3 mol
Phần trăm khối lượng mỗi ancol trong hỗn hợp:
%mCH3OH = 0,45.32/28,2.100% = 28,7%
%mC2H5OH = 100% - 28,7% = 73,1%
B. Bài tập trắc nghiệm
Bài 1: 13,8 gam ancol A tác dụng với Na dư giải phóng 5,04 lít H2 ở đktc, biết MA < 100. Vậy A có công thức cấu tạo thu gọn là :
A. CH3OH. B. C2H5OH. C. C3H6(OH)2. D. C3H5(OH)3.
Lời giải:
Đáp án: D
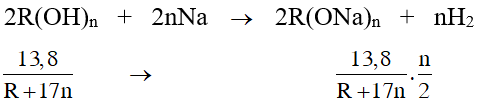
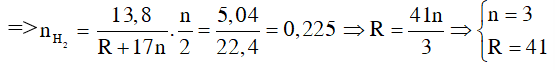
⇒C3H5(OH)3.
Bài 2: Cho 42 gam 1 ancol no, mạch hở, đơn chức l X phản ứng vừa đủ với Na thu được H2 và 57,4 gam muối. Vậy X là
A. CH4O. B. C2H6O. C. C3H8O. D. C4H10O.
Lời giải:
Đáp án: C
ROH + Na → RONa + ½ H2
nancol = (57,4-42)/22 = 0,7 mol ⇒ M = 42/0,7 = 60 ⇒ n = 3
Bài 3: Cho 68,913 gam 1 ancol hai chức Z phản ứng hết với Na thu được 24,8976 lít H2 (đktc). Vậy Z là
A. C2H6O2. B. C3H8O2. C. C4H10O2. D. C5H10O2.
Lời giải:
Đáp án: A
R(OH)2 + 2Na → R(ONa)2 + H2
nancol = nH2 = 1,1115 mol ⇒ Mancol = 62 = 14n + 2 + 32 ⇒ n = 2
Bài 4: Cho 10,1 gam hỗn hợp X gồm 2 ankanol đồng đẳng liên tiếp phản ứng với Na dư thu được 2,8 lít H2 (đktc). Vậy công thức của 2 ankanol trong hỗn hợp X là
A. CH3OH và C2H5OH. B. C2H5OH và C3H7OH.
C. C3H7OH và C4H9OH. D. C4H9OH và C5H11OH.
Lời giải:
Đáp án: A
nhh = 2nH2 = 0,25 mol ⇒ Mhh = 10,1/0,25 = 40,4 ⇒ ntb = 1,6
Bài 5: Cho 1 ancol mạch hở Z (trong đó có số nguyên tử oxi bằng số nguyên tử cacbon) phản ứng hoàn toàn với 2,3 gam Na thu được 4,97 gam chất rắn và 1,008 lít H2 (đktc). Vậy Z là
A. C2H6O2. B. C3H8O3. C. C4H10O4. D. C5H10O5.
Lời giải:
Đáp án: B
mancol = 4,97 + 0,09 – 2,3 = 2,76 g; nancol = nH2 = n.0,09 mol
⇒ M = 92/3n = 14n + 16n + 2 ⇒ n = 3
Bài 6: Cho 0,8 mol hỗn hợp A gồm 3 ancol có công thức phân tử lần lượt là C2H6O2, C3H8O2 và C5H12O2 phản ứng vừa đủ với Na, phản ứng xong thu được V lít H2 (đktc). Vậy giá trị của V là
A. 4,48. B. 8,96. C. 17,92. D. 35,84.
Lời giải:
Đáp án: C
R(OH)2 + 2Na → R(ONa)2 + H2
nH2 = nancol = 0,8 ⇒ V = 0,8.22,4 = 17,92 lít
Bài 7: Cho m gam hỗn hợp M gồm metanol, etanol và propenol phản ứng vừa đủ với Na thu được V lít H2 (đktc) và (m + 3,52) gam muối. Vậy giá trị của V là
A. 3,584. B. 1,792. C. 0,896. D. 0,448.
Lời giải:
Đáp án: A
nH2 = (m+3,52-m)/22 = 0,16 mol ⇒ V = 0,16.22,4 = 3,584 lít
Bài 8: Cho 37 gam hỗn hợp X gồm etanol, etilenglicol và glixerol phản ứng vừa đủ với Na thu được V lít H2 (đktc) và 50,2 gam muối. Vậy giá trị của V là
A. 6,72. B. 4,48. C. 2,24. D. 13,44
Lời giải:
Đáp án: A
2R(OH)n + 2nNa → 2R(ONa)n + nH2
nNa = (50,2-37)/22 = 0,6 mol ⇒ nH2 = 0,6/2 = 0,3 mol ⇒ V = 6,72 lít
Phenol phản ứng với kim loại kiềm và dung dịch kiềm
A. Phương pháp giải & Ví dụ minh họa
I. Phương pháp giải
Xác định CTCT của hợp chất phenol dựa vào số nhóm OH liên kết vào vòng benzen hoặc nhánh
TQ: Cho H/C thơm A (không chứa axit, este) tác dụng với NaOH , Na
Nếu A: - Có n nhóm OH trên vòng benzen và m nhóm OH trên nhánh:
2R(OH)n+m + 2(n+m)Na → 2R(ONa)n+m + (n+m)H2
nH2/nA = (n+m)/2 → (n+m) là số nhóm OH
Chỉ có n nhóm OH trên vòng benzen phản ứng với NaOH
R(OH)n+m + nNaOH R(OH)m(ONa)n + nH2O → Từ phản ứng này ta tìm được n, rồi tìm m.
II. Ví dụ minh họa
Bài 1: Hỗn hợp X gồm phenol và ancol etylic. Cho 14g hỗn hợp tác dụng với natri dư thấy có 2,24 lít khí thoát ra ( đktc).
a. Tính % khối lượng của các chất trong hỗn hợp.
b. Nếu cho 14 g X tác dụng với dung dịch brom thì có bao nhiêu gam kết tủa.
Hướng dẫn:
a. C6H5OH + Na → C6H5ONa + 1/2 H2
x x/2
C2H5OH + Na → C2H5ONa + 1/2 H2
y y/2
Theo bài ra ta có:
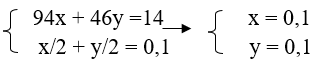
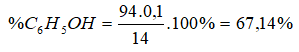
%C2H5OH = 32,86%
b. C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
Khối lượng kết tủa = 0,1.331= 33,1(gam)
Bài 2: Cho hỗn hợp X gồm etanol và phenol tác dụng với natri (dư) thu được 3,36 lít khí hi đro (đktc). Nếu hỗn hợp X trên tác dụng với nước brom vừa đủ, thu được 19,86 gam kết tủa trắng 2,4,6-tribromphenol. Thành phần phần trăm theo khối lượng của phenol trong hỗn hợp là bao nhiêu?
Hướng dẫn:
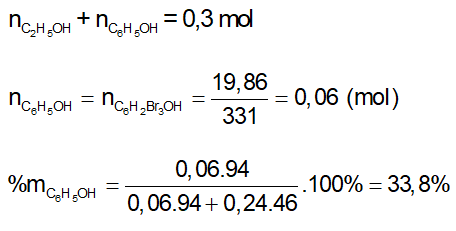
B. Bài tập trắc nghiệm
Bài 1: Một hỗn hợp gồm 25 gam phenol và benzen khi cho tác dụng với dung dịch NaOH dư thấy tách ra 2 lớp chất lỏng phân cách, lớp chất lỏng phía trên có thể tích 19,5 ml và có khối lượng riêng là 0,8g/ml. Khối lượng phenol trong hỗn hợp ban đầu là
A. 9,4 gam B. 0,625 gam C. 24,375 gam D. 15,6 gam
Lời giải:
Đáp án: A
mphenol = 25 – 0,8.19,5 = 9,4 (gam)
Bài 2: Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với natri (dư), thu được 2,24 lít khí H2 (đktc). Mặt khác, để phản ứng hoàn toàn với m gam X cần 100 ml dung dịch NaOH 1M. Giá trị của m là
A. 7,0 B. 21,0 C. 14,0 D. 10,5.
Lời giải:
Đáp án: C
nH2 = 0,1 mol ⇒ nX = 0,2 mol; nphenol = 0,1 mol ⇒ netanol = 0,1 mol ⇒ m = 0,1.94 + 0,1.46 = 14 g