Dạng bài tập Phản ứng trao đổi ion trong dung dịch - Hoá học lớp 11
Dạng bài tập Phản ứng trao đổi ion trong dung dịch
Với Dạng bài tập Phản ứng trao đổi ion trong dung dịch Hoá học lớp 11 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Phản ứng trao đổi ion trong dung dịch từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

A. Phương pháp giải & Ví dụ minh họa
Viết phương trình ion thu gọn
+ Viết phản ứng dạng phân tử, phân tích dạng phân tử thành dạng ion. Rút gọn những ion giống nhau ở hai vế, cân bằng điện tích và nguyên tử ở hai vế, thu được phương trình ion rút gọn.
+ Các chất kết tủa, chất khí và chất điện li yếu vẫn giữ ở dạng phân tử.
Ví dụ minh họa
Bài 1: Viết phương trình phân tử và ion rút gọn của các phản ứng sau (nếu có) xảy ra trong dung dịch:
a) KNO3 + NaCl b) NaOH + HNO3
c) Mg(OH)2 + HCl d) Fe2(SO4)3 + KOH
e) FeS + HCl f) NaHCO3 + HCl
g) NaHCO3 + NaOH h) K2CO3 + NaCl
i) CuSO4 + Na2S
Hướng dẫn:
a. Không xảy ra
b. NaOH + HNO3 → NaNO3 + H2O
H+ + OH- → H2O
c. Mg(OH)2 + 2HCl → MgCl2 + H2O
Mg(OH)2 + 2H+ → Mg2+ + H2O
d. Fe2(SO4)3 + 6KOH → 2Fe(OH)3↓ + 3K2SO4
Fe3+ + 3OH- → Fe(OH)3↓
e. FeS + 2HCl → FeCl2 + H2S↑
FeS + 2H+ → Fe2+ + H2S↑
f. NaHCO3 + HCl → NaCl + CO2↑ + H2O
HCO3- + H+ → CO2↑ + H2O
g. NaHCO3 + NaOH → Na2CO3 + H2O
HCO3- + OH- → CO32- + H2O
h. Không xảy ra
i. CuSO4 + Na2S → CuS↓ + Na2SO4
Cu2+ + S2- → CuS↓
Bài 2: Một dung dịch có chứa các ion: Mg2+, Cl-, Br-.
-Nếu cho dd này tác dụng với dd KOH dư thì thu được 11,6 gam kết tủa.
-Nếu cho dd này tác dụng với AgNO3 thì cần vừa đúng 200 ml dd AgNO3 2,5M và sau phản ứng thu được 85,1 g kết tủa.
a. Tính [ion] trong dd đầu? biết Vdd = 2 lít.
b. Cô cạn dung dịch ban đầu thì thu được bao nhiêu gam chất rắn?
Hướng dẫn:
Phương trình ion:
Mg2+ + 2OH- → Mg(OH)2↓
0,2 ← 0,2 mol
Ag+ + Cl- → AgCl↓; Ag+ + Br- → AgBr↓
Gọi x, y lần lượt là mol của Cl-, Br-.
x + y = 0,5 (1) ; 143,5x + 188y = 85,1 (2) . Từ (1),(2) ⇒ x = 0,2, y = 0,3
a.[Mg2+] = 0,2/2 = 0,1 M; [Cl-] = 0,2/2 = 0,1 M; [Br-] = 0,3/0,2 = 0,15 M
b. m = 0,2.24 + 0,2.35,5 + 0,3.80 = 35,9 gam

Bài 3: Dd X chứa các ion: Fe3+, SO42-, NH4+, Cl-. Chia dd X thành hai phần bằng nhau:
Phần 1: tác dụng với lượng dư dd NaOH, đun nóng thu được 0,672 lít khí (đktc) và 1,07 gam kết tủa.
Phần 2: tác dụng với lượng dư dd BaCl2, thu được 4,66 gam kết tủa. Tổng khối lượng các muối khan thu được khi cô cạn dd X là (quá trình cô cạn chỉ có nước bay hơi)
Hướng dẫn:
nNH4+ = nNH3 = 0,672/22,4 = 0,03 mol
nFe3+ = 1,07/107 = 0,01 mol; nSO42- = 4,66/233 = 0,02 mol
Áp dụng đL bảo toàn điện tích: 3.0,01 + 0,03 = 2.0,02 +x ⇒ x = 0,02
m = 0,01.56 + 0,03.18 + 0,02.96 + 0,02.35,5 = 3,73 gam
Khối lượng muối khan trong dung dịch X: 3,73.2 = 7,46 gam
Bài 4: Cho 100ml dung dịch hỗn hợp CuSO4 1M và Al2(SO4)3 1M tác dụng với dung dịch Ba(OH)2 dư, lọc lấy kết tủa nung đến khối lượng không đổi thu được chất rắn có khối lượng là
Hướng dẫn:
m = mCuO + mBaSO4 = 80.0,1 + 233.0,4 = 101,2 gam
Bài 5: Cho hỗn hợp rắn A gồm KCl và KBr tác dụng với dung dịch AgNO3 dư Lượng kết tủa sinh ra khi làm khô có khối lượng bằng lượng AgNO3 đã phản ứng. Thành phần % khối lượng KCl trong hỗn hợp A là
Hướng dẫn:
Gọi mol KCl, KBr lần lượt là x, y mol.
Ta có: 35,5x + 80y = 62.(x+y)
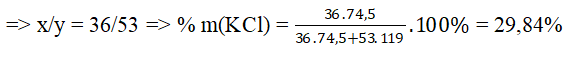
B. Bài tập trắc nghiệm
Bài 1: Phương trình ion rút gọn: H+ + HCO3- → CO2 ↑ + H2O tương ứng với PTHH dạng phân tử nào sau đây ?
(1) 2HCl + Na2CO3 → 2 NaCl + CO2 ↑ + H2O
(2) 2NaHCO3 + H2SO4 → Na2SO4 + 2CO2 ↑ + 2 H2O
(3) CaCO3 + 2HCl → CaCl2 + CO2 ↑ + H2O
(4) Ca(HCO3)2 + 2HCl → CaCl2 + 2CO2 ↑ + 2H2O
Lời giải:
Đáp án: B
Bài 2: Các tập hợp ion sau đây có thể tồn tại đồng thời trong cùng một dung dịch
A.Na+, Cu2+, OH-, NO3- B. Ca2+, Fe2+, NO3-, Cl-
C.Na+, Ca2+, HCO3-, OH- D. Fe2+, H+, OH-, NO3-
Lời giải:
Đáp án: B

Bài 3: Chất nào sau đây không tạo kết tủa khi cho vào dung dịch AgNO3
A. KBr B. K3PO4 C. HCl D. H3PO4
Lời giải:
Đáp án: D
Bài 4: Cho dung dịch chứa các ion sau : Na+ ,Ca2+ ,Mg2+ ,Ba2+ , H+ , NO3- . muốn tách được nhiều cation ra khỏi dung dịch mà không đưa ion lạ vào dung dịch người ta dùng :
A. dung dịch K2CO3 vừa đủ . B. dung dịch Na2SO4 vừa đủ.
C. dung dịch KOH vừa đủ. D. dung dịch Na2SO3 vừa đủ.
Lời giải:
Đáp án: D
Bài 5: Trong các cặp chất sau đây, cặp chất nào cùng tồn tại trong dung dịch ?
A. AlCl3 và Na2CO3 B. HNO3 và NaHCO3
C. NaAlO2 và KOH D. NaCl và AgNO3
Lời giải:
Đáp án: C
Bài 6: Phản ứng hóa học nào sau đây có phương trình ion thu gọn là H+ + OH → H2O ?
A. HCl + NaOH → H2O + NaCl
B. NaOH + NaHCO3 → H2O + Na2CO3
C. H2SO4 + BaCl2 → 2HCl + BaSO4
D. H2SO4 +Ba(OH)2 → 2 H2O + BaSO4
Lời giải:
Đáp án: A
Bài 7: Phương trình: S2- + 2H+ → H2S là phương trình ion rút gọn của phản ứng
A. FeS + 2HCl → FeCl2 + H2S↑.
B. 2NaHSO4 + 2Na2S → 2Na2SO4 + H2S↑
C. 2HCl + K2S → 2KCl + H2S↑.
D. BaS + H2SO4 → BaSO4↓ + H2S↑.
Lời giải:
Đáp án: C

Bài 8: Không thể có dung dịch chứa đồng thời các ion
A. Ba2+, OH-, Na+, SO42- B. K+, Cl-, OH-, Ca2+.
C. Ag+, NO3-, Cl-, H+ D. A và C đúng.
Lời giải:
Đáp án: D
Bài 9: Cho 1 lượng dư dung dịch AgNO3 vào 100 ml dung dịch hỗn hợp NaF 0,05M , NaCl 0,1M , NaBr 0,05M. Khối lượng kết tủa thu được là
A. 3,01 gam B. 2,375 gam C. 2,875 gam D. 3,375 gam
Lời giải:
Đáp án: B
m = 0,01.(108 + 35,5) + 0,005.(108 + 80) = 2,375 gam
Bài 10: Cho 4 dung dịch trong suốt, mỗi dung dịch chỉ chứa một loại cation và một loại anion trong các ion sau : Ba2+ ,Al3+ , Na+, Ag+ ,CO3- ,NO3- ,Cl- ,SO42-. Các dung dịch đó là :
A. BaCl2,Al2(SO4)3,Na2CO3,AgNO3.
B. Ba(NO3)2, Al2(SO4)3,Na2CO3, AgCl.
C. BaCl2, Al2(SO4)3,Na2CO3,AgNO3.
D. Ba(NO3)2, Al2(SO4)3,NaCl, Ag2CO3.
Lời giải:
Đáp án: A

