75 câu trắc nghiệm Hidrocacbon thơm - Nguồn Hidrocacbon thiên nhiên có lời giải chi tiết (nâng cao) - Hoá học lớp 11
75 câu trắc nghiệm Hidrocacbon thơm - Nguồn Hidrocacbon thiên nhiên có lời giải chi tiết (nâng cao)
Với 75 câu trắc nghiệm Hidrocacbon thơm - Nguồn Hidrocacbon thiên nhiên có lời giải chi tiết (nâng cao) Hoá học lớp 11 tổng hợp 75 bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Hidrocacbon thơm - Nguồn Hidrocacbon thiên nhiên từ đó đạt điểm cao trong bài thi môn Hoá học lớp 11.

Bài 1: C8H10 có bao nhiêu đồng phân?
A. 4 B. 5 C. 6 D. 7
Lời giải:
Đáp án A
Hướng dẫn
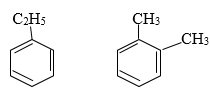
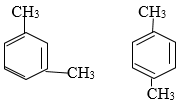
Bài 2: Cho 15,6 g C6H6 tác dụng hết với Cl2 (xúc tác bột sắt). Nếu hiệu suất của phản ứng là 80% thì khối lượng clobenzen thu được là bao nhiêu?
A. 18g B. 19g C. 20g D. 21g
Lời giải:
Đáp án A
Hướng dẫn
nC6H6 = 15,6 / 78 = 0,2 mol; mclobenzen = 0,2.0,8. 112,5 = 18 gam
Bài 3: Để phân biệt toluen, benzen, stiren chỉ cần dùng dung dịch
A. NaOH B. HCl
C. Br2 D. KMnO4
Lời giải:
Đáp án D
Hướng dẫn
Benzen không làm mất màu dd thuốc tím ở mọi điều kiện.
Toluen làm mất màu dd thuốc tím trong đk có nhiệt độ: 80-100 độ C
C6H5CH3 + 2KMnO4 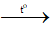
Stiren làm mất màu dd thuốc tím ở đk thường
3C6H5 -CH=CH2 + 2KMnO4 + 4H2O → 3 C6H5-CHOH-CH2OH + 2MnO2 + 2KOH
Bài 4: Cho sơ đồ điều chế polistiren:
Với 5,2 kg C2H2 có thể điều chế được bao nhiêu kg polistiren?
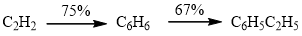
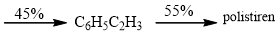
A. 0,57 kg B. 0,98 kg
C. 0,86 kg D. 1,2 kg
Lời giải:
Đáp án C
Hướng dẫn
nC2H2 = 0,2 mol ⇒ npolistiren = 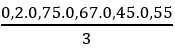
⇒ mpolistiren = 0,0083.104 = 0,86 kg
Bài 5: Đốt cháy hoàn toàn 9,2g một ankyl benzen A thu được 30,8g CO2. Công thức phân tử của A là:
A. C6H6 B. C8H10
C. C7H8 D. C9H12
Lời giải:
Đáp án C
Hướng dẫn
nCO2 = 0,7 mol; MA = 13,1n ⇒ n = 7 ⇒ A là C7H8
Bài 6: Lượng clobenzen thu được khi cho 15,6 gam C6H6 tác dụng hết với Cl2 (xúc tác bột Fe) với hiệu suất phản ứng đạt 80% là :
A. 14 gam. B. 16 gam.
C. 18 gam. D. 20 gam.
Lời giải:
Đáp án C
Hướng dẫn
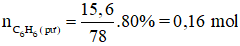
Phương trình phản ứng :
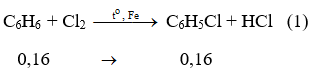
Vậy khối lượng clobenzen thu được là : 0,16.112,5= 18 gam.
Bài 7: Cho 13,8 gam chất hữu cơ X có công thức phân tử C7H8 tac dụng với một lượng dư dung dịch AgNO3 trong NH3, thu được 45,9 gam kết tủa. X có bao nhiêu đồng phân cấu tạo thõa mãn tính chất trên?
A. 5 B. 4 C. 6 D. 2
Lời giải:
Đáp án B
Hướng dẫn
Ta có:
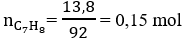
Phản ứng: C7H8 + xAgNO3 + xNH3 → C7H8-xAgx + xNH4NO3
nC7H8 = 0,15 mol ⇒ nC7H8-xAgx = 0,15 mol
⇒ (92 + 107x). 0,15 = 45,9 ⇒ x = 2.
Vậy X phải có 2 liên kết ba ở đầu mạch:
CH≡C – CH2 – CH2 – CH2 - C≡CH
CH≡C – CH(CH3) – CH2 - C≡CH
CH≡C – CH(C2H5) – C≡CH
CH≡C – C(CH3)(CH3) - C≡CH.
Bài 8: Dẫn 4,48 lít (đktc) hỗn hợp X gồm hai anken kế tiếp trong dãy đồng đẳng vào lượng dư dung dịch Br2, thấy dung dịch Br2 nhạt màu đồng thời khối lượng bình đựng tăng 7,0 gam. Công thức của 2 anken là
A. C2H4 và C3H6.
B. C3H6 và C4H8.
C. C4H8 và C5H10.
D. C5H10 và C6H12.
Lời giải:
Đáp án A
Hướng dẫn
Đặt CTPT 2 ankin là
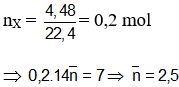
⇒ 2 anken: C2H4 và C3H6
Bài 9: Hiđrocacbon X là đồng đẳng của benzen có phần trăm khối lượng cacbon bằng 90,56%. Biết khi X tác dụng với brom có hoặc không có mặt bột sắt trong mỗi trường hợp chỉ thu được một dẫn xuất monobrom duy nhất. Tên của X là :
A. Toluen.
B. 1,3,5-trimetyl benzen.
C. 1,4-đimetylbenzen.
D. 1,2,5-trimetyl benzen.
Lời giải:
Đáp án C
Hướng dẫn
Đặt công thức phân tử của X là CnH2n-6 (n > 6).
Theo giả thiết ta có :
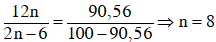
Vậy X có công thức phân tử là C8H12.
Vì X tác dụng với brom có hoặc không có mặt bột sắt trong mỗi trường hợp chỉ thu được một dẫn xuất monobrom duy nhất nên tên của X là: 1,4-đimetylbenzen.
Bài 10: Cho toluen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế 2,4,6-trinitrotoluen (TNT). Khối lượng điều chế được từ 23 kg toluen (hiệu suất 80%) là:
A. 45,40 kg B. 70,94 kg
C. 18,40 kg D. 56,75 kg
Lời giải:
Đáp án A
Hướng dẫn
C6H5CH3 + 3HONO2 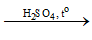
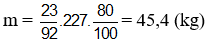
Bài 11: Từ etilen và benzene, tổng hợp được stiren theo sơ đồ:
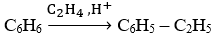
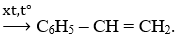
Tính khối lượng stiren thu được từ 1 tấn benzene nếu hiệu suất của quá trình là 78%.
A. 1,08 tấn B. 1,04 tấn
C. 2,08 tấn D.2,12 tấn
Lời giải:
Đáp án B
Hướng dẫn

Bài 12: Tỉ khối hơi của một hidrocacbon A với không khí là 3,586. Biết 2,08g A phản ứng tối đa với 1,792 lít H2 (đktc) và 3,12g A phản ứng vừa đủ với 100ml dung dịch brom 0,3M. Gọi tên A
A. Toluen B. Stiren
C. Benzen D. Naphtalen
Lời giải:
Đáp án B
Hướng dẫn
MA = 3,586.29 = 104
* Số mol H2:
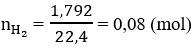
Số mol A khi phản ứng với H2 :
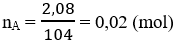
⇒ Ta có tỉ lệ: nA : nH2 = 0,02 : 0,08 = 1 : 4
⇒ Trong A có 4 liên kết π (1)
* Số mol Br2 : nBr2 = 0,3.0,1 = 0,03 (mol)
Số mol A khi phản ứng với Br2:
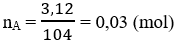
⇒ Ta có tỉ lệ: nA : nBr2 = 0,03 : 0,03 = 1 : 1
⇒ Trong A có một liên kết đôi ở mạch C = C (2)
Ta lại có: MA = 104
CxHy = 104 ⇒ 12x + y = 104 (3)
Kết hợp với điều kiên (1) (2) ta biện luận được x = 8; y =8
⇒ CTPT A: C8H8
CTCT A:
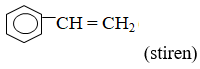
Bài 13: Đốt cháy hoàn toàn 0,1 mol hidrocacbon A, thu được 0,6 mol CO2 và 0,3 mol H2O. Cũng 0,1 mol A cho tác dụng hoàn toàn với lượng dư dung dịch AgNO3/NH3 thì thu được 29,2 gam kết tủa có màu vàng nhạt. A là:
A. 3-metyl penta-1,4-điin
B. Hexa-1,5-điin
C. hexa-1,3-dien-5-in
D. Cả A, B đúng
Lời giải:
Đáp án D
Hướng dẫn
Gọi công thức phân tử của hidrocabon A là CxHy
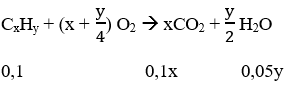
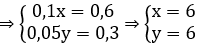
⇒ CTPT của A là C6H6.
2C6H6 + xAg2O 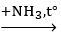
0,1 0,1 (với x là số nguyên tử H gắn ở nối ba)
⇒ 0,1.(72 + 6 – x + 108x) = 29,2 ⇒ x = 2.
⇒ Trong C6H6 phải có 2 nối ba đầu mạch
⇒ CTCT có thể có:
CH ≡ C – CH2 – CH2 – C ≡ CH : Hexa-1,5điin
và
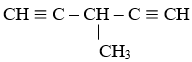
Bài 14: Hiđrocacbon X có tỉ khối đối với không khí xấp xỉ 3,173. Ở nhiệt độ thường X không làm mất màu nước brom. Khi đun nóng, X làm mất màu dung dịch KMnO4. X là
A. benzen B. etylbenzen
C. toluen D. stiren.
Lời giải:
Đáp án C
Hướng dẫn
MX = 3,173.29 = 92 (C7H8)
Bài 15: Đề hiđro hoá etylbenzen thu được stiren với hiệu suất là 60%. Đề hiđro hoá butan thu được butađien với hiệu suất là 45%. Trùng hợp butađien và stiren thu được sản phẩm A có tính đàn hồi rất cao với hiệu suất 75%. Để điều chế được 500 kg sản phẩm A cần khối lượng butan và etylbezen là bao nhiêu kg?
A. 544 và 745
B. 754 và 544
C. 335,44 và 183,54
D. 183,54 và 335,44.
Lời giải:
Đáp án A
Hướng dẫn ncao su buna-S = 500/158 = 3,16 mol; nbutan = 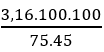
⇒ mbutan = 9,36.58 = 544 kg; netylbenzen = 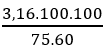
⇒ metylbenzen = 7,02.106 = 744,12 mol
Bài 16: Để điều chế được p-nitrotoluen từ benzene thì người ta tiến hành theo cách nào sau đây:
A. Bước 1: ankyl hóa; bước 2: nitro hóa.
B. Bước 1: nitro hóa; bước 2: ankyl hóa.
C. Thực hiện cả 2 bước đồng thời.
D. Ankyl hóa; bước 2: oxi hóa.
Lời giải:
Đáp án A
Hướng dẫn
Dựa vào quy luật thế trên nhân thơm: Thực hiện phản ứng ankyl hóa sau đó là phản ứng nitro hóa thì sản phẩm sẽ ưu tiên vị trí thế para
Bài 17: Hidrocacbon X có công thức phân tử C8H10 không làm mất màu dung dịch brom. Khi đun nóng X trong dung dịch KMnO4 tạo thành hợp chất C7H5KO2 (Y). Cho Y tác dụng với dung dịch HCl tạo thành hợp chất có công thức C7H6O2. Vậy tên gọi của X là:
A. etylbenzen
B. 1,2-đimetylbenzen
C. 1,3-đimetylbenzen
D. 1,4-đimetylbenzen.
Lời giải:
Đáp án A
Hướng dẫn
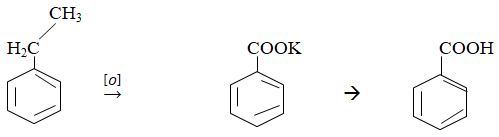
Bài 18: A là một đồng đẳng của benzene có công thức (C3H4)n. Tìm công thức phân tử A.
A. C9H12 B. C6H8
C. C12H16 D. C8H8
Lời giải:
Đáp án A
Hướng dẫn
A: (C3H4)n hay C3nH4n.
Vì A là đồng đẳng của benzene nên có dạng CmH2m-6.
Ta có:
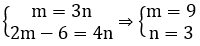
Vậy CTPT của A à C9H12
Bài 19: Cho 1 lít C6H6 (d = 0,8g/ml) tác dụng với 112 lít Cl2 (đktc) (xúc tác FeCl3) thu được 450g clobenzen. Hiệu suất phản ứng điều chế clobenzen là:
A. 62,5%
B. 75%
C. 82,5%
D. 80%
Lời giải:
Đáp án D
Hướng dẫn
Ta có:
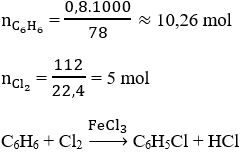
Giả sử hiệu suất phản ứng là 100%, dựa vào phương trình phản ứng ta thấy:
nCl2 = 5 mol < nC6 H6 = 10,26 mol ⇒ Hiệu suất tính theo Cl2.
Theo phương trình phản ứng: nC6 H5 Cl = nCl2 = 5 mol
⇒ 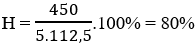

Bài 20: Đốt cháy hoàn toàn m g A đồng đẳng của benzen thu được 20,16 lít CO2 (đktc) và 10,8 ml H2O (lỏng). Công thức của A là:
A. C7H8 B. C8H10
C. C9H12 D. C10H14
Lời giải:
Đáp án C
Hướng dẫn
nCO2 = 20,16/22,4 = 0,9 mol; nH2O = 10,8/18 = 0,6 mol; 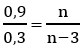
Bài 21: Nitro hóa benzen được 14,1 gam hỗn hợp hai chất nitro có khối lượng phân tử hơn kém nhau 45 đvC. Đốt cháy hoàn toàn hỗn hợp hai chất nitro này được 0,07 mol N2. Hai chất nitro đó là:
A. C6H5NO2 và C6H4(NO2)2.
B. C6H4(NO2)2 và C6H3(NO2)3.
C. C6H3(NO2)3 và C6H2(NO2)4.
D. C6H2(NO2)4 và C6H(NO2)5.
Lời giải:
Đáp án A
Hướng dẫn
Đặt CTPT chung của 2 hợp chất là C6H6-n(NO2)n
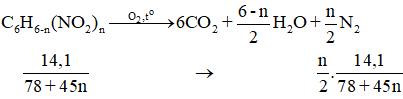
Ta có
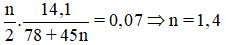
Hỗn hợp 2 chất nitro có khối lượng phân tử hơn kém nhau 45dvc nên phân tử của chúng hơn kém nhau 1 nhóm –NO2.
⇒ C6H5NO2 và C6H4(NO2)2.
Bài 22: C2H2 → A → B → m-bromnitrobenzen. A và B lần lượt là
A. Benzen; nitrobenzen
B. Benzen, brombenzen
C. Nitrobenzen; benzen
D. Nitrobenzen; brombenzen.
Lời giải:
Đáp án A
Hướng dẫn
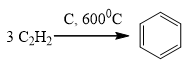
C6H6 + HNO3 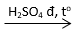
C6H5NO2 + Br2 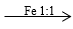
Bài 23: Nitro hoá bezen thu được hỗn hợp 2 chất hữu cơ X và Y, trong đó Y nhiều hơn X một nhóm –NO2. Đốt cháy hoàn toàn 12,75 gam hỗn hợp X, Y thu được CO2, H2O và 1,232 lít N2 (đktc). Công thức phân tử và số mol X trong hỗn hợp là :
A. C6H5NO2 và 0,9.
B. C6H5NO2 và 0,09.
C. C6H4(NO4)2 và 0,1.
D. C6H5NO2và 0,19.
Lời giải:
Đáp án B
Hướng dẫn
nN2 = 0,055 mol ⇒ nhh = 0,11/n− ⇒ M = 116 ⇒ n− = 1,1 = CTPT của X: C6H5NO2. Ta có: nX: nY = 9:1 ⇒ nX = 0,09 mol
Bài 24: Đốt cháy một thể tích hidrocacbon X thu được 7 thể tích CO2 ở cùng điều kiện. Biết tỉ khối hơi của X đối với oxi bằng 2,875. Vậy số nguyên tử hidro trong X là:
A. 8
B. 9
C. 10
D. 14.
Lời giải:
Đáp án A
Hướng dẫn
Phương trình phản ứng cháy:
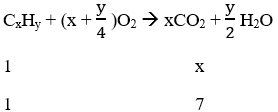
Vậy x = 7 ⇒ y = 8
Bài 25: Trùng hợp stiren thu được polistiren có khối lượng mol bằng 312000 gam. Hệ số trùng hợp của polistiren là:
A. 2575 B. 2750
C. 3000 D. 3500
Lời giải:
Đáp án C
Hướng dẫn
n = 31200/104 = 3000
Bài 26: Ankyl benzen X có phần trăm khối lượng cacbon bằng 91,31%. Gọi tên chất X.
A. Benzen B. Toluen
C. Stiren D. Cumen
Lời giải:
Đáp án B
Hướng dẫn
Đặt CTTQ X: CnH2n-6.
Theo đề %C = 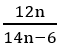
Vậy CTPT: C7H8. 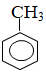
Bài 27: TNT (2,4,6- trinitrotoluen) được điều chế bằng phản ứng của toluen với hỗn hợp gồm HNO3 đặc và H2SO4 đặc, trong điều kiện đun nóng. Biết hiệu suất của toàn bộ quá trình tổng hợp là 80%. Lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluen là
A. 550,0 gam. B. 687,5 gam.
C. 454,0 gam. D. 567,5 gam.
Lời giải:
Đáp án C
Hướng dẫn
Phương trình phản ứng :
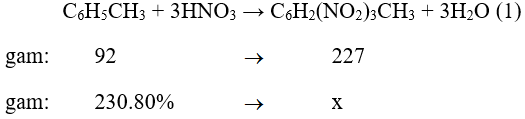
Theo phương trình và giả thiết ta thấy khối lượng TNT (2,4,6-trinitrotoluen) tạo thành từ 230 gam toluen với hiệu suất 80% là :
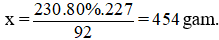
Bài 28: Đốt cháy hoàn toàn 0,1 mol CxHy thu được 15,68 lít CO2 (đktc) và 7,2 g H2O (lỏng). Công thức của CxHy là:
A. C7H8 C. C10H14
B. C8H10 D. C9H12
Lời giải:
Đáp án A
Hướng dẫn
nCO2 = 0,7 mol; nH2O = 0,4 mol; ⇒ x = 7; y = 8
Bài 29: Tiến hành thì nghiệm: Lấy 3 ống nghiệm đựng cùng một số mol ba chất benzene (1), toluen (2) và etylbenzen (3). Cho vào cả 3 ống nghiệm cùng một lượng Br2 sau đó cho thêm bột sắt và đun nóng. Vậy thứ tự làm mất màu brom như sau:
A. (1) → (2) → (3)
B. (2) → (1) → (3)
C. (3) → (2) → (1)
D. 3 ống nghiệm mất màu cùng lúc.
Lời giải:
Đáp án C
Hướng dẫn
Do các nhóm ankyl gây nên hiệu ứng cảm ứng +I đẩy electron, làm tăng mật độ trên nhân thơm. Do đó phản ứng thế xảy ra dễ dàng hơn so với benzene. Nhóm –C2H5 có hiệu ưng +I lớn hơn nhóm –CH3. Do đó thứ tự làm mất màu là (3) → (2) → (1).
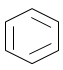
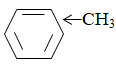
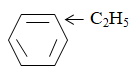
Bài 30: Chỉ dùng 1 thuốc thử nào dưới đây có thể phân biệt được các chất benzen, stiren, etylbenzen?
A. dd Brom C. dd AgNO3/NH3
B. dd KMnO4 D. dd HNO3
Lời giải:
Đáp án B
Hướng dẫn
Benzen không làm mất màu dd thuốc tím ở mọi điều kiện.
Etylen (Các ankyl benzen) làm mất màu dd thuốc tím trong đk có nhiệt độ: 80-100 độ C
Stiren làm mất màu dd thuốc tím ở đk thường
Bài 31: Cho một hidrocacbon X tác dụng được với hidro tạo thành hidrocacbon no Y. Phân tích thành phần nguyên tố của Y có 14,29% H, còn lại là cacbon. Tỉ khối hơi của Y đối với heli là 21. Xác định CTPT của X là:
A. C6H6 B. C6H12
C. C8H8 D. C8H10
Lời giải:
Đáp án A
Theo đề thì X là hidrocacbon không no hoặc thơm vì tác dụng được với hidro.
%C = 100% -14,29% = 85,71%
Đặt CTTQ Y: CxHy
Ta có: MY = 21 × 4 = 84
Tỉ lệ x : y = 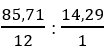
⇒ Y có dạng (CH2)n. Ta có : 14n =84 ⇒ n =6
Vậy CTPT của Y: C6H12 nên X là C6H6 (benzen).
Bài 32: Đốt cháy hết m gam 2 đồng đẳng của benzen A, B thu được 4,05 gam H2O và 7,728 lítCO2 (đktc). Giá trị của m và số tổng số mol của A, B là:
A. 4,59 và 0,04. B. 9,18 và 0,08.
C. 4,59 và 0,08. D. 9,14 và 0,04.
Lời giải:
Đáp án A
Hướng dẫn
nCO2 = 7,728/ 22,4 = 0,345 mol; nH2O = 4,05/18 = 0,225 ⇒ m = mC + mH = 0,345.12 + 0,225.2 = 4,59 g; n = (0,345 – 0,225)/3 = 0,04 mol
Bài 33: Đốt cháy hết 9,18 g 2 đồng đẳng của benzen A, B thu được 8,1 g H2O và CO2. Dẫn toàn bộ lượng CO2 vào 100ml dd NaOH 1M thu được m g muối. Giá trị của m và thành phần của muối:
A. 64,78 g (2 muối) B. 64,78g (Na2CO3)
C. 8,4g (NaHCO3) D. 10,6g (Na2CO3)
Lời giải:
Đáp án C
Hướng dẫn
mC = 9,18 – 0,45.2 = 8,28 gam; nCO2 = 0,69 mol; T = 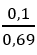
⇒ tạo muối NaHCO3
mNaHCO3 = 0,1. 84 = 8,4 g
Bài 34: Số đồng phân hidrocacbon thơm tương ứng với công thức C8H10 là:
A. 2 B. 3 C. 4 D. 5
Lời giải:
Đáp án C
Hướng dẫn
Số đồng phân của C8H10 là:
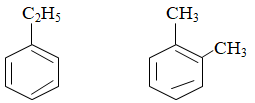
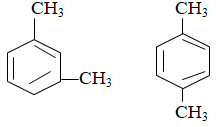
Bài 35: Trùng hợp 15,6 gam stiren thu được hỗn hợp A gồm polistiren và stiren dư. Lượng A tác dụng đủ với 200 ml dung dịch KMnO4 0,1 M. Khối lượng polistiren tạo thành là:
A. 50% B. 60% C. 70% D. 80%
Lời giải:
Đáp án D
Hướng dẫn
nstiren pu br2 = 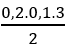
⇒ H = 0,12.100%/0,15= 80%
Bài 36: Cho các hỗn hợp gồm benzen, toluen và stiren. Có thể dùng hóa chất nào sau đây để nhận biết được chúng:
A. dung dịch brom
B. dung dịch KMnO4
C. dung dịch KOH
D. khí clo
Lời giải:
Đáp án B
Hướng dẫn
C6H5CH3 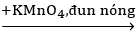
C6H5CH=CH2 
Benzen không làm mất màu brom.
Bài 37: Cho sơ đồ phản ứng sau:
CH4 → A → B → C 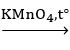
Vậy A, B, C là:
A. C2H4, C6H6, C6H5CH3
B. C2H2, C6H6, C6H5CH3
C. C2H4, C6H6, C6H4CH3
D. C2H2, C6H6, C6H5CH2
Lời giải:
Đáp án B
Hướng dẫn
Các phương trình phản ứng:
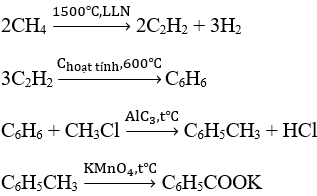
Bài 38: Một hợp chất hữu cơ X có vòng benzen có CTĐGN là C3H2Br và M=236. Gọi tên hợp chất này biết rằng hợp chất này là sản phẩm chính trong phản ứng giữa C6H6 và Br2 (xúc tác Fe).
A. o- hoặc p-đibrombenzen
B. o- hoặc p-đibromuabenzen.
C. m-đibromuabenzen.
D. m-đibromben
Lời giải:
Đáp án B
Hướng dẫn
Đặt CTPT của hợp chất X là (C3H2Br)n
⇒ (12.3+2+80).n = 236
⇒ n = 2. ⇒C6H4Br2.
Vì X là sản phẩm chính trong phản ứng giữa C6H6 và Br2 (xúc tác Fe) nên theo quy tắc thế trên vòng benzen ta thấy X có thể là o- đibrombenzen hoặc p-đibrombenzen.
Bài 39: Cho sơ đồ chuyển hóa sau:
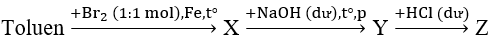
Trong đó X, Y, Z đều là hỗn hợp của các chất hữu cơ. Z có thành phần chính gồm:
A. m-metylphenol và o-metylphenol
B. benzyl bromua và o-bromtoluen
C. o-bromtoluen và p-bromtoluen
D. o-metylphenol và p-metylphenol.
Lời giải:
Đáp án D
Hướng dẫn
X: o-bromtoluen và p-bromtoluen; Y: o-NaO-C6H4-CH3 và p-NaO-C6H4-CH3
⇒ Z: o-metylphenol và p-metylphenol.

Bài 40: Đề hiđro hoá etylbenzen ta được stiren; trùng hợp stiren ta được polistiren với hiệu suất chung 80%. Khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren là :
A. 13,52 tấn. B. 10,6 tấn.
C. 13,25 tấn. D. 8,48 tấn.
Lời giải:
Đáp án C
Hướng dẫn
Sơ đồ phản ứng :
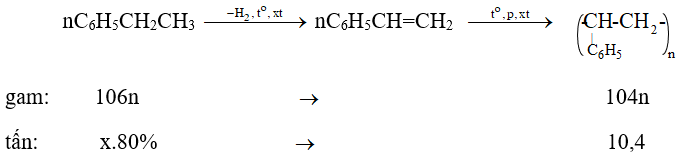
Vậy khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren với hiệu suất 80% là :
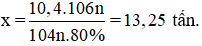
Bài 41: Đốt cháy hoàn toàn ankybenzen X thu được 7,84 lít CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của X là:
A. C6H6 B. C7H8
C. C8H8 D. C8H10
Lời giải:
Đáp án B
Hướng dẫn
Đặt CTPT X là CnH2n-6
3nX = nH2O – nCO2 = 0,35 – 0,2 = 0,15 mol ⇒ nX = 0,05 mol
⇒ 0,05n = 0,35 ⇒ n = 7 ⇒ CTPT C7H8
Bài 42: Để oxi hoá hết 10,6 gam o-xylen (1,2-đimetylbenzen) cần bao nhiêu lít dung dịch KMnO4 0,5M trong môi trường H2SO4 loãng. Giả sử dùng dư 20% so với lượng phản ứng.
A. 0,48 lít. B. 0,24 lít
C. 0,12 lít. D. 0,576 lít
Lời giải:
Đáp án C
Hướng dẫn
no-Xilen = 10,6/ 106 = 0,1 mol ⇒ nKMnO4pư = 0,1.2 = 0,2 mol; dùng dư 20% ⇒ nKMnO4 = 0,2.120/100 = 0,24 mol ⇒ V = 0,24/0,5 = 0,48 lít.
Bài 43: Cho phản ứng sau:
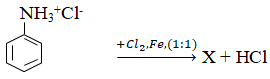
Vậy X là:
A. 3-clo-phenyl-amoniclorua
B. 2-clo-phenyl-amoniclorua
C. 4-clo-phenyl-amoniclorua
D. 2-clo-benzen-amoniclorua
Lời giải:
Đáp án A
Hướng dẫn
Do nhóm –NH3+ hút e làm giảm mật độ e trong nhân thơm, tuy nhiên tại các vị trí meta (3,5) ít giảm hơn, do đó chỉ cho sản phẩm thế tại các vị trí này.
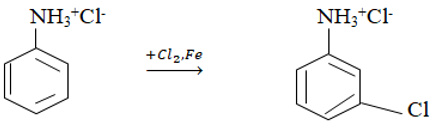
Bài 44: Đề hiđro hoá etylbenzen ta được stiren; trùng hợp stiren ta được polistiren với hiệu suất chung 80%. Khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren là:
A.13,52 tấn B.10,6 tấn
C.13,25 tấn D.8,48 tấn
Lời giải:
Đáp án C
Hướng dẫn
npolistiren = 10,4/104 = 0,1 tấn mol; netylbenzen = 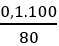
⇒ m = 0,125. 106 = 13,25 tấn
Bài 45: Chất nào sau đây làm mất màu dung dịch KMnO4 ở nhiệt độ thường?
A. benzen B. toluen
C. propan D. stiren
Lời giải:
Đáp án D
Hướng dẫn
- Stiren làm mất màu dung dịch KMnO4 và bị oxi hóa ở nhóm vinyl (giống như etilen) nên phản ứng xảy ra ngay nhiệt độ thường.
- Toluen làm mất màu dung dịch KMnO4 ở đk nhiệt độ 80-100ºC
- Benzen và Propan không làm mất màu dung dịch KMnO4
Bài 46: Khi cho clo tác dụng với 78 gam benzen (bột sắt làm xúc tác) người ta thu được 78 gam clobenzen. Hiệu suất của phản ứng là:
A. 69,33% B. 71%
C. 72,33% D. 79,33%
Lời giải:
Đáp án A
Hướng dẫn
nbenzen = 1 mol; nclobenzen = 0,6933 mol ⇒ H = 69,33%
Bài 47: Một hidrocacbon A tác dụng với H2/Ni, t°, theo tỉ lệ 1 : 3 tạo thành hidrocabon no B. Phân tích thành phần nguyên tố của B thấy tỉ lệ khối lượng mC : mH = 6 : 1. Tỉ khối của B đối với hidro là 42. Vậy CTPT của A và B là:
A. C6H12 và C6H6
B. C6H6 và C6H12
C. C6H10 và C6H12
D. C6H6 và C6H14.
Lời giải:
Đáp án B
Hướng dẫn
Gọi công thức B là CxHy.
Ta có: MB = 42.2 = 84.
Mặt khác 12x : y = 6 : 1 ⇒ y = 2x mà 12x + y = 84 ⇒ x = 6 và y = 12.
Theo đề ra, X là hidrocacbon no nên B là xiclohexan.
Vậy A là C6H6.
C6H6 + 3H2 → C6H12.
Bài 48: Để oxi hoá hết 10,6 gam o-xylen (1,2-đimetylbenzen) cần bao nhiêu lít dung dịch KMnO4 0,5M trong môi trường H2SO4 loãng. Giả sử dùng dư 20% so với lượng phản ứng.
A. 0,48 lít. B. 0,24 lít.
C. 0,12 lít. D. 0,576 lít.
Lời giải:
Đáp án D
Hướng dẫn
Phương trình phản ứng :
5H3C-C6H4-CH3 + 12KMnO4 + 18H2SO4 → 5HOOC-C6H4-COOH + 6K2SO4 + 12MnSO4 +28H2O
Theo phương trình và giả thiết ta có :
nKMnO4 = 0,24 + 0,24.20% = 0,288 mol
Vậy 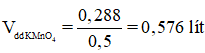
Bài 49: Đốt cháy hoàn toàn Hiđrocacbon X, thu đuộc CO2 và H2O có số mol theo tỉ lệ tương ứng 2 : 1. Mặt khác, 1 mol X tác dụng được tối đa với 4 mol H2 (Ni, t°) : 1 mol X tác dụng được tối đa 1 mol Br2. Công thức của X là.
A. C2H2 B. C4H4
C. C6H6 D. C8H8
Lời giải:
Đáp án D
Hướng dẫn
nC : nH = 2 : (1.2) = 1 : 1 ⇒ CTPT: CnHn
1 mol X + 4 mol H2 (Ni, tº); 1 mol X + 1 mol Br2
⇒ X chứa vòng benzen + 1 liên kết đôi ở nhánh ⇒ k = 5
CTPT X: CnH2n+2-2k ⇒ 2n + 2 – 2k = n ⇒ k = 5; n = 8 ⇒ CTPT: C8H8
Bài 50: Đốt cháy hết 9,18 g 2 đồng đẳng của benzen A, B thu được H2O và 30,36 g CO2. Cộng thức phân tử của A và B lần lượt là:
A. C8H10; C9H14 B. C8H10; C9H12
C. C8H12; C9H14 D. C8H14; C9H16
Lời giải:
Đáp án B
Hướng dẫn
nCO2 = 30,36/44 = 0,36 mol ⇒ nhh = 0,36/n− ⇒ M = 306n−/23 ⇒ n− = 8,625 ⇒ CTPT A và B là: C8H10; C9H12
Bài 51: Cho 19,5 gam benzen tác dụng với 48 gam brom (lỏng), có bột sắt làm chất xúc tác, thu được 27,475 gam brom benzen. Hiệu suất của phản ứng brom hóa benzen trên bằng:
A. 40% B. 50% C. 60% D. 70%
Lời giải:
Đáp án D
Hướng dẫn
Ta có:
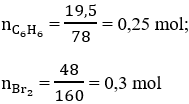
Giả sử H = 100%, dựa vào tỉ lệ mol ta thấy nC6 H6 < nBr2
⇒ Hiệu suất tính theo benzen.
C6H6 + Br2 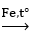
Ta có: nC6 H5 Br = 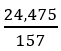
Theo phương trình phản ứng ta có: nC6 H6 )phản ứng = nC6 H5 Br = 0,175 mol
⇒ 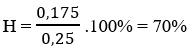
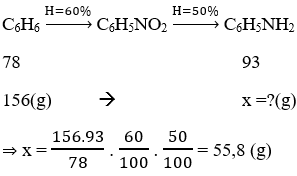
Bài 52: Người ta điều chế anilin bằng sơ đồ sau:
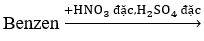
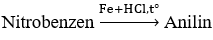
Biết hiệu suất giai đoạn tạo thành nitrobenzen đạt 60% và hiệu suất giai đoạn tạo thành anilin đạt 50%. Khối lượng anilin thu được khi điều chế từ 156 gam benzen là
A. 186,0 gam
B. 111,6 gam
C. 55,8 gam
D. 93,0 gam
Lời giải:
Đáp án C
Hướng dẫn
Sơ đồ phản ứng:
Bài 53: Hỗn hợp khí X gồm etilen, metan, propin và viyl axetilen có tỉ khối so với H2 là 17. Đốt cháy hoàn toàn 0,05 ml hỗn hợp X rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 (dư) thì khối lượng bình tăng thêm m gam. Giá trị của m là
A. 5,85 B. 3,39 C. 6,60 D. 7,30
Lời giải:
Đáp án D
Hướng dẫn
Đặt CTPT X: CxH4; MX = 17.2 = 34 ⇒ 12x + 4 = 34 ⇒ x = 2,5
⇒ nCO2 = 0,05.2,5 = 0,125 (mol); nH2O = 0,05.2 = 0,1 (mol)
⇒ m = 0,125.44 + 0,1.18 = 7,3 (gam)
Bài 54: 5,2 g stiren đã bị trùng hợp 1 phần tác dụng vừa đủ với dd chứa 0,0125 mol brom. Lượng stiren chưa bị trùng hợp chiếm bao nhiêu phần trăm trong 5,2 g:
A. 25% B. 50% C. 52% D. 75%
Lời giải:
Đáp án A
Hướng dẫn
nstiren không bị trùng hợp = 0,0125 mol ⇒ m = 0,0125.104 = 1,3 gam
⇒ %mstiren không bị trùng hợp = 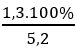

Bài 55: Sản phẩm chủ yếu trong hỗn hợp thu được khi cho toluen phản ứng với brom theo tỷ lệ mol 1 : 1 (có một bột sắt) là:
A. Benzybromua.
B. o-bromtoluen và p-bromtoluen.
C. p-bromtoluen và m-bromtoluen.
D. m-bromtoluen.
Lời giải:
Đáp án B
Hướng dẫn
Cần phân biệt điều kiện phản ứng
* Điều kiện xúc tác bột Fe:
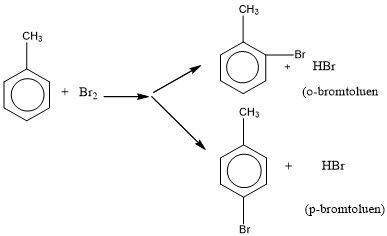
* Điều kiện chiếu sáng
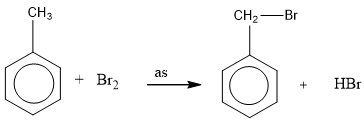
Bài 56: Một hidrocacbon X ở thể lỏng có phân tử khối < 115. Đốt 1,3 gam A thu được 4,4 g CO2 và 0,9 g H2O. 1 mol A tác dụng được với 4 mol H2 khi có xúc tác của Ni và với brom trong dung dịch theo tỉ lệ 1:1. Vậy công thức cấu tạo thu gọn của A là:
A. p-CH3 – C6H4 – CH3
B. C6H5 – CH = CH2
C. C6H5 – CH2 – CH =CH2
D. C6H5CH3
Lời giải:
Đáp án B
Hướng dẫn
Gọi công thức tổng quát của A là CxHy.
Phương trình phản ứng cháy như sau:
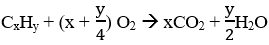
Số mol C = số mol CO2 = 4,4/44 = 0,1 mol; nH = 0,1 mol
⇒ Tỉ lệ x : y = 1 : 1
⇒ Công thức đơn giản nhất là CH ⇒ Công thức nguyên là (CH)n.
Theo đề bài: M < 115 ⇒ n < 8,7. Do đó n = 8, 7, 6…
Mặt khác: nA : nH2 = 1 : 4 ⇒ A có 4 liên kết π, trong đó có một liên kết π ở ngoài nhánh (tham gia phản ứng cộng Br2) và 3 liên kết π trong vòng benzene ⇒ A là stiren
Bài 57: Đốt cháy hoàn toàn a gam hiđrocacbon X thu được a gam H2O. Trong phân tử X có vòng benzen. X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tạo thành dẫn xuất chứa 1 nguyên tử brom duy nhất. Tỉ khối hơi của X so với không khí có giá trị trong khoảng từ 5 đến 6. X là
A. Hexan. B. Hexametyl benzen.
C. Toluen. D. Hex-2-en.
Lời giải:
Đáp án B
Hướng dẫn
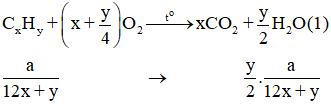
Theo (1) và giả thiết ta có:
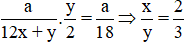
⇒CT đơn giản nhất của X là C2H3, CTPT (C2H3)n
Có 29.5 < 27n < 29.6 ⇒ n = 6 ⇒ C12H18
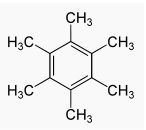
X có vòng benzene, X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tạo thành dẫn xuất chứa 1 nguyên tử brom duy nhất nên tên của X là : Hecxametyl benzen.
Bài 58: Sử dụng thuốc thử nào để nhận biết được các chất sau: benzen, stiren, toluen và hex – 1 – in
A. dd Brom và dd AgNO3/NH3
B. dd AgNO3
C. dd AgNO3/NH3 và KMnO4
D. dd HCl và dd Brom
Lời giải:
Đáp án C
Hướng dẫn
Dùng dd AgNO3/NH3 nhận được hex – 1 – in do có kết tủa vàng xuất hiện
- Cho KMnO4 vào ở nhiệt độ thường chất nào làm mất màu là stiren.
- Đun nóng dd KMnO4 chất nào làm mất màu là toluen, còn lại không có hiện tượng gì là benzen.
Bài 59: Đốt cháy hoàn toàn một thể tích hơi hợp chất hữu cơ A cần 10 thể tích oxi (đo cùng điều kiện nhiệt độ và áp suất), sản phẩm thu được chỉ gồm CO2 và H2O với mCO2 : mH2O = 44 : 9. Biết MA < 150. A có công thức phân tử là :
A. C4H6O. B. C8H8O.
C. C8H8. D. C2H2.
Lời giải:
Đáp án C
Hướng dẫn
Từ giả thiết mCO2 : mH2O = 44 : 9 suy ra : nCO2 : nH2O = 1 : 0,5 ⇒ nC : nH = 1 : 1.
A có thể có hoặc không có oxi, đặt công thức phân tử của A là CxHxOy.
Phương trình phản ứng :
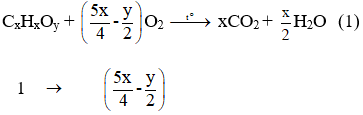
Theo (1) và giả thiết ta có :
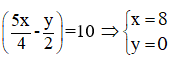
Vậy công thức phân tử của A là C8H8.
Bài 60: TNT (2,4,6- trinitrotoluen) được điều chế bằng phản ứng của toluen với hỗn hợp gồm HNO3 đặc và H2SO4 đặc, trong điều kiện đun nóng. Biết hiệu suất của toàn bộ quá trình tổng hợp là 80%. Tính lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluene?
A. 524g B.378g C.454g D. 544g
Lời giải:
Đáp án C
Hướng dẫn
Số mol toluene tham gia phản ứng: ntoluen = 230/94 = 2,5 mol
Phương trình phản ứng:
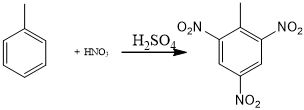
Lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluene:
mTNT = 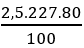
Bài 61: Lấy 97,5 gam benzen đem nitro hóa, thu được nitrobenzen (hiệu suất 80%). Đem lượng nitrobenzen thu được khử bằng hidro nguyên tử mới sinh bằng cách cho nitrobenzen tác dụng với bột sắt trong dung dịch HCl có dư (hiệu suất 100%), thu được chất hữu cơ X. Khối lượng chất X thu được là:
A. 93,00 gam
B. 129,50 gam
C. 116,25 gam
D. 103,60 gam.
Lời giải:
Đáp án A
Hướng dẫn
Ta có: 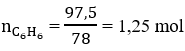
Sơ đồ phản ứng :
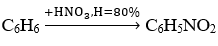
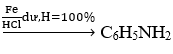
Dựa vào sơ đồ phản ứng ta có: nC6 H5 NH2 = 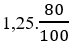
⇒ mC6 H5 NH2 = 1.93 = 93(g)
Bài 62: Đốt cháy hoàn toàn 5,3 gam ankybenzen X thu được 8,96 lít CO2 (đktc). Công thức phân tử của X là
A. C6H6 B. C7H8 C. C8H8 D. C8H10
Lời giải:
Đáp án D
Hướng dẫn
Đặt CTPT X là CnH2n-6
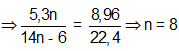
⇒ CTPT: C8H10
Bài 63: Cho toluen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế 2,4,6-trinitrotoluen (TNT). KHối lượng điều chế được từ 23 kg toluen (hiệu suất 80%) là
A. 45,40 kg B. 70,94 kg
C. 18,40 kg D. 56,75 kg
Lời giải:
Đáp án A
Hướng dẫn
C6H5CH3 + 3HONO2 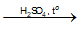
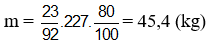
Bài 64: Tiến hành trùng hợp 10,4 gam stiren được hỗn hợp X gồm polistiren và stiren (dư). Cho X tác dụng với 200 ml dung dịch Br2 0,15M, sau đó cho dung KI dư vào thấy xuất hiện 1,27 gam iot. Hiệu suất trùng hợp stiren là:
A. 60%. B. 75%. C. 80%. D. 83,33%.
Lời giải:
Đáp án B
Hướng dẫn
nI2 = 1,27/254 = 0,005 mol ⇒ nstiren dư = 0,03 – 0,005 = 0,025 mol
⇒ nstiren pu = 0,1 – 0,025 = 0,075 mol ⇒ H = 75%.

Bài 65: Dãy các nhóm thế làm cho phản ứng thế vào vòng benzen dễ dàng hơn và ưu tiên vị trí o- và p- là:
A.CnH2n+1, -OH, -NH2,
B.-OCH3, -NH2, -NO2
C.-CH3, -NH2, -COOH
D.-NO2, -COOH, -SO3H
Lời giải:
Đáp án A
Bài 66: Chất hữu cơ X có công thức phân tử C6H6. Biết 1 mol X tác dụng với AgNO3/NH3 dư tạo ra 292 gam chất kết tủa. Khi cho X tác dụng với H2 dư (Ni, t°) thu được 3-metylpentan. Công thức cấu tạo của X là:
A. HC≡C – C – CH2 – CH3
B. HC≡ C – CH2 – CH = CH2
C. HC≡C – CH(CH3) – C ≡ CH
D. HC≡C – CH(CH3) – CH = C =CH2
Lời giải:
Đáp án C
Hướng dẫn
2C6H6 + xAg2O 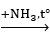
⇒ (78 – x + 108x).1 = 292 ⇒ x = 2.
⇒ Trong C6H6 phải có 2 nối ba đầu mạch.
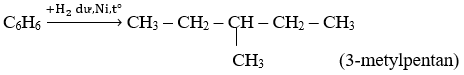
⇒ CTCT đúng của C6H6 :
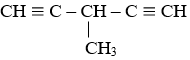
Bài 67: Đốt cháy hết 9,18 gam 2 đồng đẳng của benzen A, B thu được 8,1 gam H2O và V lít CO2 (đktc). Giá trị của V là :
A. 15,654. B. 15,465.
C. 15,546. D. 15,456.
Lời giải:
Đáp án D
Hướng dẫn
Đặt công thức phân tử trung bình của A và B là : 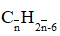
Theo giả thiết ta có :
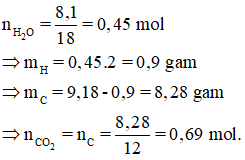
Vậy thể tích CO2 thu được là : 0,69.22,4 = 15,456 lít.
Bài 68: Đốt cháy hoàn toàn một thể tích V lít hỗn hợp gồm 2 hidrocacbon A và B ở thể khí ở điều kiện thường có khối lượng phân tử hơn kém nhau 28g. Sản phẩm tạo thành cho qua lần lượt các bình đựng P2O5 (dư) và CaO (dư). Bình P2O5 nặng thêm 9 gam còn bình CaO nặng 13,2g. Vậy A và B thuộc dãy đồng đẳng nào dưới đây:
A. Ankan
B. Anken
C. Ankadien
D. Aren.
Lời giải:
Đáp án A
Hướng dẫn
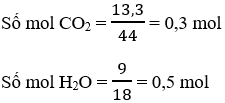
Ta thấy tỉ lệ số mol CO2 : số mol nước < 1 ⇒ A, B thuộc dãy đồng đẳng của ankan.
Bài 69: Để điều chế được m-nitrotoluen từ benzene thì người ta tiến hành theo cách nào sau đây:
A. Bước 1: ankyl hóa; bước 2: nitro hóa.
B. Bước 1: nitro hóa; bước 2: ankyl hóa.
C. Thực hiện cả 2 bước đồng thời.
D. Bước 1: nitro hóa; bước 2: khử nhóm – NO2.
Lời giải:
Đáp án B
Hướng dẫn
Dựa vào quy luật thế trên nhân thơm: Thực hiện phản ứng nitro hóa sau đó là phản ứng ankyl hóa thì sản phẩm sẽ ưu tiên vị trí thế meta
Bài 70: Nitro hóa benzen thu được 2 chất X, Y kém nhau 1 nhóm –NO2. Đốt cháy hoàn toàn 19,4g hỗn hợp X, Y thu được CO2, H2O và 2,24 lít s (đktc). CTCT đúng của X, Y là:
A. C6H5NO2 và C6H4(NO2)2
B. C6H4(NO2)2 và C6H3(NO2)3
C. C6H3(NO2)3 và C6H2(NO2)4
D. C6H5NO2 và C6H3(NO2)3
Lời giải:
Đáp án A
Hướng dẫn
Ta có: nN2 = 2,24/22,4 = 0,1 mol
Gọi x− là số nhóm –NO2 trung bình trong 2 chất X, Y.
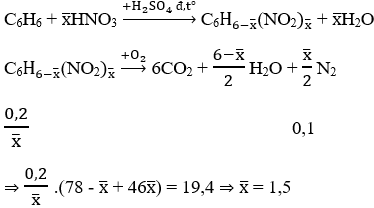
⇒ Trong X có 1 nhóm –NO2 và Y có 2 nhóm –NO2
Bài 71: Trùng hợp 10,4 gam stiren thu được hỗn hợp A gồm polistiren và stiren dư. Lượng A tác dụng đủ với 100 ml dung dịch Brom 3M. Hiêụ suất của phản ứng trùng hợp là:
A. 60% B.70% C. 75% D. 85%
Lời giải:
Đáp án B
Hướng dẫn
nstiren pu br2 = 0,3.0,1 = 0,03 mol; nstiren trùng hợp = 0,1 – 0,03 = 0,07 mol
⇒ H =0,07.100%/0,1= 70%
Bài 72: Đốt cháy hoàn toàn Hiđrocacbon X, thu được CO2 và H2O có số mol theo tỉ lệ tương ứng 2 : 1. Mặt khác, 1 mol X tác dụng được tối đa với 4 mol H2 (Ni, t°) : 1 mol X tác dụng được tối đa 1 mol Br2. Công thức của X là.
A. C2H2 B. C4H4 C. C6H6 D. C8H8
Lời giải:
Đáp án D
Hướng dẫn
nC : nH = 2 : (1.2) = 1 : 1 ⇒ CTPT: CnHn
1 mol X + 4 mol H2 (Ni, tº); 1 mol X + 1 mol Br2
⇒ X chứa vòng benzen + 1 liên kết đôi ở nhánh ⇒ k = 5
CTPT X: CnH2n+2-2k ⇒ 2n + 2 – 2k = n ⇒ k = 5; n = 8 ⇒ CTPT: C8H8
Bài 73: Cho benzen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế nitrobenzen. Khối lượng nitrobenzen điều chế được từ 19,5 tấn benzen (hiệu suất phản ứng 80%) là:
A. 30,75 tấn B. 38,44 tấn
C. 15,60 tấn D. 24,60 tấn
Lời giải:
Đáp án D
Hướng dẫn
C6H6 + HONO2 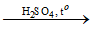
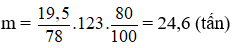
Bài 74: Đốt cháy hoàn toàn một thể tích hỗn hợp gồm 2 hidrocacbon X và Y ở thể khí ở điều kiện thường có khối lượng phân tư hơn kém nhau 28 gam. Sản phẩm tạo thành cho qua lần lượt các bình đựng H2SO4 (dư) và KOH (dư). Bình đựng H2SO4 nặng thêm 9 gam còn bình KOH nặng thêm 13,2 gam. Vậy X và Y là:
A. CH4 và C2H6
B. C2H6 và C4H10
C. CH4 và C3H8
D. C3H8 và C5H12
Lời giải:
Đáp án C
Hướng dẫn
Gọi công thức chung của 2 ankan là 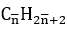
Ta có:
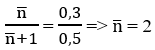
Như vậy phải có 1 ankan có số nguyên tử C nhỏ hơn 2. Do đó A là CH4 và B là C3H8.
Bài 75: Đốt cháy hết 9,18 gam 2 đồng đẳng kế tiếp thuộc dãy của benzen A, B thu được H2O và 30,36 gam CO2. Công thức phân tử của A và B lần lượt là :
A. C6H6 ; C7H8. B. C8H10 ; C9H12.
C. C7H8 ; C9H12. D. C9H12 ; C10H14.
Lời giải:
Đáp án B
Hướng dẫn
Đặt công thức phân tử trung bình của A và B là : 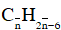
Phương trình phản ứng :
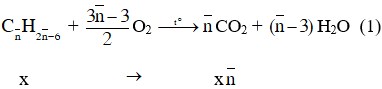
Theo (1) và giả thiết ta có :
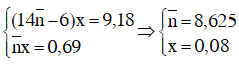
Vậy Công thức phân tử của A và B lần lượt là C8H10 và C9H12.

