Lý thuyết Dẫn xuất halogen, ancol, phenol - Hoá học lớp 11
Lý thuyết Dẫn xuất halogen, ancol, phenol
Tài liệu Lý thuyết Dẫn xuất halogen, ancol, phenol Hoá học lớp 11 sẽ tóm tắt kiến thức trọng tâm về Dẫn xuất halogen, ancol, phenol từ đó giúp học sinh ôn tập để nắm vứng kiến thức môn Hoá học lớp 11.

1. Ancol
- CTCT: CnH2n+1OH (n ≥ 1).
- Tên thông thường: Ancol + tên gốc ankyl + ic.
Ví dụ: C2H5OH: ancol etylic.
- Tên thay thế:
Tên ancol = tên hidrocacbon no mạch chính + số chỉ vị trí nhóm OH + ol.
Ví dụ:
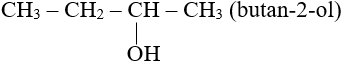
- Phản ứng thế H của nhóm OH:
R-OH + Na → R-ONa + 1/2 H2↑
- Phản ứng thế nhóm OH:
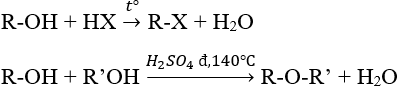
- Phản ứng tách nước:
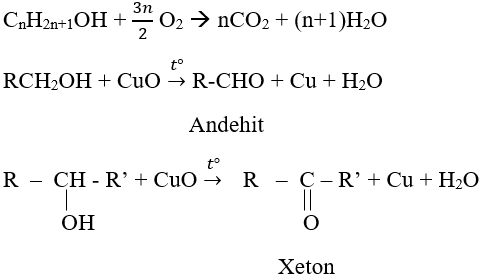
* Điều chế:
- Từ etilen:
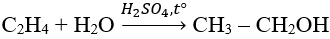
- Từ tinh bột:
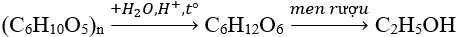
2. Phenol
- Tính axit (có lực axit mạnh hơn ancol) không làm đổi màu quỳ tím.
C6H5OH + NaOH → C6H5ONa + H2O
- Phản ứng thế nguyên tử H của nhóm –OH:
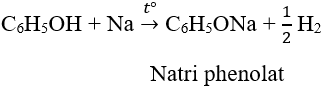
- Phản ứng thế nguyên tử H của vòng benzen (ưu tiên vị trí ortho và para)
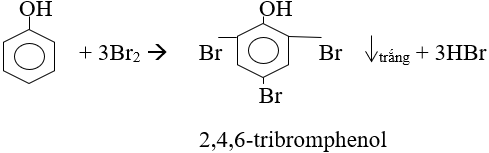
⇒ dùng nhận biết phenol.
* Điều chế:
- Oxi hóa cumen:
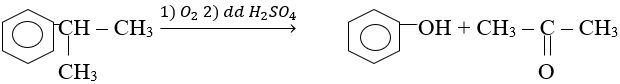
- Từ benzen: C6H6 → C6H5Br → C6H5ONa → C6H5OH.

3. Dẫn xuất halogen
a. Phản ứng thế
- Các ankyl halogenua không phản ứng với nước nhưng bị thủy phân khi đun nóng với dung dịch kiềm tạo ancol:
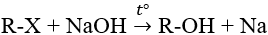
- Dẫn xuất loại anlyl halogenua bị thủy phân ngay khi đun sôi với nước:
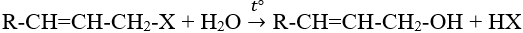
- Dẫn xuất loại vinyl halogenua và phenyl halogenua chỉ phản ứng với kiềm ở điều kiện nhiệt độ và áp suất cao:
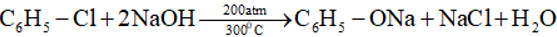
b. Phản ứng tách
Khi đun với dung dịch kiềm trong ancol, dẫn xuất halogen bị tách HX tạo thành liên kết bội:
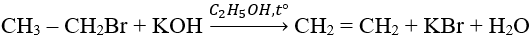
* Quy tắc Zai-xep: Khi tách HX khỏi dẫn xuất halogen, nguyên tử halogen (X) ưu tiên tách ra cùng với H ở nguyên tử C bậc cao hơn bên cạnh.
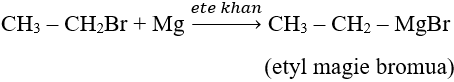
c. Ngoài ra có phản ứng với magie