Lý thuyết Tính chất của Phenol - Hoá học lớp 11
Lý thuyết Tính chất của Phenol
Tài liệu Lý thuyết Tính chất của Phenol Hoá học lớp 11 sẽ tóm tắt kiến thức trọng tâm về Tính chất của Phenol từ đó giúp học sinh ôn tập để nắm vứng kiến thức môn Hoá học lớp 11.

I. Định nghĩa, phân loại và tính chất vật lý
1. Định nghĩa
Phenol là dẫn xuất hiđrocacbon thơm trong đó 1 hay nhiều nguyên tử H của nhân benzen thay thế bằng nhóm –OH.
2. Phân loại
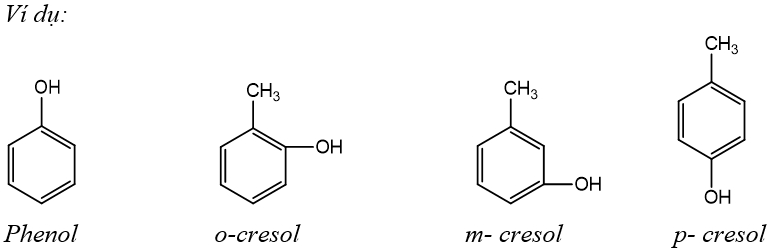
* Những phenol mà phân tử có chứa 1 nhóm OH thì phenol thuộc loại monophenol.
Ví dụ: phenol, o- crezol, m- crezol, p-crezol, ...
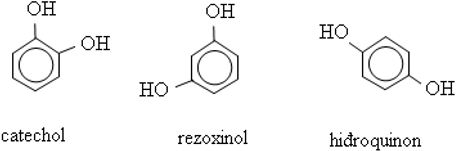
* Những phenol mà phân tử có chứa nhiều nhóm OH thì phenol thuộc loại poliphenol.
Ví dụ:
3. Tính chất vật lý
- Phenol là chất tinh thể không màu, nóng chảy ở nhiệt độ 42oC.
- Ở nhiêt độ thường, phenol ít tan trong nước, khi đun nóng độ tan tăng lên. Khi đun nóng ở nhiệt độ 70oC trở lên thì tan vô hạn trong nước. Phenol tan nhiều trong rượu, ete, clorofom, …
- Phenol độc, có tính sát trùng, làm bỏng da.
II. Tính chất hóa học
- Nhân hút e, –OH đẩy e.
1. Phản ứng thế nguyên tử hiđro của nhóm OH
* Tác dụng với kim loại kiềm:
C6H5OH + Na → C6H5ONa (Natri phenolat) + 1/2 H2↑
* Tác dụng với bazơ:
C6H5OH (rắn, không tan) + NaOH → C6H5ONa (tan, trong suốt) + H2O
→ Phenol có tính axit, tính axit của phenol rất yếu; dung dịch phenol không làm đổi màu quỳ tím.
Chú ý: tính axit yếu, không làm đổi màu quỳ tím, thứ tự: nấc II của H2CO3 < phenol < nấc I của H2CO3.
⇒ Có phản ứng:
C6H5ONa (dd trong suốt) + H2O + CO2 → C6H5OH (vẩn đục) + NaHCO3
C6H5OH + Na2CO3 → C6H5ONa + NaHCO3
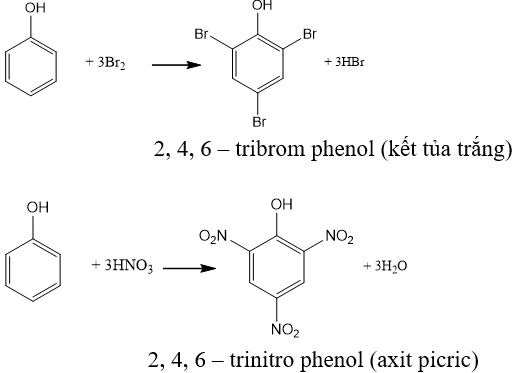
2. Phản ứng thế nguyên tử hiđro của vòng benzen
+ Phản ứng với H2:
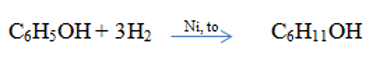
+ Phản ứng trùng ngưng với fomandehit:
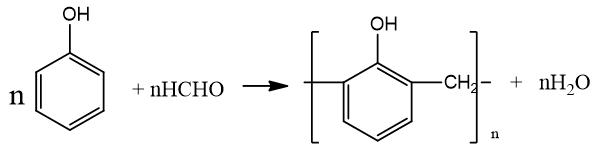

III. Ứng dụng và điều chế
1. Ứng dụng
- Phần lớn phenol dùng để sản xuất poli phenol – fomandehit.
- Điều chế dược phẩm, phẩm nhuộm, thuốc nổ (2,4,6- trinitrophenol), chất kích thích sinh trưởng thực vật, chất diệt cỏ, diệt sâu bọ, …
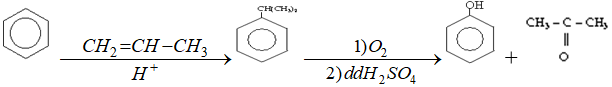
2. Điều chế
- Từ nhựa than đá:
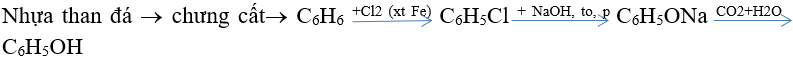
- Trong công nghiệp điều chế đồng thời phenol và xeton như sau: