Lý thuyết Hóa 11 Bài 2 Kết nối tri thức, Chân trời sáng tạo, Cánh diều
Haylamdo biên soạn và sưu tầm tóm tắt Lý thuyết Hóa học 11 Bài 2 Kết nối tri thức, Chân trời sáng tạo, Cánh diều hay, ngắn gọn giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn tập để học tốt Hóa học 11 Bài 2.
Lý thuyết Hóa học 11 Bài 2 (sách mới cả ba sách)
Lời giải sgk Hóa học 11 Bài 2:
(Kết nối tri thức) Giải Hóa 11 Bài 2: Cân bằng trong dung dịch nước
(Chân trời sáng tạo) Giải Hóa 11 Bài 2: Cân bằng trong dung dịch nước
Lưu trữ: Lý thuyết Hóa 11 Bài 2: Axit, bazơ và muối (sách cũ)
1. Axit, bazo, muối
a. Axit và bazơ theo thuyết Areniut
* Axit:Là chất khi tan trong nước phân li cho ion H+.
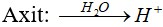
* Bazơ:Là chất khi tan trong nước phân li cho ion OH-.
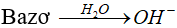
* Axit nhiều nấc:Những axit khi tan trong nước phân li nhiều nấc cho ion H+.
Ví dụ:
H3PO4 → H+ + H2PO4-
H2PO4- → H+ + HPO42-
HPO42- → H+ + PO43-
* Bazơ nhiều nấc:Những bazơ khi tan trong nước phân li nhiều nấc cho ion OH-.
Ví dụ:
Mg(OH)2 → Mg(OH)+ + OH-
Mg(OH)+ → Mg2+ + OH-
* Hiđroxit lưỡng tính: Là những hiđrôxit khi tan trong nước vừa có thể phân li như axit vừa có thể phân li như bazơ.
A(OH)n: Zn(OH)2, Pb(OH)2, Sn(OH)2, Cu(OH)2, Al(OH)3, Cr(OH)3.

Phân li theo kiểu bazơ:
Ví dụ:
Zn(OH)2 → Zn2+ + 2OH-
Al(OH)3 → Al3+ + 3OH-
Phân li theo kiểu axit:
Ví dụ:
Zn(OH)2 → ZnO22- + 2H+
Al(OH)3 → AlO2- + H3O+
b. Axit, bazơ theo Bronsted
|
Axit là chất (hoặc ion) nhường proton H+ Bazơ là chất (hoặc ion) nhận proton H+ |
Chú ý: Anion gốc axit còn H của axit yếu (H2CO3, H2SO3, H2S, H3PO4, …) đều là chất lưỡng tính, còn anion không còn H của axit yếu đều là bazơ.
Hằng số phân li axit (Ka) và bazơ (Kb).
Ví dụ:
CH3COOH → CH3COO- + H+
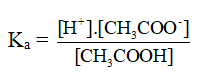
CH3COOH + H2O → CH3COO- + H+
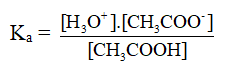
NH3 + H2O → NH4+ + OH-
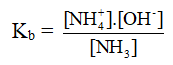
- Vì nồng độ của nước được coi như hằng số nên ta có thể bỏ qua nồng độ của nước trong biểu thức xác định hằng số phân li axit, hay bazơ.
- Đối với bazơ nhiều nấc sẽ có nhiều hằng số phân li ở các nấc khác nhau.
- Hằng số phân li bazơ chỉ phụ thuôc vào bản chất bazơ và nhiệt độ. Nếu giá trị Kb càng nhỏ thì lực bazơ của nó càng yếu (hay tính bazơ càng yếu).
- Mối liên hệ giữa hằng số Ka và Kb.
Ka = 10-14/Kb hay Ka. Kb = 10-14.
Muối axit, muối trung hoà
+ Muối axit: Muối có anion gốc axit còn khả năng phân li cho ion H+.
Ví dụ: NaHCO3; NaH2PO4; NaHSO4; ...
+ Muối trung hoà: Muối có anion gốc axit không còn khả năng phân li cho ion H+.
Ví dụ: NaCl , (NH4)2SO4, Na2CO3, ...
+ Muối bazo: Muối có nhóm –OH có thể thay thế bằng gốc axit.
Ví dụ: Mg(OH)Cl; Fe(OH)2Cl, ...
+ Ngoài ra còn kể đến một số muối kép như: HCl.NaCl; KCl.MgCl.6H2O; K2SO4.Al2(SO4)3, ...
+ Muối phức: [Ag(NH3)2]Cl; [Cu(NH3)4]SO4, ...
Sự điện li của muối trong nước: Hầu hết các muối (kể cả muối kép) khi tan trong nước phân li hoàn toàn thành cation kim loại (NH4+) và anion gốc axit.