Lý thuyết Hóa 11 Bài 8 Kết nối tri thức, Chân trời sáng tạo, Cánh diều
Haylamdo biên soạn và sưu tầm tóm tắt Lý thuyết Hóa học 11 Bài 8 Kết nối tri thức, Chân trời sáng tạo, Cánh diều hay, ngắn gọn giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn tập để học tốt Hóa học 11 Bài 8.
Lý thuyết Hóa học 11 Bài 8 (sách mới cả ba sách)
Lời giải sgk Hóa học 11 Bài 8:
(Kết nối tri thức) Giải Hóa 11 Bài 8: Sulfuric acid và muối sulfate
(Cánh diều) Giải Hóa 11 Bài 8: Hợp chất hữu cơ và hoá học hữu cơ
(Chân trời sáng tạo) Giải Hóa 11 Bài 8: Hợp chất hữu cơ và hóa học hữu cơ
Lưu trữ: Lý thuyết Hóa 11 Bài 8: Amoniac và muối amoni (sách cũ)
A. AMONIAC
I. Cấu tạo phân tử
Trong phân tử NH3, N liên kết với ba nguyên tử hidro bằng ba liên kết cộng hóa trị có cực. NH3 có cấu tạo hình chóp với nguyên tử Nitơ ở đỉnh. Nitơ còn một cặp electron hóa trị là nguyên nhân tính bazơ của NH3.
II. Tính chất vật lý
- Amoniac (NH3) là chất khí không màu, có mùi khai xốc, nhẹ hơn không khí, tan rất nhiều trong nước.
III. Tính chất hóa học
1. Tính bazơ yếu
- Tác dụng với nước:
NH3 + H2O ⇋ NH4+ + OH-
⇒ Dung dịch NH3 là một dung dịch bazơ yếu.
- Tác dụng với dung dịch muối (muối của những kim loại có hidroxit không tan):
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+
- Tác dụng với axit → muối amoni:
NH3 + HCl → NH4Cl (amoni clorua)
2NH3 + H2SO4 → (NH4)2SO4 (amoni sunfat)
2. Khả năng tạo phức
Dung dịch amoniac có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại, tạo thành các dung dịch phức chất.
Ví dụ:
* Với Cu(OH)2:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh thẫm)
* Với AgCl:
AgCl + 2NH3 → [Ag(NH3)2]Cl
Sự tạo thành các ion phức là do sự kết hợp các phân tử NH3 bằng các electron chưa sử dụng của nguyên tử nitơ với ion kim loại.
3. Tính khử
- Amoniac có tính khử: phản ứng được với oxi, clo và khử một số oxit kim loại (Nitơ có số oxi hóa từ -3 đến 0, +2).
- Tác dụng với oxi:
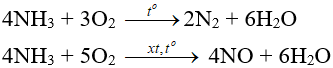
- Tác dụng với clo:
2NH3 + 3Cl2 → N2 + 6HCl
NH3 kết hợp ngay với HCl vừa sinh ra tạo “khói trắng” NH4Cl
- Tác dụng với CuO:
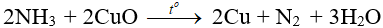
IV. Ứng dụng
- Sản xuất axit nitric, các loại phân đạm như ure (NH2)2CO; NH4NO3; (NH4)2SO4; …
- Điều chế hidrazin (N2H4) làm nhiên liệu cho tên lửa.
- Amoni lỏng dùng làm chất gây lạnh trong máy lạnh.
V. Điều chế
1. Trong phòng thí nghiệm
Đun nóng muối amoni với Ca(OH)2
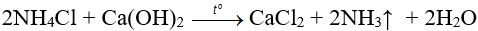
2. Trong công nghiệp
Tổng hợp từ nitơ và hiđro
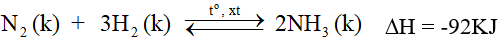
- Nhiệt độ: 450 – 500oC.
- Áp suất cao từ 200 – 300 atm.
- Chất xúc tác: sắt kim loại được trộn thêm Al2O3, K2O, ...
Làm lạnh hỗn hợp khí bay ra, NH3 hóa lỏng được tách riêng.

B. MUỐI AMONI
Là tinh thể ion gồm cation NH4+ và anion gốc axit.
I. Tính chất vật lý
- Là những hợp chất tinh thể ion, phân tử gồm cation NH4+ và anion gốc axit.
- Tan nhiều trong nước điện ly hoàn toàn thành các ion.
NH4Cl → NH4+ + Cl-; Ion NH4+ không có màu.
II. Tính chất hóa học
1.Phản ứng thuỷ phân: Tạo môi trường có tính axit làm quỳ tím hoá đỏ.
NH4+ + HOH → NH3 + H3O+ (Tính axit)
2. Tác dụng với dung dịch kiềm: (nhận biết ion amoni, điều chế amoniac trong phòng thí nghiệm)
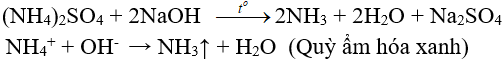
3. Phản ứng nhiệt phân
- Muối amoni chứa gốc của axit không có tính oxi hóa khi nung nóng bị phân hủy thành NH3.
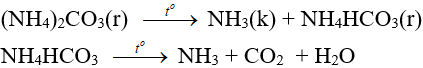
NH4HCO3 (bột nở) được dùng làm xốp bánh.
- Muối amoni chứa gốc của axit có tính oxi hóa khi bị nhiệt phân cho ra N2, N2O.
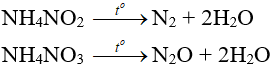
- Nhiệt độ lên tới 500oC, ta có phản ứng:
2NH4NO3 → 2N2 + O2 + 4H2O

